生命理工学系 News
難治性悪性脳腫瘍の中性子捕捉治療に有望な薬剤の開発
従来の1/50の投与量で高い腫瘍治療効果を実現
要点
- 葉酸受容体αリガンドとアルブミンリガンドを持った新規ホウ素薬剤を開発。
- 悪性脳腫瘍細胞が高選択的かつ高濃度にホウ素を取り込むことを実証した。
- CED法によって、既存の1/50倍のホウ素薬剤投与量で高い治療効果を実現。
概要
東京工業大学 科学技術創成研究院 化学生命科学研究所の中村浩之教授(ライフエンジニアリングコース主担当)の研究グループは、大阪医科薬科大学 医学部 脳神経外科学教室の川端信司准教授の研究グループ、筑波大学 陽子線治療センターの中井啓准教授の研究グループ、および京都大学 複合原子力科学研究所の鈴木実教授と共同で、悪性脳腫瘍に高い治療効果を有する中性子捕捉療法用新規ホウ素薬剤PBC-IPの開発に成功した。
ホウ素中性子捕捉療法(BNCT)[用語1]は、がん細胞のみを選択的に殺傷する治療法として近年注目を集めている。特に、悪性度の高いグリオーマ[用語2]に代表される難治性悪性脳腫瘍の新たな治療法としてBNCTには大きな期待が寄せられている一方、グリオーマ細胞に高い集積性を示すホウ素薬剤の開発が急務となっていた。
本研究では、グリオーマ細胞に高発現している葉酸受容体αのリガンド[用語3]、アルブミンリガンド、ホウ素クラスターが連結されたホウ素薬剤「PBC-IP」を新たに開発した。PBC-IPは、臨床用ホウ素薬剤の10~20倍のホウ素送達能を持つとともに、顕著な腫瘍増殖抑制効果が得られた。また、convection-enhanced delivery(CED)法[用語4]によってPBC-IPをマウス脳内患部に局所投与し、中性子照射実験を行ったところ、既存法と比べてマウスの生存期間が増加することがわかった。さらに、通常のホウ素薬剤投与量の1/50の投与量で高い治療効果が得られることから、難治性悪性脳腫瘍の治療法の開発において、極めて大きなインパクトをもたらすことが期待される。
研究成果は6月29日付(現地時間)に国際学術雑誌「Journal of Controlled Release」に掲載された。
研究の背景と経緯
ホウ素中性子捕捉療法(BNCT)は、がん細胞が取り込んだホウ素-10(10B)と熱中性子の核分裂反応によって、がん細胞のみを選択的に殺傷する治療法として近年注目を集めている。特に、外科療法や通常の放射線療法で治療が困難な、悪性度の高いグリオーマに代表される難治性悪性脳腫瘍の新たな治療法としてBNCTには大きな期待が寄せられている。現在のところ、4-borono-L-phenylalanine(L-BPA)[用語5]が、薬事承認された唯一のBNCT用ホウ素薬剤であるが、グリオーマに対して十分な腫瘍治療効果を得るには、L-BPAよりも高いグリオーマ細胞へのホウ素取り込み能を有する薬剤の開発が望まれている。これまでに本研究グループは、葉酸受容体α(FRα)がグリオーマ細胞に高発現することに着目し、FRαのリガンドである葉酸の部分構造(pteroyl基)と、12個のホウ素原子を含むdodecaborateが結合したPBCs[用語6]を開発している(Cells, 2020, 9, 1615)。また、血中のアルブミンと結合しやすいiodophenyl基とdodecaborateを結合させることで、血中アルブミンのenhance permeability and retention(EPR)効果[用語7]を利用してホウ素薬剤の血中滞留性と腫瘍集積性を高めることにも成功している(Bioorg. Med. Chem. Lett. 2022, 72, 128869)。
研究成果
本研究では、上述の背景に基づき、FRαリガンド(pteroyl基)、アルブミンリガンド(iodophenyl基)、ホウ素源(dodecaborate)が連結されたpteroyl-closo-dodecaborate-conjugated 4- (p-iodophenyl) butyric acid (PBC-IP) を新たに開発した(図1)。ヒトおよびラット由来グリオーマ細胞へのPBC-IPの取り込み能を評価したところ、L-BPAよりも10~20倍多くのホウ素が取り込まれることがわかった。そこで、グリオーマの中でも特に悪性度の高いグリオブラストーマ細胞を移植したマウスにPBC-IPを尾静脈投与し、中性子照射を行ったところ、顕著な腫瘍増殖抑制効果が得られ、同用量のL-BPAを投与した群よりも有意に腫瘍増殖を抑制していた。
さらに、グリオーマラットモデルを用いて、convection-enhanced delivery(CED)法によってPBC-IPを脳内患部に局所投与し、中性子照射実験を行った。L-BPA投与群は、生存期間中央値が37日であったのに対し、PBC-IP投与群の生存期間の延長効果は極めて高く、180日が経過しても全体の50%が生存した(図2)。さらに、PBC-IPとL-BPAを併用した群では、180日経過後も全体の70%が生存した。長期間生存したラットの脳を組織染色し観察したところ、腫瘍細胞が残存していないことが明らかとなった(図2)。
PBC-IPは、静脈投与とCED法による局所投与のどちらにおいても、グリオーマおよびグリオブラストーマ動物モデルにおいて、優れた腫瘍治療効果を示した。特に、CED法によるPBC-IPの局所投与においては、通常のホウ素薬剤投与量の1/50の投与量で高い治療効果が得られており、難治性悪性脳腫瘍の治療法の開発において、極めて大きなインパクトをもたらすことが期待される。
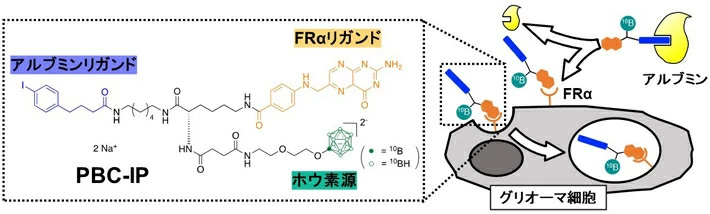
- 図1. Pteroyl-closo-dodecaborate-conjugated 4- (p-iodophenyl) butyric acid (PBC-IP) の分子デザインと細胞内取り込みの概要
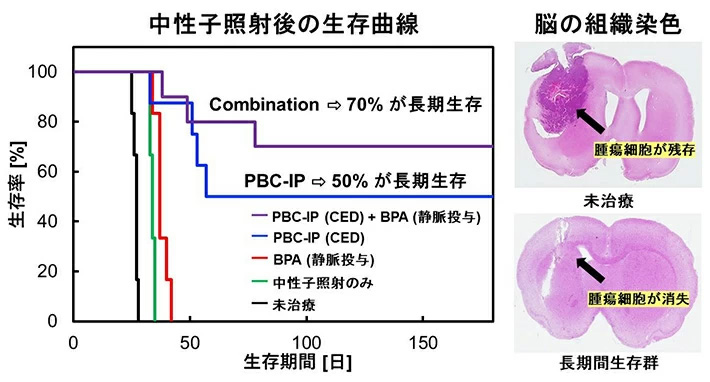
- 図2. (A)PBC-IPをラットグリオーマモデルにCED法で投与し中性子照射を行った後の生存曲線(B)長期生存したラットと未治療ラットの脳組織染色画像
社会的インパクト
グリオーマの中で特に悪性度の高いグリオブラストーマは、発見からの5年生存率が10%以下と、全てのがんの中でも予後が悪い難治性がんである。外科療法、化学療法、放射線療法はどれもグリオブラストーマに対する有効性が低く、有効な治療法はまだ確立されていない。本研究で開発したPBC-IPを用いたBNCTは、ヒトグリオブラストーマ皮下移植マウスモデルにおいて、高い腫瘍成長抑制効果を示し、さらに、CED法を用いた脳内局所投与によって、ラットグリオーマ同所モデルの70%において腫瘍が消失するといった、極めて高い治療効果を発揮した。本研究は、現行療法では困難なグリオブラストーマの治療に新たな可能性を示した点において、大きな社会的インパクトをもたらすと考えられる。
今後の展開
L-BPAとは異なる細胞取り込み機構を有するPBC-IPは、L-BPAが効かないがんに対する有効なホウ素薬剤としてBNCTの適応疾患を拡大し、グリオブラストーマのみならず他の難治性がんの治療にも大きく貢献することが期待される。今後、PBC-IPの取り込み機構を詳細に解析することで、グリオーマ治療のための新たな薬剤設計が可能になると考えられる。
- 付記
本研究は、日本医療研究開発機構(AMED)次世代がん医療創生研究事業(20cm0106262h0002)ならびに橋渡し研究プログラム(22ym0126070h0001)の支援を受けて行われた。
- 用語説明
[用語1] BNCT(Boron Neutron Capture Therapy; ホウ素中性子捕捉療法) : がん細胞に高集積させたホウ素-10(10B)と熱中性子の核分裂反応によって生じるα線とLi原子核によって、がん細胞を選択的に殺傷する放射線療法。浸潤がんにも有効。
[用語2] グリオーマ : 神経細胞とともに脳を構成するグリア細胞が腫瘍化した悪性脳腫瘍の一種。正常組織に浸潤し悪性度の高いものはグリオブラストーマと呼ばれ、治療が極めて困難。グリオブラストーマと診断された患者の生存期間中央値は14.6ヵ月であり、2年生存率は30%。
[用語3] リガンド : 生体分子と特異的に結合し、複合体を形成する物質。一般的には、受容体タンパク質やDNAと結合することで、何らかの生理機能を発揮する低分子、イオン、ペプチドなどを指す。
[用語4] CED(Convection-Enhanced Delivery)法 : 薬剤を脳細胞間隙に局所注入し高濃度かつ広範囲の薬剤分布を得る、臨床試験段階にある新たな薬剤送達法。カテーテルを用いて脳内の患部局所へ薬剤を持続投与するため、血液脳関門をバイパスすることができ、効率的な脳実質内薬物送達を可能とする投与方法として注目されている。
[用語5] L-BPA(4-borono-L-phenylalanine) : ボロン酸を有するアミノ酸誘導体で、一般名はボロファラン(10B)。がん細胞に高発現するL-アミノ酸トランスポーター1(LAT1)を介して細胞内に取り込まれる。2020年に頭頸部がんに対するBNCTが承認され保険収載されている。
[用語6] PBCs : 当研究室で開発された、葉酸の部分構造であるpteroyl基とホウ素クラスターであるdodecaborateが、アミノ酸リンカーを介して結合したホウ素薬剤。グリオブラストーマ由来細胞を含むFRα陽性細胞に効率的に取り込まれることがわかっている。
[用語7] EPR(Enhanced Permeability and Retention)効果 : 腫瘍組織において、高分子の集積性と滞留性が正常組織よりも向上する効果。腫瘍組織の血管壁およびリンパ管が未成熟であることに起因する。1986年に当時熊本大学の松村保広先生と前田浩先生によって発見された。
- 論文情報
| 掲載誌 : | Journal of Controlled Release |
|---|---|
| 論文タイトル : | Efficient neutron capture therapy of glioblastoma with pteroyl-closo-dodecaborate-conjugated 4- (p-iodophenyl) butyric acid (PBC-IP) |
| 著者 : | K. Nishimura, H. Kashiwagi, T. Morita, Y. Fukuo, S. Okada, K. Miura, Y. Matsumoto, Y. Sugawara, T. Enomoto, M. Suzuki, K. Nakai, S. Kawabata*, H. Nakamura* |
| DOI : | 10.1016/j.jconrel.2023.06.022 |
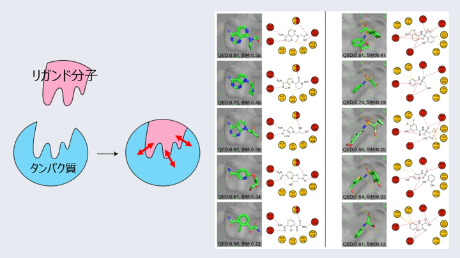
- “構造活性相関転移”による低分子医薬品候補の設計|生命理工学系 News
- ナノ空間で制御可能なヒスチジン残基化学修飾を開発|生命理工学系 News
- 膨大な活性データの網羅的解析から低分子医薬品候補を創出|生命理工学系 News
- 副反応を起こしやすいアミノ酸を迅速かつクリーンに連結 —抗HIV抗菌ペプチドの大量生産に道—|生命理工学系 News
- 中性子捕捉療法のための有望なホウ素薬剤を開発 —マウスのがんで、高い治療効果を確認—|生命理工学系 News
- 【研究室紹介】 中村・岡田研究室|生命理工学系 News
- 中村・岡田研究室
- 中村浩之 Hiroyuki Nakamura|研究者検索システム 東京工業大学STARサーチ
- 化学生命科学研究所
- 生命理工学院 生命理工学系
- 大阪医科薬科大学 脳神経外科学教室
- 筑波大学附属病院 陽子線治療センター
- 京都大学 複合原子力科学研究所
- 研究成果一覧
お問い合わせ先
東京工業大学 科学技術創成研究院 化学生命科学研究所
教授 中村浩之
E-mail : hiro@res.titech.ac.jp
Tel 045-924-5244 / 045-924-5976(研究所事務室)