生命理工学系 News
オートファジーの暴走による過剰な細胞核分解を防ぐ仕組みの発見
2つのオートファジー経路の連携という新たな視点
ポイント
- 細胞核の一部を分解するオートファジー経路(ヌクレオファジー)の破綻が細胞死を引き起こす仕組みを解明
- 異なる2つのヌクレオファジー経路の一方が停止すると、もう一方の経路が過剰に活性化されることを発見
概要
東京科学大学(Science Tokyo)※ 総合研究院 細胞制御工学研究センターの李子洋大学院生(研究当時)、中戸川仁教授(ライフエンジニアリングコース 主担当)らの研究チームは、オートファジーによる細胞核の選択的分解経路(ヌクレオファジー)の破綻が細胞死を引き起こす仕組みを解明しました。
酵母細胞には、"マクロ"ヌクレオファジー[用語1]および"ミクロ"ヌクレオファジー[用語2]の2つの異なるヌクレオファジー経路が存在します。研究チームは以前の研究で、マクロヌクレオファジーの停止した細胞では、栄養飢餓時の生存率が顕著に低下することを見出しましたが、細胞が死に至る理由は不明でした。
本研究では、マクロヌクレオファジーの停止がミクロヌクレオファジーの過剰亢進を引き起こすことを発見しました。さらに、ミクロヌクレオファジーによる過剰な核成分の分解が細胞死の主要な原因となっていることを明らかにしました。
本研究は、適切に制御された安全なヌクレオファジーの重要性を示しています。そして、オートファジーの活性制御機構の理解において、2つの異なるオートファジー関連経路間での制御という新たな視点を提示するものです。
本成果は、12月17日付(ロンドン現地時間)の「Nature Communications」誌に掲載されました。
※2024年10月1日に東京医科歯科大学と東京工業大学が統合し、東京科学大学(Science Tokyo)となりました。
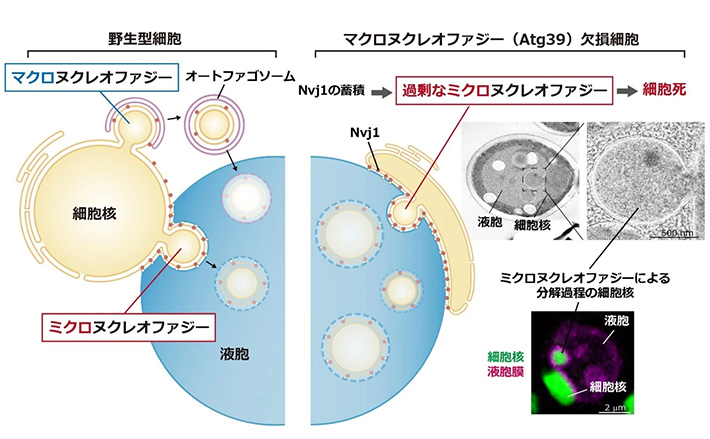
図1. マクロヌクレオファジーの停止によるミクロヌクレオファジーの過剰亢進
背景
不用となった細胞内成分の適切な分解・除去は細胞機能の維持に必須であり、そうした分解システムの異常は神経変性疾患等の発症に密接に関連します。オートファジーは栄養飢餓などで誘導される細胞内の分解機構であり、"ミクロ"オートファジーと"マクロ"オートファジーの2つの経路に大別されます。ミクロオートファジーでは、分解コンパートメントであるリソソームや液胞の膜が陥入して、分解対象を直接隔離・分解します。一方、マクロオートファジーでは、オートファゴソーム[用語3]と呼ばれる膜構造で分解対象を隔離した後にリソソームや液胞に運び入れます。
当研究チームは以前の出芽酵母を用いた研究で、マクロオートファジーによる細胞核の選択的分解機構(マクロヌクレオファジー)の存在を明らかにしました。細胞核はゲノムDNAの格納・複製や、遺伝子発現などの役割を担う巨大な細胞小器官ですが、マクロヌクレオファジーではAtg39タンパク質を介して細胞核の一部がオートファゴソームに積み込まれ、液胞内で分解されます。Atg39を欠損した細胞は、栄養飢餓条件において細胞核の形態が異常になり、野生型よりも早く生存率が低下することから、マクロヌクレオファジーは栄養飢餓への適応に重要であることが分かっていました。しかしながら、栄養飢餓時になぜ細胞核の一部を分解する必要があるのか、またマクロヌクレオファジーの停止が細胞核の形態異常や生存率の低下をどのようにして引き起こすのかは不明でした。
研究成果
研究グループは今回の研究で、栄養飢餓にさらしたAtg39欠損細胞の蛍光イメージング解析により、マクロヌクレオファジーが停止すると、細胞核の内容物を含む巨大な構造体が液胞内に取り込まれることを見出しました。その際には、液胞膜が陥入しながら核由来の構造体を液胞内に取り込むことが確認されました。そこで"ミクロ"ヌクレオファジーに必要なNvj1を欠損させると、構造体の取り込みが停止したことから、マクロヌクレオファジーの停止がミクロヌクレオファジーの過剰な亢進を引き起こしていることが明らかになりました。
核膜タンパク質であるNvj1は、栄養飢餓時にAtg39依存的なマクロヌクレオファジーによって分解されており、今回解析したAtg39欠損細胞ではNvj1が蓄積することで過剰なミクロヌクレオファジーを引き起こしたことから、正常細胞ではマクロヌクレオファジーがミクロヌクレオファジーの暴走を抑制していることが分かりました。さらに、Nvj1の欠損によって過剰なミクロヌクレオファジーを停止させると、Atg39欠損細胞における細胞核の形態異常や生存率の低下がほぼ完全に回復することも確認されました。つまり、マクロヌクレオファジーの停止によって過剰かつ致死的なミクロヌクレオファジーが惹起されること、そしてミクロヌクレオファジーの活性抑制がマクロヌクレオファジーの重要な役割の1つであることが明らかになりました。
出芽酵母の細胞核(直径約1.5-2 μm)に対し、マクロヌクレオファジーで分解される部分は小さい(直径0.15 μm以下)ですが、過剰なミクロヌクレオファジーで分解される部分は直径1 μmを越えるものもあるなど非常に大きく、DNA結合タンパク質や核小体タンパク質が内包されています。そのため、ミクロヌクレオファジーが制御不能となると、生存に必須の核成分が液胞内に取り込まれてしまうことで細胞が死に至る可能性や、核内での遺伝子発現に影響を及ぼすことで細胞が栄養飢餓に適応できなくなる可能性が考えられます。
社会的インパクト
細胞核のタンパク質の品質管理は、神経変性疾患等との関連性からも重要ですが、一方で細胞核は染色体などの生命に必須な構造体を格納しており、細胞核成分の分解は厳密に制御されている必要があります。本研究により明らかにしたヌクレオファジーの過剰亢進と細胞死の関係性は、制御された安全なヌクレオファジーの重要性を示しており、関連疾患を理解するうえでの基盤情報として有用になると期待されます。
今後の展開
本研究により、過剰亢進したミクロヌクレオファジーによって細胞が死に至ることが明らかとなりました。しかし、どの核成分の液胞への取り込みが細胞死の引き金を引くのか、そして細胞死に至るまでにどのようなプロセスがあるのかは不明のままです。今後の研究により、ミクロヌクレオファジーの異常が細胞死を引き起こす詳細なメカニズムの解明が期待されます。
これまでは、マクロオートファジーとミクロオートファジーそれぞれの分子基盤や生理機能に関する研究が進められてきた一方で、2つのオートファジー経路の連携や関係性についてはほとんど明らかにされていませんでした。本研究により、マクロヌクレオファジーがミクロヌクレオファジーの暴走を抑制する制御機構として働くという両者のつながりが明らかとなってきました。今後は、細胞核以外のオルガネラの分解においてもマクロオートファジーとミクロオートファジー間の制御機構が存在する可能性など、さらなる研究の広がりが期待されます。
- 付記
本研究は、文部科学省科学研究費助成事業(中戸川仁:17H01430, 19H05708, JP23K20044, JP24H00553)、革新的先端研究開発支援事業AMED-CREST(中戸川仁:JP21gm1410004)、武田科学振興財団研究助成(中戸川仁)、「東⼯⼤の星」⽀援【STAR】(中戸川仁)、による支援を受けて行われました。
- 用語説明
[用語1] マクロヌクレオファジー:細胞核の一部を選択的に分解するマクロオートファジー経路。核膜上に存在するAtg39が分解の目印として働き、細胞核とオートファゴソーム膜をつなぐことで、核の一部をオートファゴソームに積み込む。
[用語2] ミクロヌクレオファジー:細胞核の一部を選択的に分解するミクロオートファジー経路。Nvj1などのタンパク質を介して形成される核膜と液胞膜の接触領域が、液胞側に陥入して液胞膜が閉じることで、核の一部が液胞内に取り込まれる。
[用語3] オートファゴソーム:マクロオートファジーの進行過程で形成される膜構造。お椀型の膜構造が分解対象を取り囲むように進展し、閉じることで分解対象を隔離する。完成したオートファゴソームは、様々な分解酵素を含むリソソームまたは液胞と融合し、内容物が分解される。
- 論文情報
| 掲載誌: | Nature Communications |
|---|---|
| 論文タイトル: | Macronucleophagy maintains cell viability under nitrogen starvation by modulating micronucleophagy |
| 著者: | Ziyang Li, Keisuke Mochida, Hitoshi Nakatogawa |
| DOI: | 10.1038/s41467-024-55045-9 |
研究者プロフィール
李 子洋 Ziyang LI
東京科学大学 総合研究院 細胞制御工学研究センター 大学院生
研究分野:ヌクレオファジー
中戸川 仁 Hitoshi NAKATOGAWA
東京科学大学 総合研究院 細胞制御工学研究センター 教授
研究分野:オートファジーの分子細胞生物学的研究
関連ページ
- オートファゴソームを柔軟な網で覆うように形作る仕組み|生命理工学系 News
- オートファゴソームの“口”を大きくする因子を発見|生命理工学系 News
- オートファゴソームを効率よく作る仕組みを発見|生命理工学系 News
- オートファゴソーム膜を伸ばす仕組みを解明|生命理工学系 News
- オートファジーによる小胞体分解の分子メカニズムを解明|生命理工学系 News
- オートファゴソームに脂質を供給する仕組みを解明|生命理工学系 News
- オートファゴソーム前駆体を小胞体につなぎとめる|生命理工学系 News
- 細胞の核と小胞体を分解する新しい仕組みを発見|旧・東京工業大学
- 前田和彦准教授と中戸川仁准教授が第13回日本学術振興会賞を受賞|旧・東京工業大学
- 平成27年度「東工大の星」支援STAR 採択者決定|生命理工学系 News
- 中戸川 仁 Hitoshi Nakatogawa|研究者検索システム Science Tokyo STAR Search
- 中戸川研究室
- 総合研究院 細胞制御工学研究センター
- 総合研究院|大学組織一覧|Science Tokyoについて
- 生命理工学院 生命理工学系
お問い合わせ
東京科学大学 総合研究院 細胞制御工学研究センター
教授 中戸川仁
Tel 045-924-5735
Fax 045-924-5743
E-mail hnakatogawa@cbc.iir.isct.ac.jp