生命理工学系 News
オートファゴソームに脂質を供給する仕組みを解明
オートファジーにまつわる数十年来の謎が明らかに
要点
- オートファジーにおいて、分解対象を包む袋状の膜(オートファゴソーム)が作られる際の材料(リン脂質)がどのように供給されるのか、これまで分かっていなかった
- たんぱく質Atg2がリン脂質を直接輸送する活性を持ち、オートファゴソーム前駆体にリン脂質を供給することで膜伸長を起こすことを発見した
- オートファゴソーム形成の分子機構が明らかとなり、オートファジーを制御する特異的制御剤の開発が加速すると期待される
概要
微生物化学研究所の野田展生 部長、大澤拓生 博士研究員らは、オートファジーを担うたんぱく質群の1つであるAtg2が2つの脂質膜[用語1]の間で脂質の輸送を担う活性があることを発見し、その活性がオートファゴソーム[用語2]を作るための脂質供給を行うことを明らかにしました。
細胞内のたんぱく質を分解する仕組みの1つであるオートファジーにおいて、オートファゴソームの形成は分解対象を決定する極めて重要なステップですが、オートファゴソームを作るための脂質供給の仕組みはこれまで分かっていませんでした。
本研究グループは、オートファゴソームの前駆体膜(隔離膜)と小胞体膜の接点に局在するAtg2が、リン脂質[用語1]を収容するポケットを持つことをX線結晶構造解析法[用語3]で明らかにしました。さらに試験管内でAtg2の活性を調べた結果、Atg2が2つの膜をつなぎ止め、両者の間でリン脂質の輸送を担う活性を持つことを明らかにしました。そしてこの活性を失った変異体は酵母におけるオートファジーを強く阻害しました。以上の結果から、Atg2は脂質輸送を担う新奇たんぱく質であり、その活性を用いて小胞体などの細胞内脂質膜からオートファゴソーム前駆体へと脂質を直接輸送し、オートファゴソームの形成に働くという全く新しい仕組みが明らかになりました。
本研究により、オートファジーの要であるオートファゴソームの形成過程の基本原理が明らかとなり、今後のオートファジーの特異的制御剤の開発に向けた基盤となることが期待されます。
本研究は、東京工業大学の大隅良典 栄誉教授、中戸川仁 准教授、小谷哲也 研究員、および東京大学の鈴木邦律 准教授のグループと共同で行いました。
本研究成果は、2019年3月25日(英国時間)に英国科学誌「Nature Structural& Molecular Biology」のオンライン速報版で公開されました。
本成果は、以下の事業・研究領域・研究課題によって得られました。
科学技術振興機構(JST)戦略的創造研究推進事業 チーム型研究(CREST)
研究領域: |
「ライフサイエンスの革新を目指した構造生命科学と先端的基盤技術」 (研究総括:田中啓二 東京都医学総合研究所 理事長) |
|---|---|
研究課題名: |
「オートファジーの膜動態解明を志向した構造生命科学」 |
研究代表者: |
野田展生(微生物化学研究会 微生物化学研究所 部長) |
研究期間: |
平成25年4月~平成31年3月 |
JSTは本領域で、先端的ライフサイエンス領域と構造生物学との融合により、ライフサイエンスの革新につながる「構造生命科学」と先端基盤技術の創出を目指します。
上記研究課題では、オートファゴソーム形成に働くたんぱく質群が膜の上で繰り広げる相互作用を構造生物学的に明らかにすることで、オートファゴソーム形成機構の分子論的解明を目指します。
研究の背景と経緯
オートファジーは細胞内の主要な分解経路であり、有害なたんぱく質凝集体や傷ついたミトコンドリアなどの分解を通して、細胞の恒常性維持に働いています。そしてオートファジーの異常は神経変性疾患やがんなど、重篤な疾病を引き起こすことが知られています。すなわち生体にとって極めて基本的かつ重要な現象であり、そのメカニズムを知ることは疾病の治療・予防法の開発のために欠かせません。オートファジーの最大の特徴は、オートファゴソームと呼ばれる二重膜のオルガネラを新たに作り出す点にあります。オートファゴソームに包まれたものは全て細胞内分解の場所であるリソソームへと運ばれ分解されることから、オートファゴソームを作る過程がオートファジーによる分解対象を決定づけます。しかしオートファゴソームの形成過程は、依然として多くの謎に満ちており、中でもオートファゴソームの膜を作るための材料であるリン脂質の供給方法は全く分かっていませんでした。
リン脂質の供給源には、小胞体が有力な候補として挙げられています。しかしリン脂質は不溶性であり、細胞質を自由に移動できないことから、それをオートファゴソーム形成の材料として使うためには何らかの移動手段が必要になると考えられていました。
研究の内容
オートファゴソームの形成は、多くのAtgたんぱく質[用語4]が担っています。本研究グループは、Atgたんぱく質のうち、伸長中のオートファゴソーム前駆体(隔離膜)と小胞体の接点に局在することが知られているAtg2に着目し、その構造と機能の解明を進めました。まずX線結晶構造解析法を用いて、Atg2の一部分の立体構造を初めて高分解能で決定することに成功しました。その結果、Atg2には大きな疎水性のポケットがあること、そのポケットを使ってリン脂質を脂質膜から引き抜き、収容できることを見いだしました。
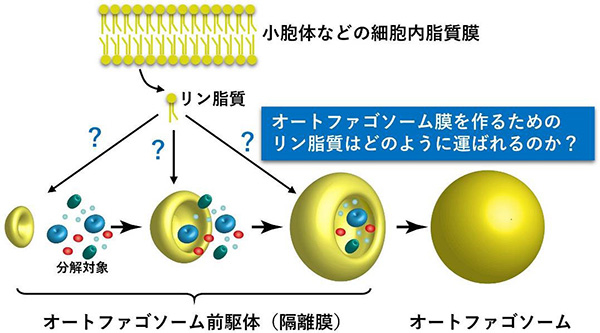
図1. オートファゴソーム形成過程の模式図
オートファジーが誘導されると、細胞質中に突如膜構造が出現し(隔離膜)、それが分解対象を包み込みながら伸長し、閉じてオートファゴソームとなる。隔離膜が伸長するためには膜の材料となるリン脂質が必要であり、小胞体などから供給されると考えられてきたが、その運び方はこれまで謎であった。
次にAtg2が持つ機能を試験管内で調べました。蛍光脂質を組み込んだ人工脂質膜(リポソーム)を用いた解析の結果、本研究グループはAtg2がリポソーム同士をつなぎ止めるとともに、つなぎ止めたリポソーム間でリン脂質の受け渡しをするという新奇活性を持つことを世界で初めて明らかにしました。このリン脂質の受け渡し活性は、Atg2の特定のアミノ酸に変異を入れることで失われますが、同じ変異を酵母内のAtg2に入れたところ、オートファゴソームが形成できないことが分かりました。すなわち試験管内で見られたAtg2の脂質輸送活性は、実際のオートファジーにおけるオートファゴソームの形成に働いていることが明らかとなりました。Atg2は小胞体と隔離膜の接点に局在することから、小胞体からリン脂質を引き抜き、直接隔離膜へと輸送することでオートファゴソーム形成のための材料を提供していると考えられます。またオートファゴソームの膜は通常のオルガネラには豊富に見られる膜たんぱく質がほとんど含まれないという特徴があります。それは長年の謎でもありましたが、Atg2はリン脂質のみの移動を許可し、他のたんぱく質などが隔離膜へ流入するのを防ぐ役割も担っていると考えられます。
従来、オートファゴソーム形成のためのリン脂質供給の仕組みとして、小胞輸送を介したモデルや、小胞体膜が直接隔離膜につながることで脂質が移動するモデルなどが考えられてきました。今回明らかとなった、新奇脂質輸送たんぱく質であるAtg2を介したリン脂質の供給は、オートファゴソーム形成の仕組みとして全く考えられてこなかったものであり、オートファジーの基礎研究に劇的な変化を起こすような、画期的な成果であると考えられます。
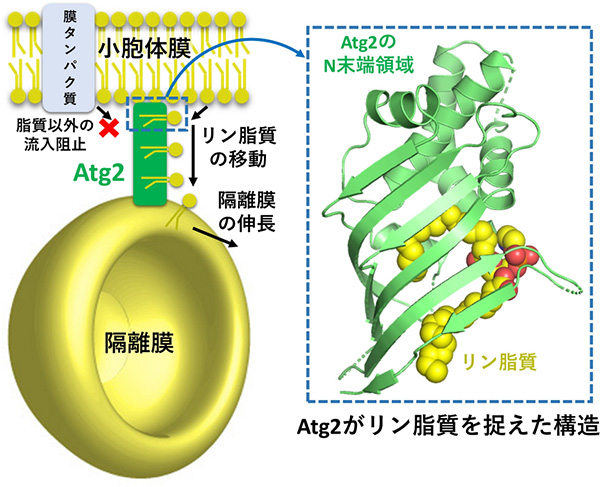
図2. Atg2による小胞体から隔離膜へのリン脂質の供給モデル
Atg2は伸長中の隔離膜の先端に局在し、小胞体と隔離膜をつなぎ止める。さらにAtg2は小胞体からリン脂質を引き抜き、それを隔離膜側へと送り込むことで隔離膜伸長を引き起こす。Atg2はまた、小胞体の脂質以外の成分(膜たんぱく質など)が隔離膜に流入するのを防ぐ役割も担っていると考えられる。
今後の展開
オートファジー分野における積年の課題であった脂質供給機構が明らかになったことで、オートファゴソーム形成の分子機構の完全理解に向けた研究が加速されることが期待されます。そしてオートファゴソーム形成機構の理解が深まることで、オートファジーの人為的制御を介したさまざまな疾病の治療・予防法の開発研究が促進されることが期待されます。さらに今回見いだした「たんぱく質を介した脂質輸送による脂質膜の新生」は、オートファジー分野のみならず、細胞生物学全般において初めて明らかとなった現象であり、細胞生物学の基礎研究全般の推進に貢献する成果です。
用語説明
[用語1] リン脂質と脂質膜 : リン脂質とはリン酸エステルを持つ脂質の総称で、親水性の部分と疎水性の部分の両方を持つ。疎水性の部分があるため単独では水に溶けないが、疎水性部分を向かい合わせて脂質二重層を形成することで水溶液中でも安定して存在できる。細胞のさまざまな脂質膜は主にリン脂質からなる脂質二重層で作られている。
[用語2] オートファゴソーム : オートファジーが誘導されると、細胞質に新たに作り出される二重膜のオルガネラ。オートファゴソームが取り囲んだもの(さまざまなたんぱく質や核酸など)はすべて分解の場であるリソソーム(酵母の場合は液胞)へと輸送され、リソソーム内の分解酵素群の働きで分解される。
[用語3] X線結晶構造解析法 : 結晶はX線を回折する性質があるが、この性質を利用して結晶の構成物の原子がどのように立体的に配列しているのかを決定する手法。たんぱく質は結晶になる性質があるため、たんぱく質の立体構造を明らかにするために広く利用されている。
[用語4] Atgたんぱく質 : 酵母で同定されたオートファジーを制御するたんぱく質群の名称で、これまでに40種類以上報告されている。Atgの後におおよそ同定された順に通し番号がつけられている。Atgたんぱく質群のうち、栄養飢餓時のオートファゴソーム形成に重要なものは18種類である。
論文情報
| 掲載誌 : | Nature Structural& Molecular Biology |
|---|---|
| 論文タイトル : | Atg2 mediates direct lipid transfer between membranes for autophagosome formation |
| 著者 : | Takuo Osawa1, Tetsuya Kotani2, Tatsuya Kawaoka3, Eri Hirata3, Kuninori Suzuki3,4,5, Hitoshi Nakatogawa2, Yoshinori Ohsumi6, Nobuo N. Noda1* |
| 所属 : |
1Institute of Microbial Chemistry (BIKAKEN), Tokyo, Japan. 2School of Life Science and Technology, Tokyo Institute of Technology, Yokohama, Japan. 3Department of Integrated Biosciences, Graduate School of Frontier Sciences, University of Tokyo, Kashiwa, Japan. 4Life Science Data Research Center, Graduate School of Frontier Sciences, University of Tokyo, Kashiwa, Japan. 5Collaborative Research Institute for Innovative Microbiology, University of Tokyo, Tokyo, Japan 6Cell Biology Center, Institute of Innovative Research, Tokyo Institute of Technology, Yokohama, Japan. |
| DOI : | 10.1038/s41594-019-0203-4 |
- オートファゴソーム前駆体を小胞体につなぎとめる│生命理工学系 News
- 細胞の核と小胞体を分解する新しい仕組みを発見│東工大ニュース
- 新しいMOOC「オートファジー」を世界に向けて公開│生命理工学系 News
- オートファジー-ノーベル賞を受賞した大隅栄誉教授の研究とは│生命理工学系 News
- 顕微鏡観察がすべての出発点~あらゆる生物に備わる生存戦略「オートファジー」と出会って~ ― 大隅良典|研究ストーリー|研究
- 前田和彦准教授と中戸川仁准教授が第13回日本学術振興会賞を受賞│東工大ニュース
- 中戸川研究室―研究室紹介 #7―│生命理工学系 News
- 中戸川仁研究室
- 大隅研究室
- 研究者詳細情報(STAR Search) - 中戸川仁 Hitoshi Nakatogawa
- 研究者詳細情報(STAR Search) - 大隅良典 Yoshinori Osumi
- 東京工業大学 科学技術創成研究院 (IIR)
- 科学技術創成研究院 細胞制御工学研究センター
- 研究成果一覧
大隅良典栄誉教授が「オートファジーの仕組みの解明」により、2016年ノーベル生理学・医学賞を受賞しました。受賞決定後の動き、研究概要をまとめた特設ページをオープンしました。
お問い合わせ先
研究に関すること
微生物化学研究会 微生物化学研究所 構造生物学研究部 部長
野田展生
E-mail : nn@bikaken.or.jp
Tel : 03-3441-4173 Fax : 03-6455-7348
JSTの事業に関すること
科学技術振興機構 戦略研究推進部 ライフイノベーショングループ
川口哲
E-mail : crest@jst.go.jp
Tel : 03-3512-3524 Fax : 03-3222-2064