生命理工学系 News
牛乳や血液をそのまま薄めず標的分子を検出できる免疫センサーを開発
持ち運び簡単な紙デバイスへの加工で「その場」分析を実現
ポイント
- ナノボディと生物発光酵素を組み合わせて熱や変性に強い免疫センサーを開発。
- 生物発光を利用することで、希釈していない牛乳や血液の中の標的分子を検出。
- 肉眼でも青から赤への発光色変化を確認できる紙デバイスを実現。
概要
東京科学大学(Science Tokyo)※ 総合研究院 化学生命科学研究所の北口哲也准教授(ライフエンジニアリングコース 主担当)、朱博助教(ライフエンジニアリングコース 主担当)、安田貴信助教(ライフエンジニアリングコース 主担当)、同生命理工学院 生命理工学系のYANG Yinghui(ヤン・インホイ)大学院生(博士後期課程2年)、井上暁人(博士後期課程・当時)らの研究チームは、抗原を混ぜるだけで発光色が青から赤へ変化する頑強な生物発光免疫センサーBRET nano Q-bodyの開発に成功しました。さらに、この免疫センサーを持ち運びが容易な紙デバイスに加工することで、どこでも手軽に分析できるようになりました。
免疫測定法[用語1]は、抗原抗体反応を使って試料中のごくわずかな物質を特異的に測定する方法で、病気の診断や食品の安全管理、環境調査などで重要な役割を果たしています。近年では特に、患者の傍らでリアルタイムに診断して治療の方針を決める臨床現場即時検査(Point of Care Testing:POCT)[用語2]の重要性が増しており、より安定で簡便かつ素早く抗原を検出できる免疫センサーの開発が求められています。
本研究で開発した免疫センサーは、抗体の中でも特に頑強性に優れたナノボディ[用語3]を活用することで、熱や変性などの条件下でも安定的に機能します。また光の散乱や自家蛍光による影響が蛍光よりも小さい生物発光を利用しているため、牛乳や血液といった不透明な懸濁液を希釈せずに標的分子を検出できます。さらに、この免疫センサーをろ紙に染み込ませたあと、凍結乾燥により紙デバイスに加工したところ、室温で1カ月放置したあとでも抗原を検出可能であることが確認できました。この免疫センサーの生物発光シグナルは、肉眼やスマートフォンなどでも確認できるため、ベッドサイドだけでなく、野外や家などでの「その場」分析にも大きく貢献することが期待されます。
本成果は、11月11日付(現地時間)の「ACS Sensors」誌に掲載されました。
※2024年10月1日に東京医科歯科大学と東京工業大学が統合し、東京科学大学(Science Tokyo)となりました。
背景
免疫測定法は、抗体が抗原を特異的に認識し、高い親和性で結合するという性質を生かした微量物質の測定法です。この測定法は、高価な分析装置を使わずに、試料の中に含まれるごくわずかな物質を高精度で検出できるため、病気の診断や薬物の血中濃度モニタリングだけでなく、食品の品質管理や環境汚染の調査などさまざまな分野で活躍しています。最近では、病気の早期発見と治療が患者の回復に大きく影響するという観点から、患者の傍らで即座に検査できるPOCTの需要が増しており、より簡単に操作でき、どんな場所でも素早く結果が得られる免疫センサーの開発が求められています。
本研究チームはこれまで、POCTへの適用を目指した免疫センサーの開発に注力してきました。特に生物発光共鳴エネルギー移動(Bioluminescence Resonance Energy Transfer:BRET)[用語4]を利用したクエンチ抗体(Q-body)[用語5]は、肉眼でもシグナルを確認できる、2種類の光の強度比を取ることで誤差の小さい測定結果が得られる、検出装置が安価である、といった特長からPOCTとの相性がよく、実用化への期待が高まっていました。しかし、牛乳や血液など不透明な懸濁液の中に含まれる標的分子を検出する場合は、高濃度の夾雑物によって免疫センサーのシグナルが埋もれてしまったり、免疫センサー自体が不安定になったりするため、試料を希釈なしにそのままで検出することは困難でした。また、POCT用デバイスを作る過程で行う凍結乾燥や、輸送や非常時への備えで重要となる室温での長期保存が、免疫センサーの性能を低下させてしまうという課題もありました。
研究成果
本研究では、シグナルが夾雑物による影響を受けにくく、さらにセンサー自身が熱などのさまざまな過酷な条件に対して安定な生物発光免疫センサーBRET nano Q-bodyを開発しました。この免疫センサーは、ラクダ科動物に由来する重鎖抗体の可変領域(ナノボディ)に、赤色の蛍光色素TAMRAが化学修飾されており、さらにリンカーを介して青色の生物発光酵素NanoLuc[用語6]が融合されています(図1a)。ナノボディは高温下や変性条件下といったタンパク質にとって過酷な環境でも安定性が高く、NanoLucは明るい生物発光を示すという特長を持っています。これらの特長を生かすことで、POCTに適した、丈夫で長持ちし、かつ応答の大きい免疫センサーを作製できると考えました。なお生物発光は、励起光を必要としないこと、蛍光に比べて光散乱の影響が少ないことが知られています。そのため、生物発光を利用したこの免疫センサーは、よりシンプルな検出装置で操作でき、不透明な懸濁液への応用も視野に入れることができます。今回の研究ではモデルとして、抗がん剤の一つで、投与後の血中濃度モニタリングが必要なメトトレキサート(MTX)を認識するナノボディを用いることにしました。
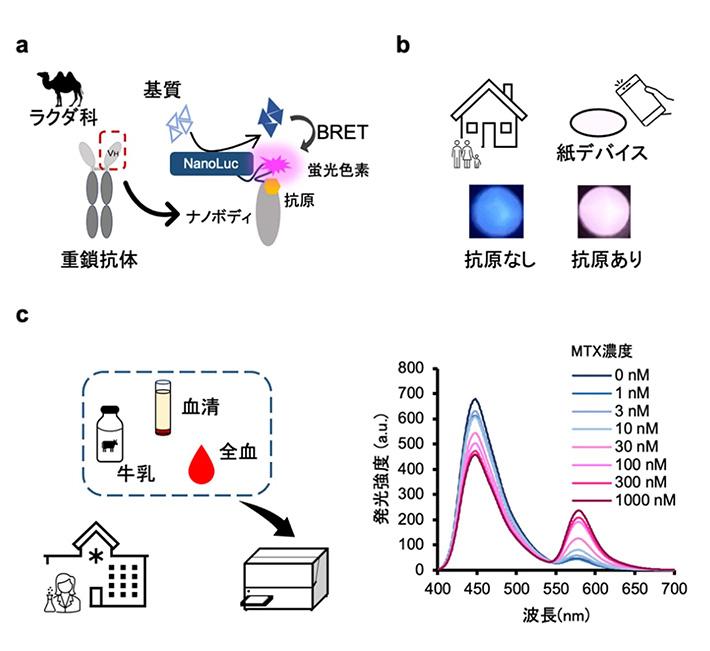
図1. BRET nano Q-bodyの概要(a)分子デザインと作動原理。(b)作製した紙デバイスをスマートフォンで撮影したときの抗原の有無による発光色の変化。(c)抗原を測定したときの濃度依存的な発光スペクトル変化。 DOI:10.1021/acssensors.4c01800より一部改変。
開発したBRET nano Q-bodyは、抗原が存在しないときはTAMRAが消光されてNanoLuc由来の青色の光を放ち、抗原が存在するとTAMRA由来の赤色の光を放ちました(図1b)。これは、抗原が結合するとTAMRAの消光状態が解除され、かつNanoLucとTAMRAの距離が近くなることで、NanoLucからTAMRAへのBRETが起きたためだと考えられます。さらに、NanoLucとナノボディの間の距離がBRETの効率に影響を与えると考えられることから、リンカーを最適化したところ、発光強度比(応答)がMTXの濃度依存的に最大7倍以上変化するBRET nano Q-bodyを作製することに成功しました(図1c)。応答が大きいことは安定な検出につながり、POCTへの適用に発展させることが可能となります。
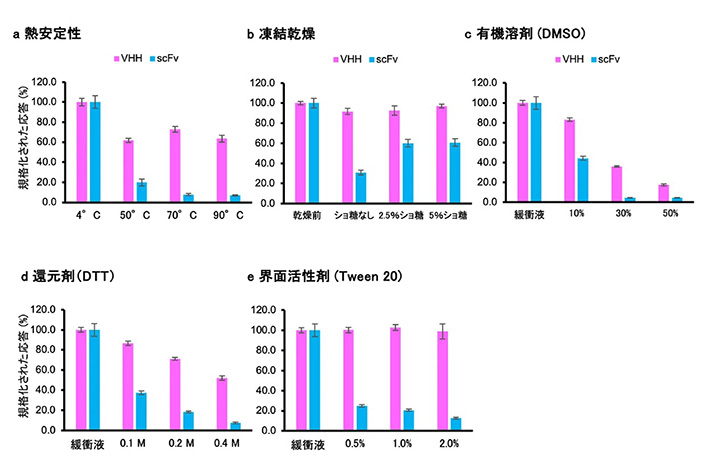
図2. BRET nano Q-bodyの頑強性評価(a)熱安定性。(b)凍結乾燥。(c)有機溶剤(DMSO)。(d)還元剤(DTT)。(e)界面活性剤(Tween 20)。DOI:10.1021/acssensors.4c01800より一部改変
次にBRET nano Q-bodyの頑強性を評価するために、熱や有機溶剤、還元剤、界面活性剤がセンサーの活性にどのように影響するかを調べました。その結果、以前に開発した、単鎖抗体(scFv)を使ったBRET Q-bodyと比べて、BRET nano Q-bodyは加熱後やDMSO、DTT、Tween20を含む溶液中でも、より厳しい条件下で活性を維持していることが分かりました。さらに、凍結乾燥してもほぼ100%の活性を保っており、BRET nano Q-bodyが非常に高い頑強性を持つことが確認できました(図2)。これらの結果から、この免疫センサーはPOCTに適していると考えられます。
続いて、BRET nano Q-bodyが、生体試料や環境水のような夾雑物を多く含む試料でも抗原を検出できるかを調べました。特に不透明で夾雑物の影響が大きいと考えられる懸濁液として牛乳と血液を選択しました。まずMTXを牛乳および血液に添加した疑似的なサンプルを用意し、いずれも希釈せずにこの免疫センサーと混合することで、試料中のMTXの検出を試みました。その結果、どちらの試料でも、緩衝液で測定した場合と比べて発光強度そのものは小さくなるものの、ほぼ同等の応答が得られ、MTXの濃度依存的に変化しました(図3)。このことから、この生物発光を利用した免疫センサーによって、従来の蛍光センサーでは困難であった不透明な懸濁液における検出が可能であることが確認できました。
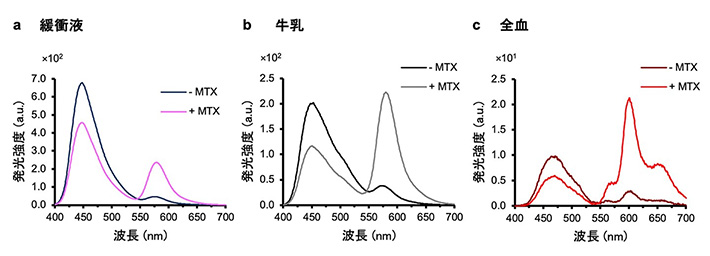
図3. さまざまな溶液中のBRET nano Q-bodyの発光スペクトル(a)緩衝液。(b)牛乳。(c)血液(全血)。DOI:10.1021/acssensors.4c01800より一部改変。
最後に、BRET nano Q-bodyをさまざまな場所で手軽に活用できるよう、ろ紙に染み込ませて凍結乾燥させた紙デバイスに加工しました。この紙デバイスに基質とともにMTXを加えると発光色が変化し、その変化はスマートフォンのカメラだけでなく、肉眼でも確認できました(図4a)。さらに、全血、血清、牛乳などの生体試料を希釈せずに使用しても、緩衝液で測定した場合と同様の検出限界と高い応答を示しました(図4b)。この紙デバイスは、25℃で1カ月保存しても性能を維持しており、POCTに利用するデバイスとしても実用的であることが分かりました。将来的には、診断や治療にとどまらず、さまざまな分野での応用が進むと予想され、医療から日常生活まで幅広い活用が期待されます。
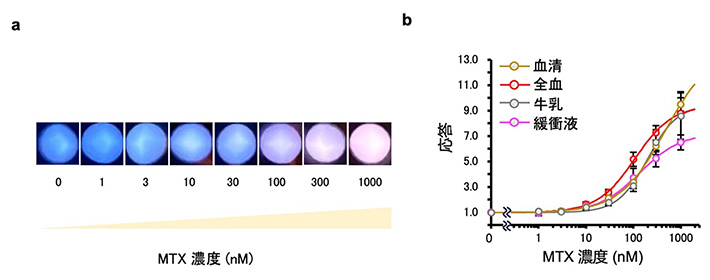
図4. (a)スマートフォンのカメラで撮影した紙デバイスの発光色の変化。(b)生体試料に添加したMTXを紙デバイスで検出したときの濃度依存曲線。DOI:10.1021/acssensors.4c01800より一部改変。
社会的インパクト
BRET nano Q-bodyは、ELISA[用語7]のような煩雑な洗浄操作を行うことなく、ただ混ぜるだけで簡単に抗原を検出できます。さらに、この免疫センサーは紙デバイスにすることで、軽くて持ち運びやすくなります。そのため、野外や家のような大型の検出装置がない場所でも標的分子の測定ができるようになります。この技術は、POCTにとどまらず、食の安全や環境保護にも大いに役立つと考えられ、社会全体への大きな貢献が見込まれます。
今後の展開
BRET nano Q-bodyは、使用するナノボディを変えることで、理論的にはあらゆる抗原を検出できるようになります。この特長を生かし、今後は今回用いたMTXのような低分子薬剤だけでなく、ホルモンや病気のマーカーとなるタンパク質、さらにはウイルスの検出が可能なBRET nano Q-bodyの開発を進めていく予定です。そして、さらに技術を進化させることで、より高感度で精度の高い免疫センサーを開発し、ELISAや免疫クロマトグラフィーでは実現し得ない測定を可能にする革新技術としての地位の確立を目指します。
- 付記
本研究は、科学研究費助成事業(課題番号:JP22H05176、JP24K01264、JP21K14468、JP24H01123)、次世代研究者挑戦的研究プログラム(課題番号:JPMJSP2106)の支援を受けて行われました。
- 用語説明
[用語1] 免疫測定法:抗原と抗体の反応を利用して、特定の分子を検出・定量する手法の総称で、臨床検査、食品分析、環境調査など幅広い分野で使用されている。
[用語2] 臨床現場即時検査(Point of Care Testing、POCT):患者の傍らで医療従事者が簡易な装置や試薬を使って素早く行う検査。
[用語3] ナノボディ:ラクダ科動物に由来する重鎖のみからなる抗体(重鎖抗体)の可変領域ドメイン。12 – 15 kDaとサイズが小さく安定であるという特長から、診断薬や治療薬の材料として注目されている。
[用語4] 生物発光共鳴エネルギー移動(Bioluminescence Resonance Energy Transfer、BRET):発光物質と蛍光物質が近接するときに、発光物質が光を放出するために使うエネルギーが蛍光物質に移動する現象。BRETが起こると発光物質由来の波長の光が弱くなり、蛍光物質由来の波長の光が強くなる。
[用語5] クエンチ抗体(Quenchbody、Q-body):部位特異的に蛍光色素修飾された抗体あるいは抗体断片。抗原が結合していないとき、蛍光色素は抗体内のトリプトファンからの光誘起電子移動によって消光状態となるが、抗原が結合すると消光が解除される。
[用語6] NanoLuc:深海エビ(Oplophorus gracilirostris)由来の発光酵素で、460 nm付近にピークを持つ強い青色の光を放つ。サイズが19 kDaと比較的小さく、ホタル由来の発光酵素と比べて100倍以上明るいという特長がある。
[用語7] ELISA:Enzyme-Linked Immunosorbent Assayの略で、試料に含まれる目的の抗原や抗体を酵素反応によって定量する免疫測定法。高い感度と特異性を持つ反面、検出までの工程が長く時間がかかる。
- 論文情報
| 掲載誌: | ACS Sensors |
|---|---|
| 論文タイトル: | BRET Nano Q-body: A Nanobody-Based Ratiometric Bioluminescent Immunosensor for Point-of-Care Testing |
| 著者: | Yinghui Yang, Akihito Inoue, Takanobu Yasuda, Hiroshi Ueda, Bo Zhu, Tetsuya Kitaguchi* |
| DOI: | 10.1021/acssensors.4c01800 |
関連ページ
- 幼少期の脳における記憶維持にはたらくオステオクリン|生命理工学系 News
- 抗体と混ぜるだけで抗原を素早く検出!病気やアレルギーの検査をより手軽に|Science Tokyoニュース
- 抗体と混ぜるだけで洗浄不要の免疫測定法を実現する新たな測定素子を開発|生命理工学系 News
- 引張り力で体中の蛍光色が変わるマウスの作出に成功|生命理工学系 News
- 10^5個以上の菌株を数日で選別するタンパク質分泌生産株ハイスループットスクリーニング法を開発|生命理工学系 News
- 赤色蛍光タンパク質型cGMPセンサーの開発と多色イメージングへの応用|生命理工学系 News
- 赤色蛍光タンパク質型グルコースセンサーの開発|生命理工学系 News
- 緑色蛍光タンパク質型乳酸センサーとピルビン酸センサーの開発|生命理工学系 News
- 新規緑色蛍光タンパク質型グルコースセンサーを開発|生命理工学系 News
- 生命活動の燃料「ATP」を観察する3色の蛍光センサーの開発に成功|生命理工学系 News
- 令和5年度 手島精一記念研究賞の受賞者決定|生命理工学系 News
- 令和4年度手島精一記念研究賞の授与式を挙行|生命理工学系 News
- 北口哲也 Tetsuya Kitaguchi|研究者検索システム Science Tokyo STAR Search
- 朱博 Bo Zhu|研究者検索システム Science Tokyo STAR Search
- 安田貴信 Takanobu Yasuda|研究者検索システム Science Tokyo STAR Search
- 北口哲也研究室
- 総合研究院 化学生命科学研究所
- 生命理工学院 生命理工学系
- 総合研究院|大学組織一覧|Science Tokyoについて
- 生命理工学院|大学組織一覧|Science Tokyoについて