生命理工学系 News
人工細胞の分裂のタイミングや順序の制御による分子コンピューティングを実証
自己複製する人工細胞やRNA診断をする液滴コンピュータの実現に期待
要点
- DNA液滴で作製した人工細胞の分裂のタイミングや順序を分子反応によって時間的に制御することに成功
- がんのバイオマーカーとなるマイクロRNAの濃度差を判断する分子コンピューティング機能を持った人工細胞を実現
- 制御された多段階の複製ができる人工細胞や、病気の診断を行う分子コンピュータや知的な人工細胞などへの応用に期待
概要
東京科学大学* 情報理工学院 情報工学系および総合研究院 自律システム材料学研究センターの瀧ノ上正浩教授(生命理工学コース 副担当)、生命理工学院 生命理工学系の丸山智也大学院生(博士後期課程3年)、公婧大学院生(研究当時)らの研究グループは、DNA液滴[用語1]を用いて作った人工細胞[用語2]の分裂のタイミングや順序の制御に成功し、がんのバイオマーカーとなるマイクロRNA(miRNA)[用語3]の濃度比較を行う分子コンピューティングへ応用した。
核酸(DNA、RNA) 、タンパク質、脂質などの生体分子を組み合わせて作られる人工細胞は、生細胞モデルや分子コンピュータなどを通じて、次世代の医療やコンピュータへの応用が期待されている。人工細胞の分裂のタイミングや順序が制御できると、自己複製などの複雑な細胞機能を構築することや、複雑な分子情報処理の手順をプログラムすることが可能になる。本研究で人工細胞の構築に用いたDNA液滴では、分子のセンシングをトリガーにした分裂などは確認されているが、分裂のタイミングや順序の制御はこれまで実現していなかった。
本研究では、RNAや酵素を用いた分子反応によって、DNA液滴の分裂現象に要する時間を制御する機構を開発し、DNA液滴の多段階分裂における分裂順序の制御に成功した。さらに、マイクロRNAの濃度によって分裂の順番が変わるようにプログラミングし、その濃度差を判断する分子コンピューティング機能を持つ人工細胞を構築した(図1)。
本研究で開発された技術は、よく制御された多段階の分裂を示す自己複製が可能な人工細胞や、生体内で特定の分子の検出を行う自律型分子ロボット[用語4]の開発に貢献すると考えられる。
本研究成果は、2024年8月27日(英国時間)に英国科学誌「ネイチャー・コミュニケーションズ(Nature Communications)」![]() で公開された。
で公開された。
*2024年10月1日に東京医科歯科大学と東京工業大学が統合し、東京科学大学(Science Tokyo)となりました。
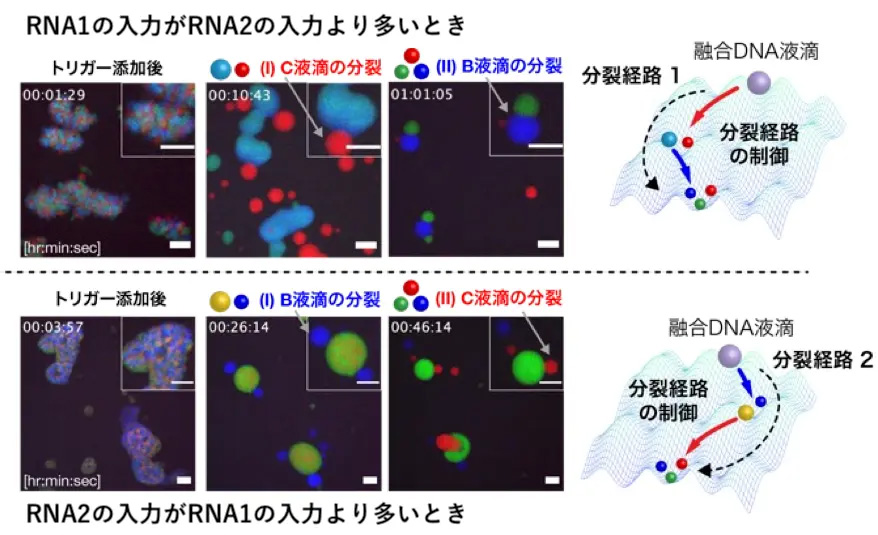
図1. DNA液滴による人工細胞の分裂順序制御による分子コンピューティングの概要。分裂する経路を確認することで、がんのバイオマーカーであるマイクロRNA (miRNA) の濃度の比較を行うことができる。
背景
近年、脂質やタンパク質、核酸分子(DNA・RNA)などの生体分子を組み合わせることで、生細胞の機能を模した人工細胞を創る取り組みが広く行われている。人工細胞は、複雑な生命現象を理解するための単純な生細胞モデルとしての利用や、生体内での病気の診断や治療を行う分子ロボットなどへの応用が期待されている。このような用途をさらに拡げるためには、人工細胞の機能を向上させる必要があり、そのために人工細胞が動的に変化する現象をプログラムする技術の構築が求められている。人工細胞の変形や分裂のタイミングや、その順序を制御できれば、生細胞が持つ細胞周期のような多段階の制御された分裂機構が再現でき、そこから自己複製などの複雑な細胞機能を構築できる。また、人工細胞にあらかじめプログラムした複数の機能の発動の順番を制御できるようになるため、より複雑な分子情報処理の手順をプログラムすることも可能になり、高機能な細胞型の分子コンピュータの構築にもつながる。
DNA液滴は、Y字型やX字型などの分岐構造を持つDNAナノ構造の自己集合で形成される、流動性のある細胞サイズ(直径数十µm)の球形の凝集体(液滴)であり、人工細胞としての利用が期待されている[参考文献1]。DNA液滴は分子反応によって分裂でき、さらに分裂現象を利用して、AND演算機能などの分子コンピューティング機能を構築できることも報告されている[参考文献2]。しかし、これまでにDNA液滴が分裂するタイミングや順序などの時間的な現象の制御は実現されていなかった。
研究成果
本研究グループは、DNA液滴の分裂に要する時間を制御する機構を開発し、DNA液滴の多段階分裂における分裂経路の制御を実現した。また、DNA液滴の多段階分裂を利用し、DNA液滴に対して、がんのバイオマーカーであるマイクロRNAの濃度比較を行う分子コンピューティング機能を実装することに成功した(図2)。
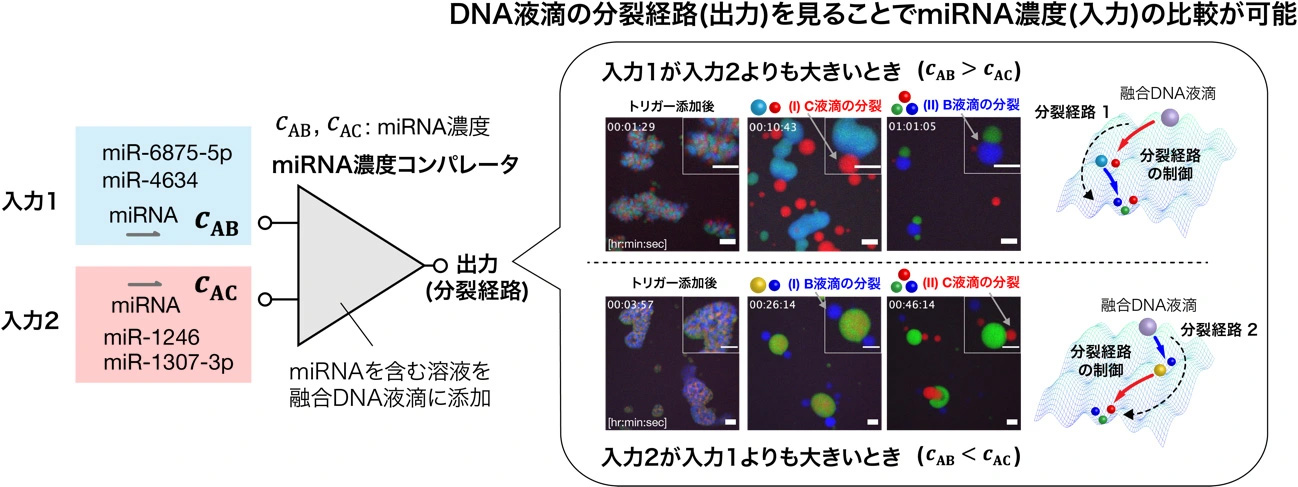
図2. 融合DNA液滴の分裂経路制御を利用した分子コンピューティング機能の概要図。分裂経路を確認することで、がんのバイオマーカーであるマイクロRNA(miRNA)の濃度の比較を行うことができる。
(1)融合DNA液滴の形成と分裂時間の制御
DNA液滴は、DNAナノ構造体が粘着末端同士の結合を介して自己集合することで形成される。お互いに結合しない2種類のY字型DNAナノ構造体(YA, YB)と、両方の粘着末端を持ち、YAとYBを架橋するリンカーDNAナノ構造体(リンカー)を自己集合させることで形成される融合DNA液滴(図3a)は、1本鎖DNAである分裂トリガーが引き起こす鎖置換反応[用語5]によってリンカーが切断されることで、YA由来のDNA液滴(A液滴)と YB由来のDNA液滴(B液滴)に分裂することが知られている[参考文献1](図3b)。そこで研究グループは、酵素反応を用いて分裂トリガーの生成を時間制御し、リンカーの切断速度を変化させることで、融合DNA液滴の分裂に要する時間を制御できると考えた。
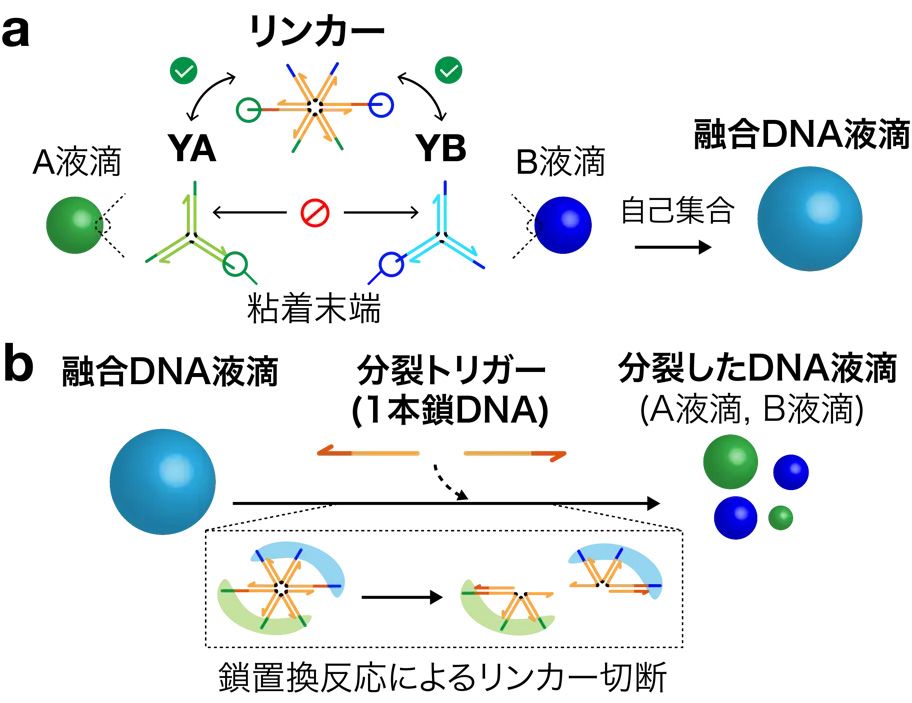
図3. (a) 融合液滴の作製図。 (b) 融合DNA液滴の分裂。
このリンカーの切断速度を変化させるための反応として、「時間遅れ回路」を設計した(図4a)。時間遅れ回路は、(i) 分裂トリガー(1本鎖DNA)と阻害RNA(マイクロRNA)の結合による不活性トリガーの形成、(ii) リボヌクレアーゼH(RNase H)[用語6]による不活性トリガーから分裂トリガーの生成、の2つの反応によって構築される。これらの反応の速度を変化させることで、分裂トリガーの生成速度が制御され、結果的にDNA液滴の分裂の速度が制御される。本研究では、YA, YBと、2種類のリンカーナノ構造体(Lα, Lβ)を自己集合させることで形成される融合DNA液滴を用いた(図4b)。ここでは、Lβの切断速度が時間遅れ回路で変化する(図4c)。阻害RNA濃度を上げると、(i) の反応が促進されることでDNA液滴の分裂が遅くなることが確認されたことから(図4d)、時間遅れ反応を用いることで分裂に要する時間を制御できることが示された。
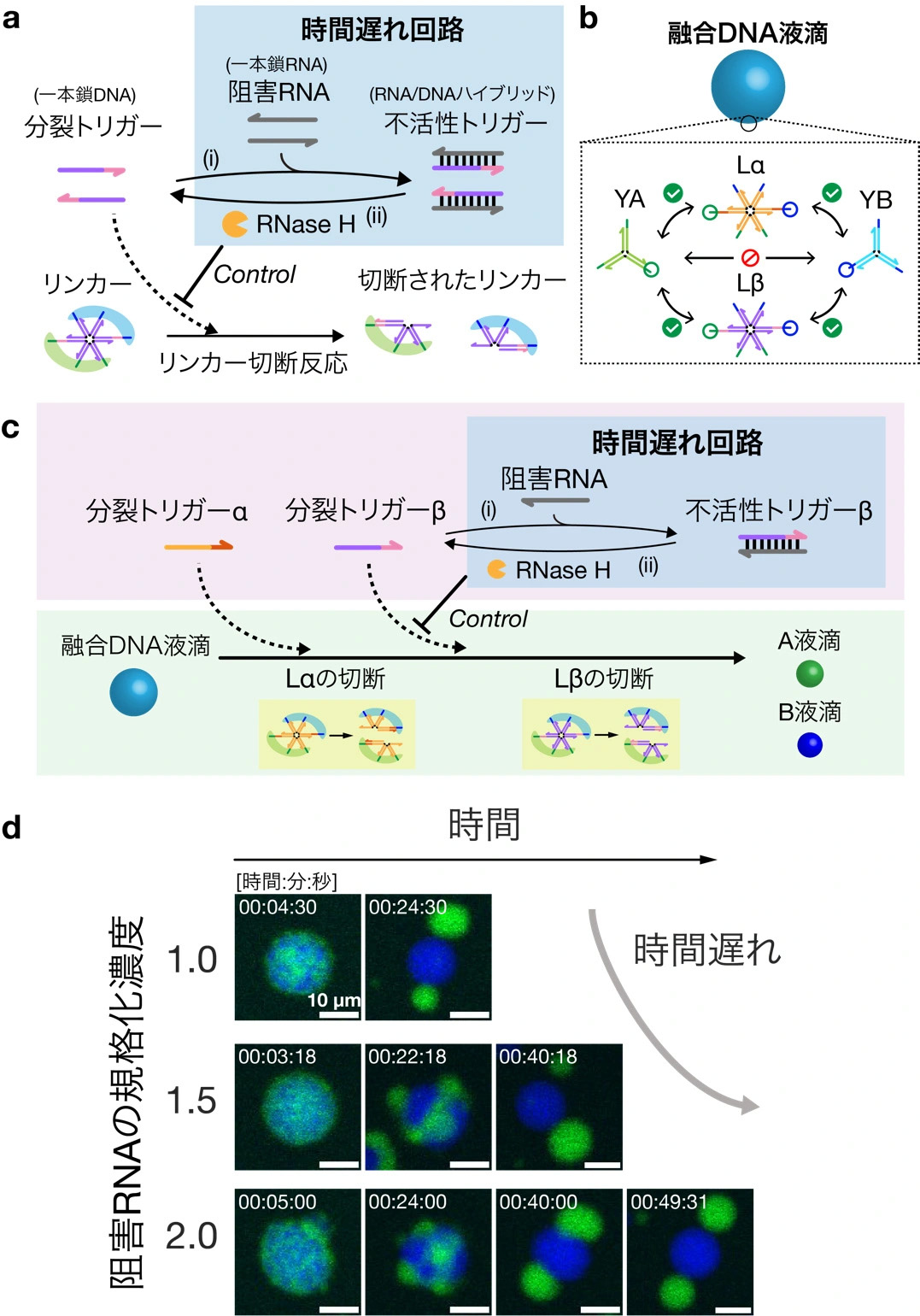
図4. 融合DNA液滴の分裂時間の制御。(a) 時間遅れ反応の模式図。(i) 分裂トリガーが阻害RNAと結合して不活性化トリガーを形成する反応、(ii) 不活性トリガーがリボヌクレアーゼH(RNase H)と反応して分裂トリガーが生成される反応によって構成される。(b) 融合DNA液滴の形成図。(c) 融合DNA液滴の分裂時間制御。(d) 融合DNA液滴の分裂の顕微鏡画像。スケールバーは10 µm。
(2)DNA液滴の多段階分裂の経路制御
次に、融合DNA液滴の多段階分裂における分裂経路の制御を行った。本実験で用いた融合DNA液滴(ABC液滴) は、3種類のY字型DNAナノ構造体(YA, YB, YC)と2種類のリンカー(Lβ, Lγ)によって形成されており、リンカーの分裂によってA液滴, B液滴, C液滴の3種類の液滴に分裂する(図5a, b)。このとき、2種類のリンカーが切断される順番によって、融合DNA液滴は異なる分裂経路をたどる(図5a)。具体的には、時間遅れ回路によってLβがLγの後に切断される場合は、分裂経路1をたどり、C液滴が分裂した後にB液滴が分裂する(図5c、上図)。一方で、LγがLβの後に切断される場合は、分裂経路2をたどり、B液滴が分裂した後にC液滴が分裂する(図5c、下図)。実験では、時間遅れ反応を用いてリンカーの切断の順番を制御することによって、分裂経路1と分裂経路2をたどる分裂がそれぞれ起こった(図5d, e)。以上から、融合DNA液滴の多段階分裂における分裂経路の制御を実現した。
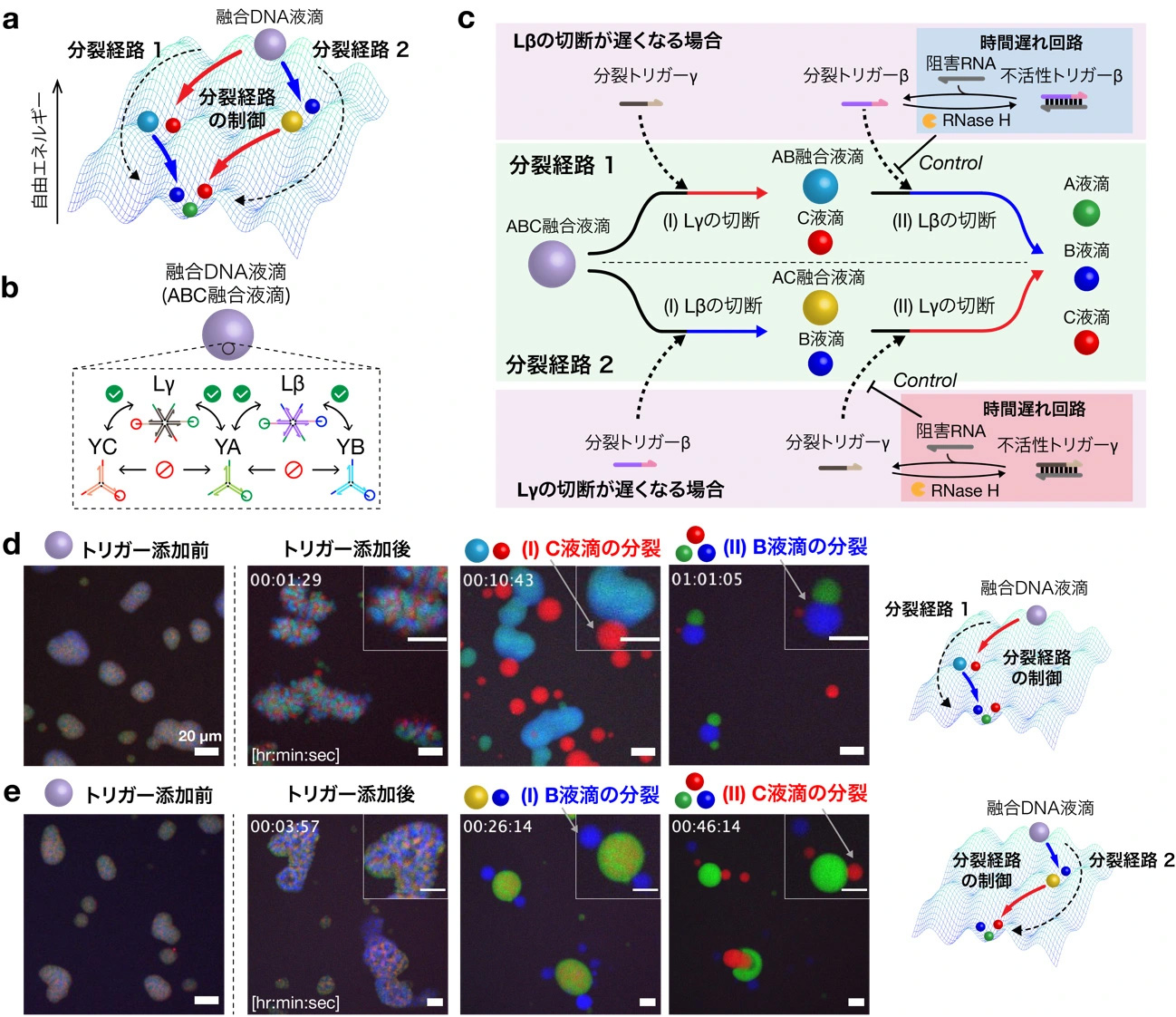
図5. 融合DNA液滴の多段階分裂の分裂経路制御。(a) 融合DNA液滴が3種類の液滴に分裂する過程の模式図。 (b) 融合DNA液滴(ABC融合液滴)の形成図。 (c) 時間遅れ反応によるABC融合DNA液滴の分裂経路の制御。 (d, e) DNA液滴分裂の顕微鏡観察画像。スケールバーは20 µm。
(3)DNA液滴分子コンピュータによるマイクロRNAの濃度の比較
最後に、多段階分裂の経路制御を利用し、がんのバイオマーカーとなるマイクロRNA(miRNA)の濃度を比較する、分子コンピューティング機能の構築を目指した(図6a)。LβとLγの両方のリンカーに対して時間遅れ回路を用いた反応系では、2つの時間遅れ回路の阻害RNAの濃度の差に応じてABC融合液滴の分裂経路が変わる(図6b, c)。ここで、LβとLγの阻害RNAの濃度を入力(入力1、入力2)、分裂経路を出力として見た場合、この反応系は2つの入力の大小に応じて異なる分裂経路を出力する分子コンピューティングとして働いている。このように複数の入力の大小によって出力が変わるコンピュータ素子はコンパレータ[用語7]と呼ばれており、今回の反応系はDNA液滴を用いた分子コンパレータとなっている。
また、本研究では、阻害RNAに乳がんのバイオマーカーとなるマイクロRNA(miRNA) を用いている。そのためDNA液滴は、乳がんのバイオマーカーとなるmiRNAのうち、どのmiRNAがより多く存在しているかを調べるためのセンシングシステムとしても働いている。実験での顕微鏡観察により、cABとcACの差がある閾値を超えたところで分裂の経路が変化することが分かった(図6d)。この結果から、融合DNA液滴の多段階分裂における分裂経路制御を用いることで、miRNAの濃度を比較可能な分子コンパレータを構築できることが示された。
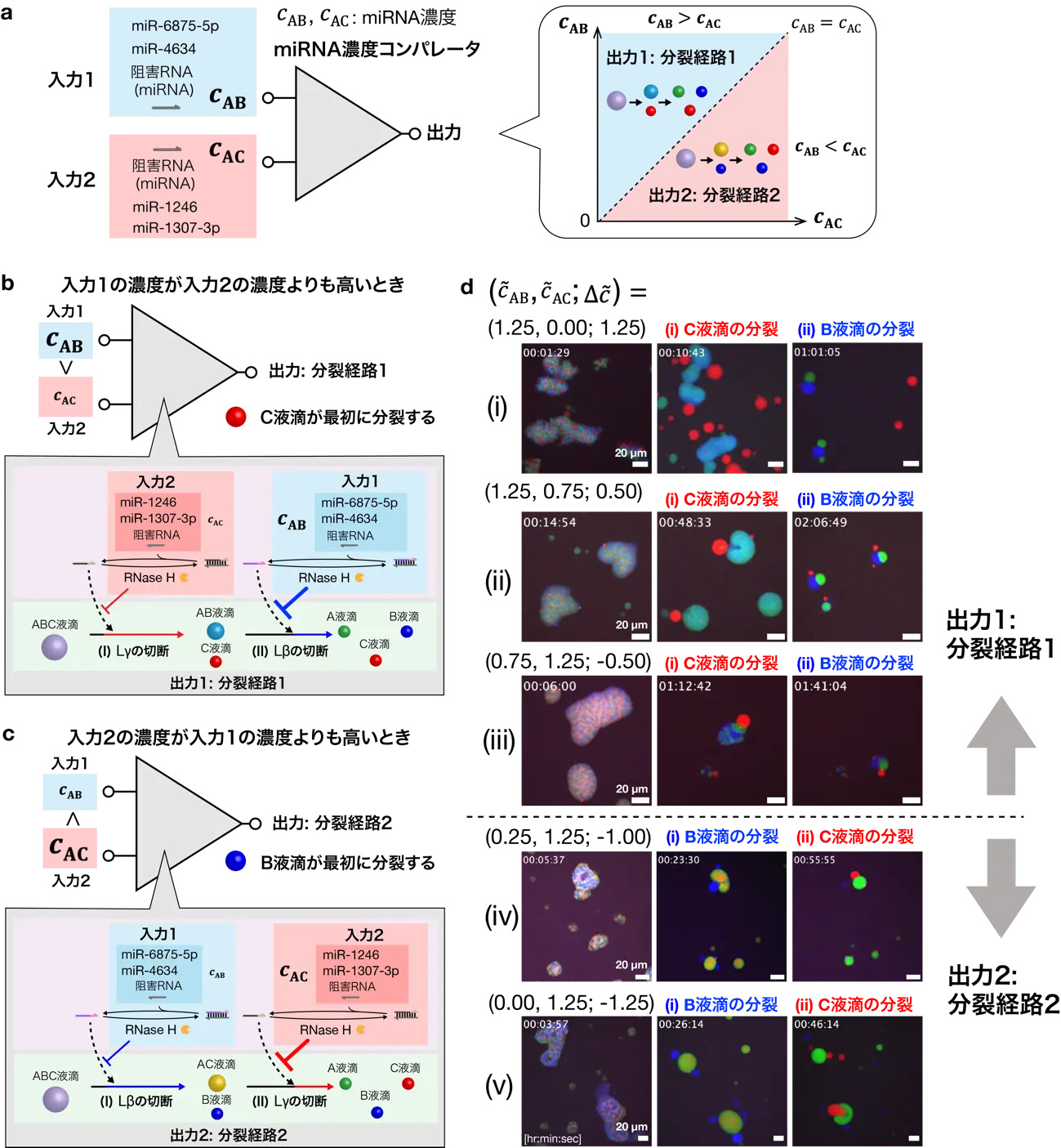
図6. 融合DNA液滴の多段階分裂を用いた「DNA液滴分子コンピュータ」の開発。(a-c) 分裂経路を出力とするmiRNA分子濃度コンパレータ。ここでは、cAB = cACのときに分裂の経路がスイッチする場合を示している。(d) 多段階分裂の顕微鏡画像。実験では、-0.5 < cAB - cAC < -1.0となるところで分裂経路がスイッチする結果が得られた。スケールバーは20 µm。
社会的インパクト
本研究成果は、バイオマーカーであるmiRNAを検出するがん早期診断技術への活用が見込まれる。ターゲットに応じた配列設計が可能であるため、今回用いた乳がんのバイオマーカーmiRNA以外にも、多種多様なRNAの検出が可能で、柔軟かつ汎用的な応用が期待される。また、複数の論理演算を組み合わせて、プログラム通り順序よく機能を発現させるような、より高度な論理回路を組み込んだ自律的なDNA液滴コンピュータへの展開も可能であり、生体内で治療する分子ロボットの開発などにも貢献できる。
今後の展望
本研究で示した時間制御可能な分裂機能は、非平衡系としての人工細胞の自己複製機能の実現において重要であるため、そうした機能を備えたDNA液滴の開発に貢献すると考えられる。また、DNA液滴を利用したmiRNAの検出によるがん診断やセンシングの研究がさらに発展すると考えられる。本研究は、miRNAの存在/非存在を調べる従来の機能に加えて、miRNA濃度を比較する機能も実現した。本研究では乳がんのバイオマーカーとなるmiRNAを用いたが、DNA液滴に用いるDNAの配列を適切に設計することにより、他の病気のバイオマーカーとなるmiRNAを検知できるようにプログラムすることも可能だと考えられる。
- 付記
本研究成果は、MEXT/JSPS科学研究費助成事業(Nos. JP20H05701, JP20H00619, JP20H05935, JP24H00070)、Human Frontier Science Program (HFSP; RGP0016/2022-102)、学術振興会特別研究員奨励費 (JP22KJ1346) の支援のもとで得られた成果である。
- 参考文献
-
[1]
「DNA液滴」の形成と制御に成功(東工大ニュース 2020年6月12日)

-
[2]
液滴の分裂によって、がんの可能性の有無を示す「DNA液滴コンピュータ」の開発に成功(東工大ニュース 2022年6月6日)

- 用語説明
[用語1] DNA液滴:Y字型やX字型などの分岐構造を持つDNAナノ構造が集まって作られるマイクロスケールの凝集体。DNA塩基配列の設計によって、安定性などの性質を制御したり、情報処理能力などを液滴に付与したりすることができる。
[用語2] 人工細胞:DNA、RNA、タンパク質、脂質などの生体分子によって構築される、細胞を模倣した小胞や微小液滴。
[用語3] マイクロRNA(miRNA):生細胞内に存在する18~25塩基程度の1本鎖RNA。がんなどの生命現象に関与していることが知られている。
[用語4] 分子ロボット:DNAやタンパク質などの生体分子によって構築され、分子センシング、分子コンピューティング、分子による運動や機械的動作が統合された、自律的な微小サイズのロボット。
[用語5] 鎖置換反応:トリガーとなる1本鎖DNA (P) が、2本鎖DNA (Q+R) の一方の鎖 (Q) と入れ替わることで、より安定な2本鎖DNA (P+R) が形成される反応。
[用語6] リボヌクレアーゼ H(RNase H):RNA分解酵素の一種。1本鎖DNAと1本鎖RNAが結合して形成される2本鎖構造のRNA/DNAハイブリッドのうち、RNAのみを分解する。
[用語7] コンパレータ:一般的には電子部品の1種であり、2つの入力の大小によって出力が切り替わる素子のことである。本研究では、2つの分子の濃度の大小によって動作(出力)が変わるように設計されている。
- 論文情報
| 掲載誌 : | Nature Communications |
|---|---|
| 論文タイトル : | Temporally controlled multistep division of DNA droplets for dynamic artificial cells |
| 著者 : | Tomoya Maruyama, Jing Gong, Masahiro Takinoue(丸山智也、公婧、瀧ノ上正浩) |
| DOI : | 10.1038/s41467-024-51299-5 |
- 複数のマイクロRNAを同時検出する「RNA液滴コンピュータ」の開発に成功|生命理工学系 News
- 酵素-DNA複合体ネットワークによる3種マイクロRNAの同時検出|生命理工学系 News
- 液滴の分裂によって、がんの可能性の有無を示す「DNA液滴コンピュータ」の開発に成功|生命理工学系 News
- 酵素反応が可能な細胞サイズの相分離DNAカプセルの構築に成功|生命理工学系 News
- エピゲノムの制御を受けた転写の方程式|生命理工学系 News
- 「DNA液滴」の形成と制御に成功|生命理工学系 News
- 粒子混雑効果による自発的なラチェット輸送に成功|生命理工学系 News
- DNAオリガミによる人工細胞微小カプセルの開発に成功|生命理工学系 News
- 骨格で支えられた人工細胞の形成に成功 薬用カプセルや化粧品などの応用に耐える補強が実現|東京工業大学
- 人工細胞の中でDNAをコンピュータとして使うことに成功―生体内で働く分子ロボットの実現に向けて―|東京工業大学
- 細胞を模倣した微小反応容器のコンピューター制御に成功―人工細胞や分子ロボットの開発に期待―|東京工業大学
- 令和4年度手島精一記念研究賞の授与式を挙行|生命理工学系 News
- 瀧ノ上正浩准教授が令和2年度 化学とマイクロ・ナノシステム学会 奨励賞を受賞|生命理工学系 News
- 東工大関係者9名が平成29年度科学技術分野の文部科学大臣表彰で「若手科学者賞」を受賞|東京工業大学
- DNAから人工細胞や分子ロボットをつくる-物質と生命の境界を探求-|生命理工学系 News
- 瀧ノ上正浩 Masahiro Takinoue|研究者検索システム Science Tokyo STAR Search
- 瀧ノ上研究室
- 情報理工学院 情報工学系
- 情報理工学院
- 生命理工学院
- 総合研究院
- 自律システム材料学研究センター
- 研究