生命理工学系 News
半分天然、半分人工の固体光合成材料を開発
CO2還元酵素を固体触媒化する結晶の細胞内合成に成功
要点
- タンパク質結晶にCO2還元酵素と光捕集分子を組み込んだ人工光合成固体触媒を開発。
- 細胞内タンパク質結晶化反応により、CO2還元酵素を自発的に内包した結晶の合成に成功。
- 有用な酵素と人工分子のハイブリッド機能化法として、さまざまな固体触媒開発への応用に期待。
概要
東京工業大学 生命理工学院 生命理工学系の潘鉄錚博士研究員と安部聡助教、マイティ・バスデブ特任助教、上野隆史教授(生命理工学コース 主担当)のグループは、細胞内タンパク質結晶化反応[用語1]を用いて、CO2還元活性を有するギ酸脱水素酵素(FDH)[用語2]と光増感剤であるエオシンY(EY)[用語3]の両方を組み込んだハイブリッド固体触媒の合成に成功した。
自然界に存在する酵素は、温和な環境下でも目的の反応を効率よく触媒する分子であり、近年の環境問題や地球温暖化の解決策の1つとして注目されている。また天然酵素など複数の機能性分子をタンパク質結晶にカプセル化した固体触媒には多くの応用が期待される。しかしこれまでのカプセル化では、単純な触媒反応を行う酵素に限られていた。
今回の研究では、細胞内タンパク質結晶化を応用した手法によって、CO2還元酵素FDHを内包したタンパク質結晶を効率的に合成することに成功した。このFDHを内包した複合結晶は、複雑な精製プロセスを必要とせず、容易に単離できる。またFDHを内包した複合結晶は再生利用可能で、熱的にも安定である。さらにこの結晶に光捕集分子であるEYを組み込むことで、天然分子と人工分子を組み込んだハイブリッド固体触媒を実現した。この研究成果は、天然分子と人工分子を融合させた設計戦略により、人工光合成を実現する安定性の高い環境低負荷型の固体触媒の合成が可能であることを示している。
本成果は、ナノ科学分野において権威のある学術誌「ナノレターズ(Nano Letters、米国化学会出版社)」のオンライン版で7月12日(現地時間)に公開された。
背景
タンパク質結晶は、ビルディングブロックであるタンパク質が規則正しく並んだ固体の集合体である。この特異な規則性が、高い安定性を有するバイオマテリアル素子としての可能性を拓くと期待されている。さらに、タンパク質結晶は多孔質構造を形成するため、ゲスト分子を内部に固定化することができる。これまでに、金属クラスター、金属錯体触媒、天然酵素などがタンパク質結晶に固定化されてきた。このタンパク質結晶に複数の機能性分子をカプセル化したハイブリッド材料が実現できれば、多くの応用が期待できる。
しかし、現在のタンパク質結晶のカプセル化システムで扱えるのは、低分子か、単純な触媒反応を行う酵素に限られており、ハイブリッド材料としての可能性は十分に検討されてこなかった。
研究成果
これまで研究グループは、タンパク質結晶へのさまざまな分子の内包と、その機能化に力を注いできた。しかし、タンパク質を大腸菌で合成した後、精製と結晶化を経てタンパク質結晶を得る従来の方法では、大量合成は実現できない。そこで本研究では、多角体[用語4]の細胞内タンパク質結晶化反応と遺伝子工学的手法を組み合わせることにより、複数の機能性分子を内包したハイブリッドタンパク質結晶材料を合成した。
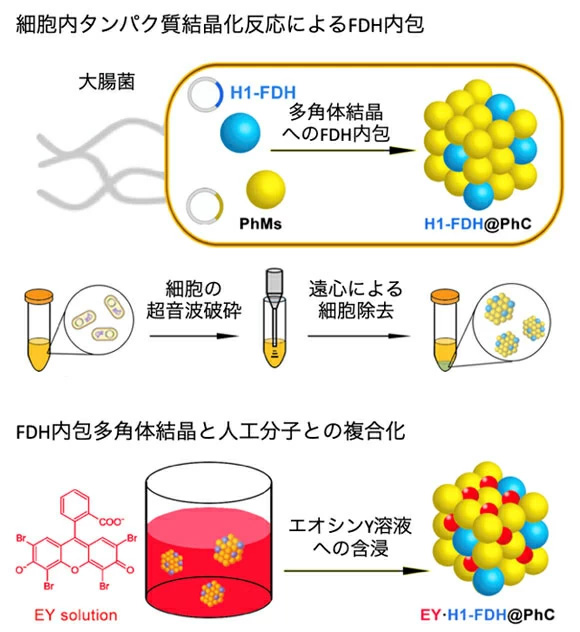
図1. 人工光合成を実現するハイブリッドタンパク質結晶材料の合成法
はじめに1つの大腸菌細胞内で、多角体タンパク質と生体分子であるH1-FDH(ギ酸脱水素酵素(FDH)に、多角体結晶(Polyhedrin Crystal: PhC)への取り込みを促進する構造(H1)を融合させた分子)を同時に産生させることによって、自発的にH1-FDHを内包した多角体複合結晶(H1-FDH@PhC)を得ることに成功した(図1上)。この多角体複合結晶は、細胞内で数百ナノメートル[用語5]サイズの固体粒子として自発的に形成されるため、複雑な精製プロセスを必要とせず、容易に単離できる。
次に、その複合結晶を光増感剤である人工分子のエオシンY(EY)の溶液に含浸させることによって、H1-FDHとEYの両方をカプセル化した、人工光合成を実現するハイブリッド固体触媒(EY・H1-FDH@PhC)の調製に成功した(図1下)。
このEY・H1-FDH@PhCハイブリッド固体触媒を用いて、NADH[用語6]存在下でのカスケード人工光合成反応を行ったところ(図2上)、光存在下でCO2固定化を達成できることが分かった。特に、FDHの集積に有利な大きな細孔を形成し、負電荷を有するEYの結合を安定化させる正電荷アミノ酸の変異を導入したPhCd38-K58G/G60K/E63K変異体では、触媒活性の向上が確認された。触媒機能については、PhCに固定化されたFDHは、溶液中のFDHと比較して、ギ酸の酸化反応では94%の触媒活性を示すことが分かった。さらに、10回の再生利用でも75%の活性を維持することや、耐熱性が溶液中のFDHに比べて24℃も向上することが確認された(図2下)。これらの結果は、タンパク質結晶が内包FDHの再利用性を著しく向上させることを示している。
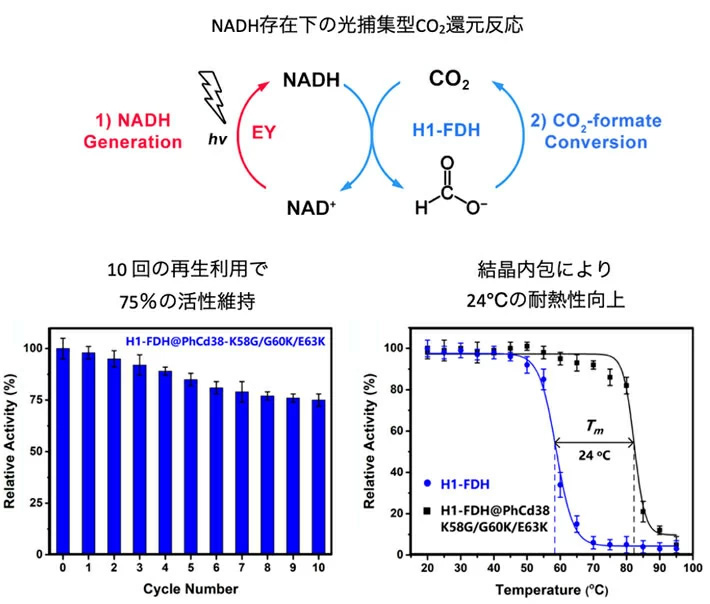
図2. ハイブリッド固体触媒としての機能向上
結論として、本研究ではハイブリッドタンパク質結晶を設計し、FDHとEYの両方をカプセル化することにより、人工光合成を促進するハイブリッド固体触媒を開発することに成功した。今回行ったような、タンパク質結晶への生体分子と人工分子のカプセル化によるハイブリッド材料の構築は、ナノ材料や人工光合成の分野において、環境低負荷で高効率な合成戦略を提供することが期待される。
社会的インパクト
今回用いた方法では、H1-FDHとPhCを細胞内で複合結晶として直接材料化でき、その結晶も煩雑な精製操作を必要とせず、簡単な遠心分離で単離できる。分子のカプセル化後も、94.4%のFDH活性が維持されたことを考えると、この遺伝子工学的手法は、酵素固定化や生体触媒としての利用において大きな可能性を秘めていると言える。さらに、今回開発した複合結晶では、酵素FDHと人工分子EYの両方を内包することにより、人工光合成を実現した点がポイントである。このような細胞内タンパク質結晶を用いた酵素と人工分子のハイブリッド機能化は、エネルギー分野における再利用可能な固体触媒への実用的方法として大きな可能性を有するものである。
今後の展開
今回の研究では、結晶を形成する多角体タンパク質と酵素を1つの細胞内で同時に合成することによって、酵素を固定化した多角体の合成に成功した。この手法では、従来必要とされた、タンパク質精製や材料への固定化といった煩雑な操作が不要なため、不安定性と低収量のために利用が困難とされてきた酵素を応用できる可能性が広がる。さらに、結晶細孔の設計によって、触媒の活性や選択性を簡単に制御することができるため、新たな固体触媒材料への展開が期待される。
- 付記
本成果は、文部科学省科学研究費助成事業(21F51326、22H00347、JP18H05421)の支援によるものである。
- 用語説明
[用語1] 細胞内タンパク質結晶化反応 : タンパク質結晶は通常、タンパク質と、結晶化を促進する沈殿剤を混合することで結晶化させる。一方、細胞内タンパク質結晶は、タンパク質自身の安定化や細胞内分子の貯蔵や運搬によって、細胞内で自発的に結晶を形成する。1960年代からこの現象は確認されているものの、細胞内での詳細な結晶化機構はいまだ明らかになっていない。
[用語2] ギ酸脱水素酵素(Formate dehydrogenase ; FDH) : ギ酸 + NAD+ CO2 + NADHを触媒する酸化還元酵素であり、光酸化還元触媒であるエオシンYとカップリングすることにより、NADH存在下でCO2をギ酸に変換する。
[用語3] エオシンY(EY) : 光酸化還元触媒として機能する。NADH/NAD+の変換に利用される。
[用語4] 多角体 : 細胞質多角体病ウイルスの感染後期に合成される多角体タンパク質が自律的に集合して結晶化した、タンパク質の結晶構造体。水中や有機溶媒中でも溶解しない高い安定性を有している。細胞内タンパク質結晶化反応で、研究対象として利用されているタンパク質結晶の1つ。
[用語5] 数百ナノメートル : ナノメートルは100万分の1ミリ。数百ナノメートルの超微小なタンパク質結晶は、触媒として高い反応性を示す。
[用語6] NADH(ニコチンアミドアデニンジヌクレオチド) : さまざまな脱水素酵素の補酵素として機能する。酸化型、還元型の2つの状態を取りうる。
- 論文情報
| 掲載誌 : | Nano Letters |
|---|---|
| 論文タイトル : | In-Cell Engineering of Protein Crystals into Hybrid Solid Catalysts for Artificial Photosynthesis |
| 著者 : | Tiezheng Pan, Basudev Maity, Satoshi Abe, Taiki Morita, Takafumi Ueno |
| DOI : | 10.1021/acs.nanolett.3c02355 |
- 無細胞タンパク質合成を用いた迅速なタンパク質結晶の合成|生命理工学系News
- 動画で見る東工大研究「タンパク質でつくる―次世代スマート材料」|生命理工学系News
- 金属錯体が生まれ変わる分子のカゴ|生命理工学系News
- 動いて並んでつながって。タンパク質が幾何学模様に!|生命理工学系News
- 細胞が分子の3Dプリンターに?!|生命理工学系News
- 7大学参加の研究グループ「コロナ制圧タスクフォース」発足|生命理工学系News
- タンパク質分子の彫刻を創る|生命理工学系News
- タンパク質カゴの中で踊る金原子を観る―タンパク質結晶を使った金属イオン集積過程の観察―|生命理工学系News
- タンパク質用いて細胞内分子フィルターを開発―細胞内の解毒、細胞内在分子の構造解析への応用に期待―|生命理工学系News
- 結晶の鎧まとう酵素?!―酵素の簡便な合成と長期保存を一挙に実現―|東工大ニュース
- 光で働く細胞内のカゴ状スイッチ―炎症抑制効果をもつたんぱく質の活性化とCOの関係を解明―|東工大ニュース
- 平成29年度「東工大挑戦的研究賞」授賞式を実施-独創性豊かな若手研究者に-|東工大ニュース
- 平成28年度手島精一記念研究賞授与式|生命理工学系News
- 上野研究室
- 安部聡 Satoshi Abe|研究者検索システム 東京工業大学STARサーチ
- マイティ・バスデフ Maity Basudev|研究者検索システム 東京工業大学STARサーチ
- 上野隆史 Takafumi Ueno|研究者検索システム 東京工業大学STARサーチ
- 生命理工学院 生命理工学系
- 研究成果一覧