生命理工学系 News
減数分裂期の遺伝情報交換を促進する機構を解明
相同組換え酵素の制御機構の一分子解析
要点
- 減数分裂期の相同組換えの中核を担う酵素Dmc1の制御機構を一分子レベルで解析。
- 一本鎖DNAへのDmc1の結合が、2種類の補助因子によって異なる様式で制御されることを発見。
- 不妊や遺伝性疾患の原因解明や新規治療法の開拓に期待。
概要
東京工業大学 科学技術創成研究院 細胞制御工学研究センターの坪内英生助教(生命理工学コース 主担当)、岩崎博史教授と国立台湾大学の李弘文教授(Prof. Hung-Wen Li)らの国際共同研究グループは、減数分裂期に誘導される相同組換えの活性化のメカニズムを一分子レベルで明らかにした。
遺伝情報[用語1]を次の世代に伝える上で、減数分裂[用語2]は必須の役割を果たしている。減数分裂期には、父方と母方の遺伝情報が相同組換え[用語3]というメカニズムにより積極的に撹拌され、これが生命の多様性を生む原動力となる。本研究では、この過程で中心的な役割を果たすDmc1という相同組換え酵素が2種類の因子により全く異なる様式で活性促進されることを、一分子解析技術を用いて明らかにした。減数分裂期の相同組換え異常は不妊や遺伝性疾患(ダウン症候群など)を引き起こすことから、そのメカニズムの解明は医学的見地からも大変重要と考えられる。
本研究は、7月4日(日本時間)に科学雑誌「Nucleic Acids Research」のオンライン速報版で掲載された。
背景
二本鎖DNAは互いに相補的な一本鎖DNA同士がより合わさった二重らせん構造を形成している。どちらかのDNA鎖に損傷がある場合、もう片方の相補的なDNA鎖を参照して正確な修復が可能である。しかし二本鎖が同時に損傷した場合は、正確に修復するのは極めて困難であり、一般には相同組換えという機構に頼る必要がある(図1)。相同組換えの根幹は、傷害を受けたDNAの周りの塩基配列を手がかりに、ゲノム中からよく似た配列(相同配列)を見つけ出すことであり、相同配列が見つかれば、その配列を参照して損傷部位を正確に修復することが可能となる。
興味深いことに、ヒトを含む多くの真核生物では、相同組換えはDNA傷害修復だけでなく、減数分裂でも必須の役割を果たしている。減数分裂前期にはゲノム全域でDNAに対して二重鎖切断が導入され、大規模な相同組換え誘導が起こる。相同染色体間で相同組換えが活発に起こった結果として、父方と母方の遺伝情報が活発に交換・撹拌される。この減数分裂期の相同組換えは、減数第一分裂期の相同染色体の分配に必須の役割を果たすとともに、進化の面でも生命の多様性を生み出す原動力となってきたと考えられている。
この相同組換えの根幹を担うのが、RecAおよびその相同タンパク質(RecAホモログ[用語4])である。このRecAホモログは、DNA間の相同性の検索およびDNA鎖交換反応を行う(図1)。興味深いことに、多くの真核生物は、減数分裂期の相同組換えに特化したDmc1と呼ばれるRecAホモログを持つ。このDmc1は、数々の補助因子と協働的に機能することが分かっている。そうした補助因子の中で、Dmc1の機能促進に中心的役割を果たすのが、本研究グループが世界に先駆けて同定・解析した複合体Hop2-Mnd1とSwi5-Sfr1である。
Dmc1が機能する上では、まず一本鎖DNA上に多量体からなるらせん状のフィラメントを形成することが必要である。研究グループはこれまでに、Dmc1による相同組換え反応と、Hop2-Mnd1およびSwi5-Sfr1によるDmc1の活性化を試験管内で再構成することに成功している。本研究では、Hop2-Mnd1とSwi5-Sfr1がDmc1を活性化するメカニズムを一分子レベルで解明することを目指した。
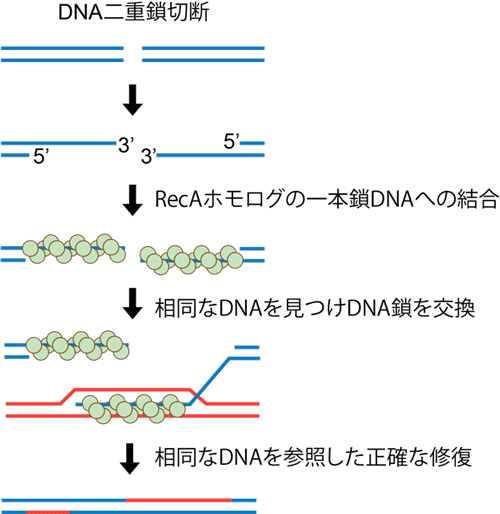
図1. 相同組換え過程とRecAホモログの役割
研究成果
今回の研究では、Dmc1の一本鎖DNA上への結合を一分子単位で検出するために、FRETペア[用語5]を形成する2種類の蛍光色素でラベルした一本鎖DNAを基質に用いた。この2種類の蛍光色素は短い一本鎖DNAにより隔てられている。一本鎖DNA自体はフレキシブルなので、2種類の蛍光色素が容易に近づくことができるため、FRET現象が頻繁に生じる。この一本鎖DNAにDmc1が一分子結合するたびに、DNAが引き伸ばされてFRET効率が低下する。したがってFRET効率をモニターすることで、Dmc1の一本鎖DNAへの結合と解離を一分子単位でリアルタイムに検出することが可能となる(図2)。この原理を用いて、Hop2-Mnd1とSwi5-Sfr1のDmc1への影響を調べたところ、Hop2-Mnd1はDmc1の一本鎖DNAへの結合を促進する一方で、Dmc1の一本鎖DNAからの解離には影響を与えないことが分かった。興味深いことに、Swi5-Sfr1ではHop2-Mnd1とは反対に、Dmc1の一本鎖DNAへの結合が安定化されて、一本鎖DNAからの解離頻度が著しく低下することが明らかとなった。
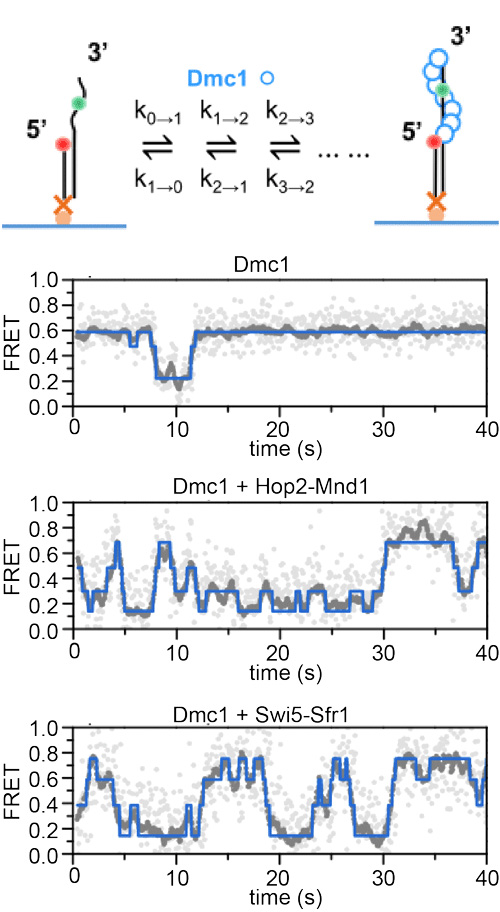
図2. FRETを利用したDmc1フィラメント形成の一分子解析
次に、一方の端を固定した一本鎖DNAの他端にプラスチックの微小ビーズを付着させたものを基質に用いて実験を行った。Dmc1の結合により、一本鎖DNAが引き伸ばされるので、微小ビーズのブラウン運動幅を顕微鏡下で観察することで、Dmc1フィラメントの形成と解離をリアルタイムで検出できる(図3)。この系により、Hop2-Mnd1はDmc1フィラメント形成を開始させることが分かった。さらに一本鎖領域に短い二本鎖領域を作ると、フィラメント形成が開始することから、Hop2-Mnd1は一本鎖と二本鎖の境界でDmc1フィラメント形成の開始を促進することが明らかとなった。一方、Dmc1単独のフィラメントは一定時間安定に保持された後、一斉に一本鎖DNAから解離した。これに対して、Swi5-Sfr1存在下では、Dmc1フィラメントはより長い時間維持されたが、一度解離が始まるとDmc1単独の場合よりも急激に崩壊が進行することが分かった。
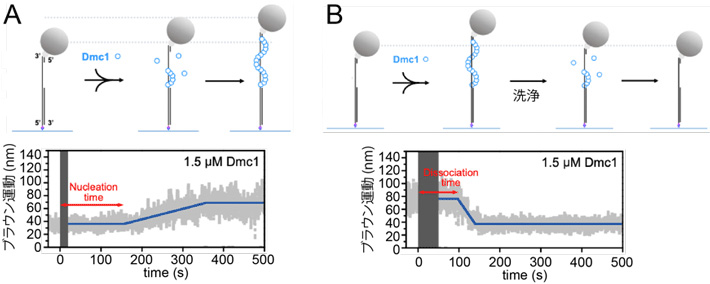
図3. DNAに結合させたビーズのブラウン運動を利用したDmc1フィラメントの形成(A)および解離(B)の検出
以上の結果から、減数分裂期の相同組換えの中核を担うDmc1は、Hop2-Mnd1とSwi5-Sfr1という2種類の制御因子によって、それぞれフィラメントの形成と解離という全く異なるステップで制御を受けていることが明らかとなった(図4)。
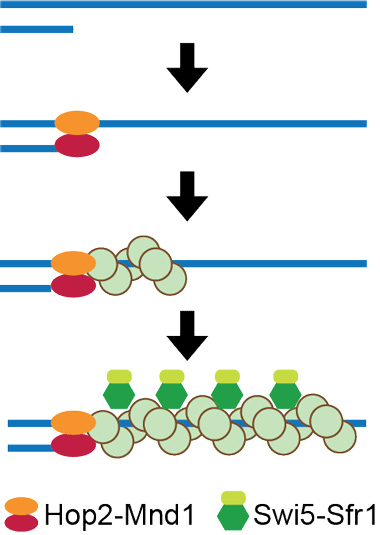
図4. Dmc1がフィラメント形成過程で受ける制御。Hop2-Mnd1は一本鎖と二本鎖の境界からDmc1フィラメント形成の開始を促進し、Swi5-Sfr1は形成したフィラメントからのDmc1の解離を抑制することでDmc1フィラメントを安定化する。どちらの因子も結果的にDmc1による相同組換えを促進する。
社会的インパクト
多くの真核生物で相同組換えが減数第一分裂において必須の役割を果たすのは、相同染色体の正確な分配には、染色体同士がDNA塩基配列レベルでお互いの相同性を認識し、キアズマを形成することが不可欠だからである。よって、相同組換え過程が異常になると、染色体が配偶子に正常に分配されず、不妊やダウン症候群(21番染色体が普通より1本多く分配されることで引き起こされる)などの遺伝性疾患の原因となる。相同組換えのメカニズムを知ることにより、不妊や遺伝性疾患の原因究明や新規治療法への道が開かれることが期待される。
今後の展開
本研究では、相同組換えの中でも特に、Dmc1が一本鎖DNA上にフィラメントを形成する過程にフォーカスした解析を行ったが、Hop2-Mnd1はフィラメント形成後の相同性検索やDNA鎖の交換過程でも機能すると考えられている。Dmc1のフィラメント形成のダイナミズムと相同性検索がどのように関連しているのか、その過程を一分子解析で捉えることができれば面白いだろう。減数分裂期に誘導される相同組換えは、何十種類ものタンパク質が関与する、緻密に制御された複雑な反応である。そのメカニズムの全貌を一分子レベルで理解するには長期的な取り組みが必要であり、今回の研究成果はその出発点となるものだといえる。
- 付記
本研究は、科学研究費助成事業 基盤研究(B)(18H02371 代表:坪内英生助教)および基盤研究(A)(22H00404 代表:岩崎博史教授)の支援を受けて行われた。
- 用語説明
[用語1] 遺伝情報 : 生命の遺伝情報はDNAの塩基配列として記述されている。そのため、DNAの塩基配列を一定に保つことは生命機能を正常に保つ上で重要である。
[用語2] 減数分裂 : 遺伝情報を次世代に伝えることに特化した細胞である、配偶子(ヒトでは精子と卵)を生み出すための特別な細胞周期。1回のDNAの複製後に細胞分裂が2回連続して起こる点が特徴である。特に減数第一分裂では相同染色体の分配が起こる点が、姉妹染色分配が起こる体細胞分裂とは大きく異なる。減数第一分裂前期では、相同組換えが高頻度で誘発され、父方と母方の遺伝情報が活発に交換される。一方で減数第二分裂では、体細胞分裂同様に姉妹染色分体が分配される。
[用語3] 相同組換え : 2つのDNA分子が相同性を有する場合、その部分で分子の乗り換え(すなわち組換え)が起こり、新しい分子が生じる現象を相同組換えと呼ぶ。相同組換えはDNAに二重鎖切断を導入することで誘導できる。
[用語4] RecAホモログ : 大腸菌RecAタンパク質は、DNAが二重鎖切断を受けた場合にその末端に形成される一本鎖DNAにらせん状に結合した上で、その部分と相同性のある二本鎖DNA分子を見つけ出して、一本鎖DNAを二本鎖DNAに潜り込ませる活性(DNA鎖交換活性)を有する。多くの真核生物ではRad51とDmc1という2種類のRecAファミリータンパク質を持つ。Rad51が体細胞分裂期と減数分裂期の両方で機能するのに対してDmc1は減数分裂期に特異的に発現して機能することが知られている。
[用語5] FRETペア : FRET(Fluorescence Resonance Energy Transfer)とは、蛍光を発する2種類の分子がごく近傍に位置する場合、発光を伴わないエネルギーの授受が起こる現象をいう。この場合に、ごく近傍に位置する2種類の蛍光物質をそれぞれドナー、アクセプターと呼ぶ。ドナーの蛍光波長とアクセプターの励起波長に重なりが見られる場合、ドナーを励起すると、発光を伴わずにエネルギーがアクセプターに移動し、アクセプターが励起される。このようなドナーとアクセプターの関係にある蛍光分子をFRETペアと呼ぶ。
- 論文情報
| 掲載誌 : | Nucleic Acids Research |
|---|---|
| 論文タイトル : | Hop2-Mnd1 and Swi5-Sfr1 stimulate Dmc1 filament assembly using distinct mechanisms |
| 著者 : | Wei Lee, Hiroshi Iwasaki, Hideo Tsubouchi*, Hung-Wen Li* (*co-corresponding authors) |
| DOI : | 10.1093/nar/gkad561 |
- 壊れたDNAを安全に修復するための第一歩を解明|生命理工学系 News
- 相同組換えを活性化するメカニズムを解明|生命理工学系 News
- 「がん遺伝子」として働くのか?組換え酵素Rad52が染色体異常を引き起こすことを発見|生命理工学系 News
- 相同組換えのDNA鎖交換反応開始の分子機構を解明|生命理工学系 News
- 分裂酵母の性(接合型)変換を制御する新たな遺伝子を発見|生命理工学系 News
- 姉妹染色分体間接着の形成機構を解明|生命理工学系 News
- 相同組換えのDNA鎖交換の素過程を世界で初めて解明|生命理工学系 News
- 遺伝子撹拌装置をタイミング良く染色体から取り外す仕組み|生命理工学系 News
- 葉緑体増殖の基礎的しくみを解明―葉緑体分裂・増殖時にDNA分配を制御する酵素の発見―|生命理工学系 News
- 岩崎博史教授が2016年日本遺伝学会木原賞を受賞|生命理工学系 News
- 岩﨑研究室
- 坪内英生 Hideo Tsubouchi|研究者検索システム 東京工業大学STARサーチ
- 岩﨑博史 Hiroshi Iwasaki|研究者検索システム 東京工業大学STARサーチ
- 科学技術創成研究院 細胞制御工学研究センター
- 科学技術創成研究院(IIR)
- 生命理工学院 生命理工学系
- 国立台湾大学
- 研究成果一覧