生命理工学系 News
【研究室紹介】 久堀・若林研究室(~2023.3)
生命理工学系にはライフサイエンスとテクノロジーに関連した様々な研究室があり、基礎科学と工学分野の研究のみならず、医学や薬学、農学等、幅広い分野で最先端の研究が活発に展開されています。
研究室紹介シリーズでは、ひとつの研究室にスポットを当てて研究テーマや研究成果を紹介。今回は、光合成生物の多様な生存戦略を研究している、久堀・若林研究室です。
※久堀教授と若林准教授は2023年3月31日、東工大を退職しました。

ライフエンジニアリングコース
教授 久堀徹
准教授 若林憲一
| キーワード | ATP合成酵素、レドックス制御、クラミドモナス、鞭毛運動 |
|---|---|
| Webサイト | 久堀・若林研究室 |
研究紹介
葉緑体ATP合成酵素の調節
ATP合成酵素は、生物界のエネルギー代謝で最も重要な酵素のひとつです。植物の場合には、葉緑体ATP合成酵素が太陽の光エネルギーを化学エネルギーであるATPに変換する重要な役割を担っています。この酵素は、1997年に回転分子モーターであることが証明されました。これは、当時、資源化学研究所の吉田賢右教授のグループが明らかにしたもので、東工大発の素晴らしい成果です。
生物がATP合成酵素を使って必要なときに必要なだけATPを生産するためには、この酵素の活性制御が重要です。すなわち、回転を制御するわけですが、植物の葉緑体が持っているATP合成酵素では、この制御機構は回転軸のタンパク質が酸化還元によって構造変化をするというユニークなシステムです。2018年にようやくこの制御部位の立体構造が明らかになりましたが、まだどのような分子機構で回転の制御が行われるのかはわかっていません。
光合成生物のレドックス制御ネットワークの包括的理解
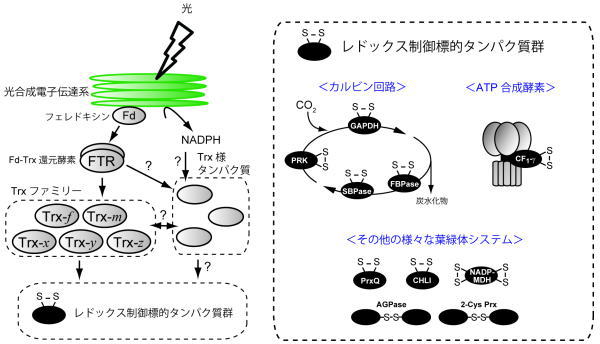
ATP合成酵素だけでなく、明暗の環境で生きる植物の酵素は、昼間だけ働くように絶妙に調節されています。この制御を行うシステムは、レドックス(酸化還元)制御機構と呼ばれています。光合成生物では光合成電子伝達系と炭酸同化系がレドックス制御機構で密接に結ばれています。さらに、光合成による酸素発生も細胞内レドックス状態の変動を招く大きな要因であり、細胞内は常にレドックスバランスを精密に保っていると予想されます。私たちの研究室では、原核光合成細菌であるシアノバクテリア、単細胞真核藻類であるクラミドモナス、そして、私たちに身近に存在する高等植物といった様々な光合成生物を用いて、レドックス制御システムの実態を明らかにすることを目指して研究を続けています。
クラミドモナスの鞭毛運動と光反応行動
クラミドモナス(Chlamydomonas reinhardtii)(図1)は、淡水性の単細胞緑藻です。1つの細胞には、運動装置である2本の鞭毛(図2)と、光受容装置である1つの眼点があります。眼点で光を感受すると細胞内のCa2+濃度が上昇し、それに応じて鞭毛の動かし方が変わり、光反応行動を示します。光反応行動は大きく分けて走光性と光驚動反応があります(図3)。前者は光源に向かって、あるいは光源から逃げるように泳ぐ行動(それぞれ正の走光性、負の走光性と呼びます)であり、後者は急激な光強度変化に伴い、遊泳方向を逆転させる反応です。走光性は2本の鞭毛の打つバランスの変化、光驚動反応は波の打ち方の変化によって生じます。私たちの興味の1つは、この鞭毛運動の制御機構です。真核生物の鞭毛・繊毛は原生生物からヒトまでほぼ共通した構造を持ちます。さまざまな光反応行動の突然変異株を使って、真核生物に共通した鞭毛・繊毛制御機構を分子レベルで明らかにしたいと考えています。
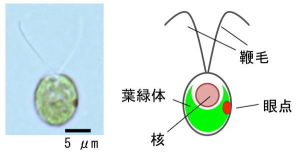
図1.クラミドモナスの明視野顕微鏡写真(左)と模式図(右)。
クラミドモナスの細胞はほぼ葉緑体で満たされており、2本の鞭毛と1つの眼点を持つ。
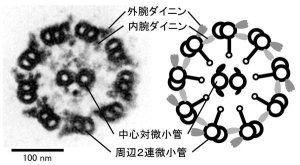
図2.クラミドモナス鞭毛の内部構造の超薄切片法による透過電子顕微鏡像(左)とその模式図(右)。
9組の周辺微小管と2本の中心対微小管から成る、特徴的な9+2構造を持つ。2本の鞭毛は,外腕ダイニンがない周辺2連微小管の場所を向かい合わせにして生えている。
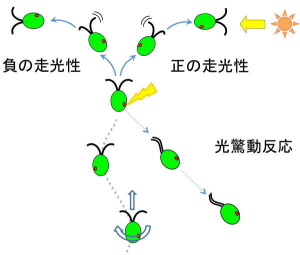
図3.クラミドモナスの光行動。
光源に向かう正の走光性、光源から逃げる負の走光性、急激な光照射に応じて鞭毛運動波形を変えて後方遊泳に転じる光驚動反応がある。
クラミドモナス走光性異常ミュータントから分かった、細胞レンズ効果
私達はいま、クラミドモナスが光を感受してから鞭毛運動が変化するまでの過程を分子レベルで解き明かそうとしている。最近単離したあるミュータントから、光感受の素過程の重要な知見が得られた。
私達は、クラミドモナス野生株が、細胞内に活性酸素が多くなると正の走光性、少なくなると負の走光性を示すことを見出した(Wakabayashi et al., 2011 Proc Natl Acad Sci USA)。この知見を利用して、野生株と逆方向に泳ぐ新規ミュータントlts1-211を単離した(Ueki et al., 2016 Proc Natl Acad Sci USA)(図4)。このミュータントは眼点に蓄積する赤いカロテノイド色素の合成経路が失われており、そのために細胞の内側を通ってきた光の遮蔽が起こらず、光源方向を誤認してしまうのである。この研究の過程で、クラミドモナスのように細胞内に葉緑体が詰まった複雑な内部構造をもっていても、細胞が凸レンズをして振る舞うことが判明した。
その後も次々に新しい走光性ミュータントを単離しており、その遺伝子解析を行うことで、走光性の制御機構の分子実態を明らかにしようとしている。
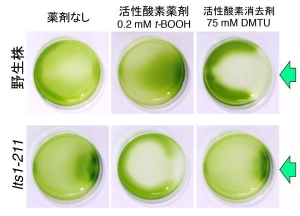
図4.クラミドモナスの走光性実験。
培養液をディッシュに入れて、右から光を当てた。野生株は活性酸素を加える正、活性酸素の消去剤を加えると負の走光性を示すが、lts1-211は逆方向に泳ぐ。
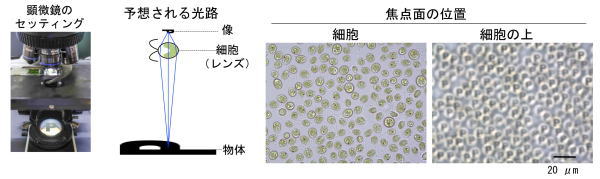
図5.クラミドモナスの細胞レンズ効果。
顕微鏡の光路に「P」の字を置き、顕微鏡の焦点面をクラミドモナスから上にあげると、各細胞の上にPの字が浮き出る。
研究成果
最近の論文
2018
- [1] Assessment of the flagellar redox potential in Chlamydomonas reinhardtii using a redox-sensitive fluorescent protein, Oba-Qc. Biochem Biophys Res Commun. 2018 Sep 10;503(3):2083-2088. doi: 10.1016/j.bbrc.2018.07.163. Epub 2018 Aug 10.
- [2] Structure of the γ-ε complex of cyanobacterial F1-ATPase reveals a suppression mechanism of the γ subunit on ATP-hydrolysis in phototrophs. Biochem J. 2018 Jul 27. pii: BCJ20180481. doi: 10.1042/BCJ20180481.
- [3] Thioredoxin-like2/2-Cys peroxiredoxin redox cascade supports oxidative thiol modulation in chloroplasts. Yoshida K, Hara A, Sugiura K, Fukaya Y, Hisabori T. Proc Natl Acad Sci U S A. 2018 Aug 28;115(35):E8296-E8304. doi: 10.1073/pnas.1808284115
- [4] Amputation of a C-terminal helix of the γ subunit increases ATP-hydrolysis activity of cyanobacterial F1 ATP synthase. Biochim Biophys Acta. 2018 May;1859(5):319-325. doi: 10.1016/j.bbabio.2018.02.004.
- [5] Development of heme protein based oxygen sensing indicators. Nomata J, Hisabori T. Sci Rep. 2018 Aug 7;8(1):11849. doi: 10.1038/s41598-018-30329-5.
- [6] Detergent-extracted Volvox model exhibits an anterior-posterior gradient in flagellar Ca2+ sensitivity. Proc Natl Acad Sci U S A. 2018 Jan 30;115(5):E1061-E1068. doi: 10.1073/pnas.1715489115. Epub 2018 Jan 8.
- [7] Application of CRISPR Interference for Metabolic Engineering of the Heterocyst-Forming Multicellular Cyanobacterium Anabaena sp. PCC 7120. Plant Cell Physiol. 2018 Jan 1;59(1):119-127. doi: 10.1093/pcp/pcx166
- [8] Spatio-Temporal Gene Induction Systems in the Heterocyst-Forming Multicellular Cyanobacterium Anabaena sp. PCC 7120. Plant Cell Physiol. 2018 Jan 1;59(1):82-89. doi: 10.1093/pcp/pcx163.
2017
- [1] A γ-subunit point mutation in Chlamydomonas reinhardtii chloroplast F1Fo-ATP synthase confers tolerance to reactive oxygen species. Biochim Biophys Acta. 2017 Dec;1858(12):966-974. doi: 10.1016/j.bbabio.2017.09.001.
- [2] Thioredoxin regulates G6PDH activity by changing redox states of OpcA in the nitrogen-fixing cyanobacterium Anabaena sp. PCC 7120. Biochem J. 2017 Apr 4;474(8):1347-1360. doi: 10.1042/BCJ20161089.
- [3] Distinct electron transfer from ferredoxin-thioredoxin reductase to multiple thioredoxin isoforms in chloroplasts. Biochem J. 2017 Apr 4;474(8):1347-1360. doi: 10.1042/BCJ20161089.
- [4] Phototaxis assay for Chlamydomonas reinhardtii Bio-protocol 2017 Vol 7, Iss 12, e2356. doi: 10.21769/BioProtoc.2356
- [5] Designing Synthetic Flexible Gene Regulation Networks Using RNA Devices in Cyanobacteria. ACS Synth Biol. 2017 Jan 20;6(1):55-61. doi: 10.1021/acssynbio.6b00201.
- [6] Functional Significance of NADPH-Thioredoxin Reductase C in the Antioxidant Defense System of Cyanobacterium Anabaena sp. PCC 7120. Plant Cell Physiol. 2017 Jan 1;58(1):86-94. doi: 10.1093/pcp/pcw182.
教員紹介
久堀徹 教授 理学博士
| 1980年 | 早稲田大学 教育学部理学科生物学専修 卒業 |
|---|---|
| 1982年 | 早稲田大学大学院理工学研究科 物理学及び応用物理学専攻 博士前期課程 修了 |
| 1985 | 早稲田大学大学院理工学研究科 物理学及び応用物理学専攻 博士後期課程 修了, 理学博士 |
| 1985 - 1987年 | 早稲田大学 教育学部理学科 生物学専修 助手 |
| 1987 - 1994年 | 横浜市立大学 文理学部理科 生物課程 助手 |
| 1995 - 2009年 | 東京工業大学 資源化学研究所 助教授/准教授 |
| 2009年より | 東京工業大学 大学院生命理工学研究科 分子生命科学専攻 教授(兼担) |
| 2009年より | 東京工業大学 大学院総合理工学研究科 化学環境学専攻 教授(兼担) |
| 2009 - 2016年 | 東京工業大学 資源化学研究所附属資源循環研究施設教授 |
| 2009 - 2016年 | 東京工業大学 資源化学研究所附属資源循環研究施設長 |
| 2012 - 2016年 | 東京工業大学 資源化学研究所副所長 |
| 2016年より | 東京工業大学生命理工学院 教授(ライフエンジニアリングコース主担当) |
| 2016年より | 東京工業大学 科学技術創成研究院化学生命科学研究所教授 |
| 2016 - 2018年 | 東京工業大学 科学技術創成研究院化学生命化学研究所副所長 |
| 2017年 | 手島精一記念研究賞研究論文賞 |
| 2018年より | 東京工業大学 科学技術創成研究院副研究院長(安全担当)、化学生命化学研究所所長 |
| 2018年 | 手島精一記念研究賞発明賞 |
- 所属学会
- 日本学術会、日本植物学会、日本生化学会、大隅基礎科学創成財団
教員からのメッセージ
- 久堀徹教授より
-
大学院修士の頃に取り組んだ葉緑体ATP合成酵素の研究から研究人生を始めて以来、一貫して植物生化学の研究を行っています。学生時代から長いことホウレンソウと付き合ってきましたが、研究の進展とともにアベナ、エンドウマメ、シロイヌナズナといろいろな植物を相手にしてきました。 さらに、東工大では、シアノバクテリアや大腸菌も扱っています。私の研究室では、光合成生物のATP合成酵素などの酵素がどのように調節され、それはどのような生理的な意味があるのか、という問題です。多くの仲間の面白い研究成果に、いつも心躍らせています。
若林憲一 准教授 博士(理学)
| 1996年 | 東京大学理学部生物学科動物学コース 卒業 |
|---|---|
| 1998年 | 東京大学大学院理学系研究科生物科学専攻修士課程 修了 |
| 2001年 | 東京大学大学院理学系研究科生物科学専攻博士課程修了, 博士(理学) |
| 1998 - 2001年 | 日本学術振興会特別研究員DC1 |
| 2001 - 2002年 | 基礎生物学研究所 細胞情報研究部門 非常勤研究員 |
| 2002 - 2005年 | 米国コネチカット大学ヘルスセンター 博士研究員 |
| 2005 - 2007年 | 東京大学大学院理学系研究科生物科学専攻 助手 |
| 2007 - 2012年 | 東京大学大学院理学系研究科生物科学専攻 助教 |
| 2012 - 2016年 | 東京工業大学 資源化学研究所 准教授 |
| 2012 - 2016年 | 東京工業大学大学院総合理工学研究科化学環境学専攻 准教授を兼任 |
| 2013 - 2016年 | 東京工業大学大学院生命理工学研究科分子生命科学専攻 准教授を兼任 |
| 2016年より | 東京工業大学 科学技術創成研究院 化学生命科学研究所 准教授 |
| 2016年より | 東京工業大学 生命理工学院 生命理工学系 准教授(ライフエンジニアリングコース主担当) |
| 2017年 | 手島精一記念研究賞(研究論文賞)受賞 |
- 所属学会
- 日本生物物理学会、日本植物生理学会、日本動物学会
教員からのメッセージ
- 若林憲一准教授より
-
学生実習で出会ったクラミドモナスの可愛らしさと、電顕観察した真核生物鞭毛の「9+2構造」の精緻な構造の虜になり、以来、クラミドモナスを用いた細胞運動研究を一貫して続けています。現在はクラミドモナスをはじめとするボルボックス目緑藻が光環境に応じて示す運動変化(光行動)の生理的意義に関わる研究に取り組んでいます。細胞運動と光合成という、異なる分野が重なった独自の研究です。私達の研究成果は、細胞生物学、動物生理学、医学、植物生理生化学、光生物学などの多様な分野に影響を与える、基礎研究としての波及効果が高いものになると期待しています。
※この内容は掲載日時点の情報です。