生命理工学系 News
【研究室紹介】 岩崎研究室
科学を楽しもう
生命理工学系にはライフサイエンスとテクノロジーに関連した様々な研究室があり、基礎科学と工学分野の研究のみならず、医学や薬学、農学等、幅広い分野で最先端の研究が活発に展開されています。
研究室紹介シリーズでは、ひとつの研究室にスポットを当てて研究テーマや研究成果を紹介。今回は、相同組換えの生理機能やその分子制御メカニズムを明らかにする、岩崎研究室です。

主担当 生命理工学コース
教授 岩崎博史![]()
(科学技術創成研究院 細胞制御工学研究ユニット 所属)
| キーワード | 相同組換え / DNA修復 / 染色体生物学 / ゲノム動態 |
|---|---|
| Webサイト | 岩崎研究室 細胞制御工学研究ユニット |
研究紹介
ゲノムを正確に複製するしくみが、生命の連続性を保証しています。すなわち、一つの細胞が分裂してできた2つの娘細胞は全く同じ遺伝情報(DNAの塩基配列)をもっていることになります。
しかし、同一生物種であっても遺伝情報を完全に同じくする2つの個体は存在しません。
同じ両親から生まれた兄弟姉妹ですら(一卵性双生児を除いて)、遺伝情報が100%一致しているわけではないのです。
すなわち、卵や精子が形成されるとき、染色体上のDNA配列のダイナミックな再編成(すなわち、相同組換え)がおこり、二つとて同一のDNA配列をもたない生殖細胞が出来上がります。そして、そのような2つの細胞の受精によって生じる個体の遺伝情報は、当然、親とは別物で、さらに、兄弟姉妹によっても異なることになります(種の多様性の創出)。
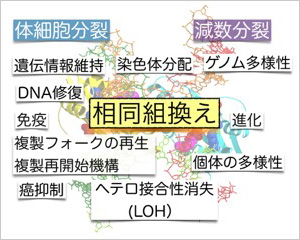
相同組換えの多彩な機能
一方、体細胞分裂時には、相同組換えはDNA 損傷の修復に利用されます。
例えば、DNAの二重鎖が切断されると、相同な染色体(多くの場合は,相同染色体でなく姉妹染色体)の遺伝情報をコピーして、切断部分の情報を修復します(組換え修復)。
それゆえ、相同組換えは生物種内ではゲノムの多様性を創出する一方で、個体内ではゲノムの安定維持への寄与という、一見、相反するユニークな生理機能と担っていることになります。しかも、面白いことに、DNA複製や転写に代表される核内イベントと同様、すべての地球上の生物がもっている根源的な生命機能です。
相同組換えや組換え修復の分子機構は、未だに不明な部分が多く、詳細に研究が進んでいる核内イベントの中では、唯一最後に残された分子遺伝学上の大問題といっても過言ではないでしょう。我々の研究室では、この問題を解明するために精力的に研究しています。
研究成果
- 代表論文
- [1] Multiple regulation of rad51-mediated homologous recombination by fission yeast fbh1. Tsutsui Y, Kurokawa Y, Ito K, Siddique MS, Kawano Y, Yamao F and Iwasaki H. PLoS Genet. (2014) 28. e1004542.
- [2] Dual regulation of Dmc1-driven DNA strand exchange by Swi5-Sfr1 activation and Rad22 inhibition. Murayama Y, Kurokawa Y, Tsutsui Y, Iwasaki H. Genes Dev. (2013) 27:2299-2304.
- [3] Mechanistic insights into the activation of Rad51-mediated strand exchange from the structure of a recombination activator, the Swi5-Sfr1 complex. Kuwabara N, Murayama Y, Hashimoto H, Kokabu Y, Ikeguchi M, Sato M, Mayanagi K, Tsutsui Y, Iwasaki H and Shimizu T. Structure (2012) 20:440-449.
- [4] An in vitro assay for monitoring the formation and branch migration of Holliday junctions mediated by a eukaryotic recombinase. Murayama Y and Iwasaki H. Methods Mol. Biol. (2011) 745:385-405.
- [5] The fission yeast meiosis-specific Dmc1 recombinase mediates formation and branch migration of Holliday junctions by preferentially promoting strand-exchange in a direction opposite to that of Rad51. Murayama Y, Tsutui, Y and Iwasaki H. Genes Dev. (2011) 25:516-527.
- [6] Nbs1 flexibly tethers Ctp1 and Mre11-Rad50 to coordinate DNA double-strand break processing and repair. Williams RS, Dodson GE, Limbo O, Yamada Y, Williams JS, Guenther G, Classen S, Glover JN, Iwasaki H, Russell P and Tainer JA. Cell (2009) 139: 87-99.
- [7] RAD6-RAD18-RAD5 pathway-dependent tolerance to chronic low-dose UV light. Hishida T, Kubota Y, Carr AM, and Iwasaki H. Nature (2009) 457: 612-615.
- [8] Molecular characterization of the role of the Schizosaccharomyces pombe nip1+/ctp1+ gene in DNA double strand break repair in association with the Mre11-Rad50-Nbs1 complex. Akamatsu Y, Murayama Y, Yamada T, Nakazaki T, Tsutsui Y, Ohta K and Iwasaki H. Mol. Cell. Biol. (2008) 28: 3639-3651.
- [9] Reconstitution of DNA strand exchange mediated by Rhp51 recombinase and two mediators. Kurokawa Y, Murayama Y, Haruta-Takahashi N, Urabe I and Iwasaki H. PLoS Biol (2008) 6: e88.
- [10] Formation and branch migration of Holliday junctions mediated by eukaryotic recombinases. Murayama Y, Kurokawa Y, Mayanagi K and Iwasaki H. Nature (2008) 451: 1018-1021.
- [11] Fission yeast Swi5/Sfr1 and Rhp55/Rhp57 differentially regulate Rhp51-dependent recombination outcomes. Akamatsu Y, Tsutsui Y, Morishita T, Siddique, MDP, Kurokawa, Y. Ikeguchi M, Yamao F, Arcangioli B and Iwasaki H. EMBO J. (2007) 26: 1352-1362.
- [12] The Swi5-Sfr1 complex stimulates Rhp51/Rad51- and Dmc1-mediated DNA strand exchange in vitro. Haruta N, Kurokawa Y, Murayama Y, Akamatsu Y, Unzai S, Tsutsui Y and Iwasaki H. Nature Struct. Mol. Biol. (2006) 13: 823-730.
- [13] Two different Swi5-containing protein complexes are involved in mating-type switching and recombination repair in fission yeast. Akamatsu Y, Dziadkowiec D, Ikeguchi M, Shinagawa H and Iwasaki H. Proc. Natl. Acad. Sci. USA. (2003) 100: 15770-15775.
- [14] Atomic structure of the RuvC resolvase: a Holliday junction specific endonuclease from E. coli. Ariyoshi M, Vassylyev DG, Iwasaki H, Nakamura H, Shinagawa H and Morikawa K. Cell (1994) 78: 1063-1072.
- [15] Escherichia coli RuvA and RuvB proteins specifically interact with Holliday junctions and promote branch migration. Iwasaki H, Takahagi M, Nakata A and Shinagawa H. Genes Dev. (1992) 6: 2214-2220.
- [16] Escherichia coli RuvC protein is an endonuclease that resolves the Holliday structure. Iwasaki H, Takahagi M, Shiba T, Nakata A and Shinagawa H. EMBO J. (1991) 10: 4381-4389.
- 主な著書
- [1] 岩崎博史、田口英樹 著「池上彰が聞いてわかった生命のしくみ ー東工大で生命科学を学ぶー」 朝日新聞出版(2016)
教員紹介
岩崎博史 教授(医学博士)
| 1991年3月 | 大阪大学 大学院医学研究科 博士課程修了 |
|---|---|
| 1991~2001年 | 大阪大学 微生物病研究所 助手 |
| 2001~2007年 | 横浜市立大学 大学院総合理学研究科 助教授 |
| 2007~2009年 | 横浜市立大学 国際総合科学研究科 教授 |
| 2009~2012年 | 東京工業大学 大学院生命理工学研究科 分子生命科学専攻 教授 |
| 2012~2016年 | 東京工業大学 大学院生命理工学研究科 生体システム専攻 教授 |
| 2016年~ | 東京工業大学 科学技術創成研究院 細胞制御工学研究ユニット 教授 |
| 1997年3月~1998年3月 | 文部省在外特別研究員としてYale 大学に留学(G.S. Roeder研) |
|---|---|
| 1998年10月~2001年9月 | 科学技術振興機構さきがけ研究21研究者を兼任 |
| 2011年より | 第22期・23期 日本学術会議連連携会員 |
| 2001年 | 日本遺伝学会 奨励賞 |
|---|---|
| 2013年 | 文部科学大臣表彰 科学技術賞 |
| 2016年 | 日本遺伝学会 木原賞 |
- 教育活動
- 学部:生命科学基礎 分子生物学I、分子遺伝生化学I(生体機構コース)
- 大学院:分子細胞生物学
- 所属学会
- 日本遺伝学会、日本分子生物学会、蛋白質科学会、American Society for Microbiology
教員からのメッセージ
- 岩崎教授より
-
「子曰、知之者不如好之者、好之者不如樂之者。(子曰わく、これを知る者はこれを好む者に如かず。これを好む者はこれを楽しむ者に如かず)」
ピュアなサイエンスを一緒に楽しみましょう。
お問い合わせ先
教授 岩崎博史
大岡山キャンパス 緑が丘地区 M6棟 401号室
E-mail : hiwasaki@bio.titech.ac.jp
※この内容は掲載日時点の情報です。最新の研究内容については研究室サイト![]() をご覧ください。
をご覧ください。
※ 2025年5月1日:一部最新の情報に更新しました。