生命理工学系 News
ハッチンソン・ギルフォード・プロジェリア症候群で細胞核膜の修復が遅延するメカニズムを解明
東京科学大学(Science Tokyo)※ 総合研究院 細胞制御工学センターの木村宏教授(生命理工学コース 主担当)、金沢大学ナノ生命科学研究所(WPI-NanoLSI)の河野洋平研究員、市川壮彦特任助教、志見剛特任准教授、福間剛士教授、ソウル峨山生命科学研究院の白燦基教授らを中心とする共同研究グループは、早老症の一つであるハッチンソン・ギルフォード・プロジェリア症候群(HGPS)の原因となるラミンA・ラミンC・プロジェリン[用語1]の核膜修復動態に差を生じさせているファルネシル化[用語2]の寄与を解明、およびテール領域内の特定配列(LACS1/2)を同定しました。
本研究グループはこれまで、細胞分裂の間期にDNAを包む核膜が一部破損すると、ラミンCタンパク質が迅速に集積し修復に関与することを報告していました。しかし、ラミンAがラミンCよりも遅れて核膜へ局在するメカニズムは未解明のままでした。
今回の研究では、原子間力顕微鏡(AFM)による任意の細胞核の圧縮技術や、共焦点蛍光顕微鏡による局所的なレーザー照射技術を用いて、核膜ラプチャー[用語3]させる実験を行いました。その結果、HGPSの細胞では、正常細胞に比べて核膜の修復が遅れることが明らかになりました。また、この遅延のメカニズムを詳細に解明しました。さらに、ファルネシル転移酵素阻害薬であるロナファルニブを用いることで、核膜破損部位へのラミンの再局在化が促進されることも確認しました。
本研究は、日本と韓国に加え、米国ノースウエスタン大学、英国ロンドン大学クイーン・メアリー校、スイス・チューリッヒ大学の研究者と共同で進められた国際プロジェクトです。合計5カ国の研究者が参加する広範な国際共同研究の推進により、国際的に卓越した成果を上げることができました。
これらの知見は将来、ハッチンソン・ギルフォード・プロジェリア症候群や、ラミノパチー[用語4]の治療薬開発に活用される可能性があります。また、細胞核膜およびラミンが制御するさまざまな生命現象の理解にも大きく寄与すると期待されます。
本研究成果は、2024年11月21日(英国時間)に国際学術誌「PNAS Nexus」のオンライン版に掲載されました。
※2024年10月1日に東京医科歯科大学と東京工業大学が統合し、東京科学大学(Science Tokyo)となりました。
背景
早老症の一つであるハッチンソン・ギルフォード・プロジェリア症候群(HGPS)とは、世界的に約400万人に1人の頻度といわれる小児期発症の超希少難治性疾患です。出生時には異常がみられませんが、次第に成長障害や老化症状に似た特徴的な臨床症状が現れます。精神発達は正常ですが、年齢とともに動脈硬化症が進行し、その合併症として心筋梗塞や心不全、脳卒中を発症し、多くの場合は思春期を迎える頃に命を落とす非常に重篤な疾患です。
HGPSは、LMNA遺伝子の点突然変異(主にc.1824C>T)[用語5]によって引き起こされます。動物細胞では、DNAを包んでいる核膜のDNA側に、ラミナとよばれる薄い網目構造が存在しています。このラミナの厚さは約13.5 nmで、この極めて薄い構造がクロマチンと相互作用し、核の安定性を維持する重要な役割を果たしているとされています。そのラミナの構成成分の一つであるラミンA/Cタンパク質(LA、LC)と、HGPSの原因タンパク質であるプロジェリン(PG)は、すべてLMNA遺伝子から発現します。しかし、LAとLC、PGはテール領域の長さが異なり、特にPGは末端にファルネシル化とよばれる修飾が残ったまま核膜内膜につなぎ留められます。
健常な人の体細胞では、LMNA遺伝子から主にLAとLCが発現しますが、HGPS細胞では、LA、LCに加えてPGが微量に発現します。この微量なPG発現が、HGPSの病態形成の本質となっていると考えられています。
研究成果
これまでの研究で、細胞分裂の間期にDNAを包む核膜が一部破れて孔が開いた場合、LCが迅速に集積して修復に関与する一方、LAはLCよりも遅れて局在することが分かっていました。しかし、LAの遅延の理由や、LMNA遺伝子の異常スプライシング[用語6]によって発現するPGの核膜修復への影響については未解明でした。
今回、WPI-NanoLSIの研究グループは、原子間力顕微鏡(AFM)を用いて任意の細胞核を圧縮し、核膜を破損(ラプチャー)させる技術を活用しました。HGPSモデルマウス由来の細胞を解析した結果、正常細胞に比べて核膜修復が遅延することを発見しました(図1)。
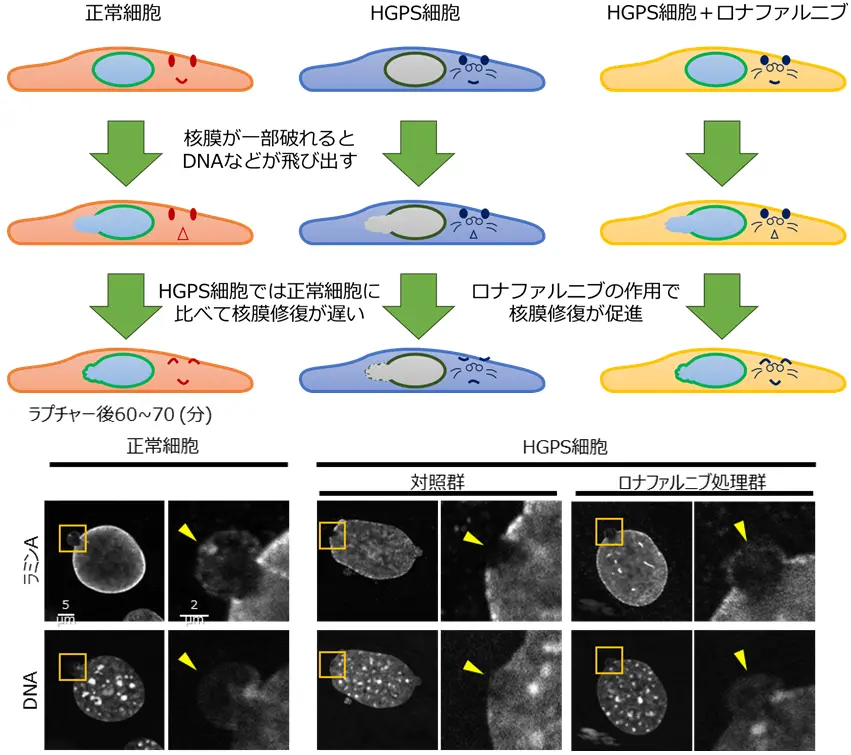
図1. HGPS細胞で遅延する核膜ラプチャー修復
さらに、東京科学大学(旧・東京工業大学)の共焦点蛍光顕微鏡の局所的なレーザー照射技術による核膜ラプチャー実験では、PGはLAよりもさらに遅れて破損部位へ局在することを確認しました。また、HGPS細胞では、LCやLAの修復動態も正常細胞に比べ遅延することが明らかになりました。また、これらの遅延は、ファルネシル転移酵素阻害薬ロナファルニブによって改善され、PGやLAの核膜修復が促進されることも明らかになりました。
さらに、LAとLCの集積動態に差が生じるメカニズムとして、LAのテール領域にLCと比べてLAの局在を遅延させる2つの配列(LACS1/2)が存在することを発見しました(図2)。
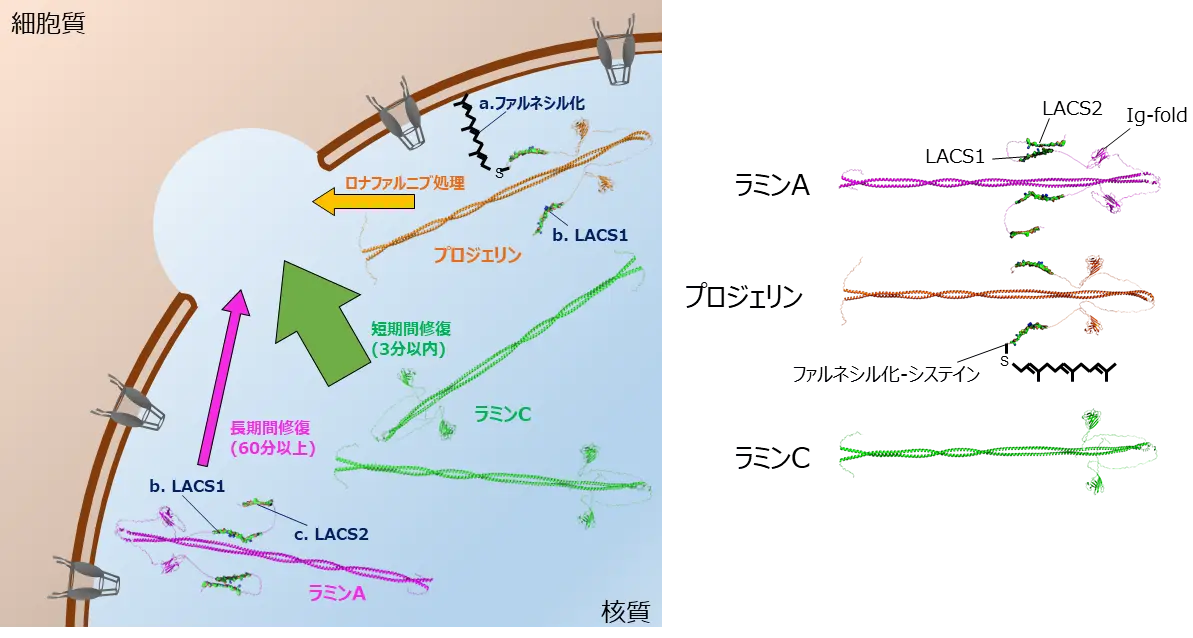
図2. ファルネシル化とラミンA特徴的配列(LACS1/2)による核膜修復の制御
今後の展開
本研究により、HGPSにおいて核膜修復が遅延するメカニズムと、LA、PGのファルネシル転移酵素阻害薬であるロナファルニブがその改善に寄与することが示されました。これらの知見は、HGPSのみならず、LMNA遺伝子の変異によって引き起こされるラミノパチーと総称される疾患の発症メカニズム解明や、新たな治療法開発に役立つことが期待されます。また、本研究の結果からLAとLCがそれぞれ異なる役割を果たすことが強く示唆されており、これまで同一のタンパク質であるかのように扱われてきたLAとLCの生物学的意義について、基礎研究のさらなる発展が見込まれます。
- 付記
本研究は、文部科学省世界トップレベル研究拠点プログラム(WPI)、日本学術振興会科学研究費助成事業(課題番号:20KK0158、20K06617、18H05527、21H04764)、英国Wellcome Trust(098291/Z/12/Z)、英国心臓財団British Heart Foundation(FS/IBSRF/22/ 25121)の助成、および東京工業大学基礎研究機構専門基礎研究塾細胞科学分野(大隅塾)、東京工業大学オープンファシリティセンターバイオ部門、ソウル峨山病院融合研究支援センター細胞イメージング分析室の支援、文部科学省先端研究基盤共用促進事業(コアファシリティ構築支援プログラム)JPMXS0440200022で共用された機器を利用して実施されました。
- 用語説明
[用語1] ラミンA・ラミンC・プロジェリン:核膜の足場となる核ラミナを構成するラミン分子のうち、LMNA遺伝子によってコードされているA型ラミンタンパク質。プロジェリンはLMNA遺伝子の変異によって発現し、ハッチンソン・ギルフォード・プロジェリア症候群の原因となる。ラミンは細胞分裂時の核膜の分解・再構築や核の機械的ストレスの受容体となるだけでなく、クロマチンに直接作用して遺伝子発現制御にも関与している。
[用語2] ファルネシル化:タンパク質の翻訳後修飾の一種。ファルネシル転移酵素により、タンパク質の末端にファルネシル基が結合する。この修飾によってタンパク質末端が疎水性になり、細胞膜や核膜などの脂質二重膜に固定される。
[用語3] 核膜ラプチャー:一般的に知られている細胞分裂期の核膜崩壊とは異なり、間期の細胞において核が圧縮・引張を受ける、あるいは実験的にレーザー照射されることで、核膜の一部に孔が生じ、核内成分が細胞質へ漏れ出る現象。骨格筋、心筋、皮膚、結合組織など機械的ストレスを受けやすい組織で発生しやすい。
[用語4] ラミノパチー:核膜病の一種で、ラミン遺伝子変異によって生じる疾患の総称。LMNA遺伝子変異が原因となるものが多い。LMNA遺伝子全長にわたって500種以上の点突然変異から、早老症(プロジェリア)、心筋症、筋ジストロフィー、リポジストロフィーなどのさまざまな症状を呈する。その他のラミン遺伝子として、B型ラミンのLMNB1遺伝子変異による白質ジストロフィーやLMNB2遺伝子変異によるリポジストロフィーが報告されている。
[用語5]
点突然変異:遺伝子のDNAまたはRNAの1ヌクレオチド塩基が別の塩基に置き換わってしまう突然変異のこと。点突然変異は、生物の遺伝的多様性の源となるが、一方で遺伝性疾患の原因となることがある。点突然変異は、生まれた後に起こる後天的なものと、生まれつき持っている先天的なものに分かれる。後天的変異は、生物が生きていく過程において物理的あるいは化学的な変異原によって自然に引き起こされることがある。先天的変異には親から遺伝するものと、胎生期の環境要因によって生じるものがあるが多くは原因不明である。
ハッチンソン・ギルフォード・プロジェリア症候群の原因となるc.1824C>T変異は、患児の両親には存在せず、各々の症例において新規に生じている
[用語6] LMNA遺伝子のスプライシング:LMNA遺伝子によってコードされるメッセンジャーRNA(mRNA)は、選択的スプライシングを経て通常ラミンAとラミンCに翻訳される。プロジェリンは、LMNA遺伝子のエクソン11に点変異(主にc.1824C>T)が生じた場合、潜在的なスプライス部位ドナーの活性化により、異常スプライシングによって翻訳された病的ラミンタンパク質である。この異常スプライシングでは、エクソン11後半が欠失しエクソン12と接続される。ほかにも生殖細胞では代替的スプライシングによって、ラミンC2やラミンAΔ10が発現している。
- 論文情報
| 掲載誌: | PNAS Nexus |
|---|---|
| 論文タイトル: |
Roles of the lamin A-specific tail region in the localization to sites of nuclear envelope rupture
(ラミンA特異的テール領域の核膜ラプチャー部位局在化への役割) |
| 著者: |
Yohei Kono, Chan-Gi Pack, Takehiko Ichikawa, Arata Komatsubara, Stephen A. Adam, Keisuke Miyazawa, Loïc Rolas, Sussan Nourshargh, Ohad Medalia, Robert D. Goldman, Takeshi Fukuma, Hiroshi Kimura, Takeshi Shimi (河野洋平、白燦基、市川壮彦、小松原新大、ステファン・アダム、宮澤佳甫、ロイック・ロラ、スーサン・ノーシャー、オハッド・メダリア、ロバート・ゴールドマン、福間剛士、木村宏、志見剛) |
| DOI: |
10.1093/pnasnexus/pgae527 |
関連リンク
- 世界初!卵子にDNA溶液を注入することで人工細胞核の構築に成功|生命理工学系 News
- 遺伝子の活性化をリアルタイムで検出する「STREAMING-Tag」システムを開発|生命理工学系 News
- 細胞内で破壊された核膜の修復機構におけるラミン分子の役割を解明|生命理工学系 News
- 生細胞内タンパク質の量と動態を蛍光抗体で観察することに成功|生命理工学系 News
- 蛹期に備えて幼虫脂肪体のオートファジーは抑制される|生命理工学系 News
- 遺伝子の転写の「伸長」場所は動きやすいことを発見|生命理工学系 News
- DNA複製へのスイッチ、鍵は何?|生命理工学系 News
- 組織の細胞集団に潜む幹細胞のエピゲノム解析手法を開発|生命理工学系 News
- 細胞内抗体プローブを用いて遺伝子の転写が活性化している細胞を生体内で特定することに成功|生命理工学系 News
- 同一の細胞から複数のエピゲノム情報を同時に検出する技術開発に成功|生命理工学系 News
- 発生過程の胚での最初の遺伝子発現のきっかけを作る重要なヒストン修飾を発見|生命理工学系 News
- ヒストンタンパク質の翻訳後修飾の可視化に成功 エピジェネティックマークを色で観察する細胞内抗体プローブ開発|生命理工学系 News
- 生細胞イメージングのための新しい分子ツールを開発|生命理工学系 News
- 世界初!ヘテロクロマチンによる染色体異常の抑制を発見|生命理工学系 News
- 世界初、単一細胞での遺伝子発現制御解析に成功|生命理工学系 News
- 受精卵から体の様々な細胞や組織に分化する仕組みの解明~エピゲノムの研究~ — 木村宏|生命理工学系 News
- 木村 宏 Hiroshi Kimura|研究者検索システム Science Tokyo STAR Search
- 木村研究室
- 細胞制御工学センター
- 生命理工学院 生命理工学系
- 総合研究院|大学組織一覧|Science Tokyoについて