生命理工学系 News
熱ショックタンパク質が自身を増産する新たな仕組みを発見
タンパク質を「余らせず補充する」新たな調節機能
要点
- 低分子量の熱ショックタンパク質は、有害なタンパク質を凝集させて細胞内で隔離する
- 大腸菌の低分子量熱ショックタンパク質が、タンパク質凝集の蓄積に伴う自身の消費を感知し、速やかに合成量を増やす仕組みを発見
- 本研究成果を応用することで、細胞中の凝集体蓄積レベルを生きたまま測ることができると期待
概要
東京工業大学 科学技術創成研究院 細胞制御工学研究センターの三輪つくみ研究員、茶谷悠平特任助教、田口英樹教授(生命理工学コース主担当)の研究グループは、熱ショックタンパク質(ヒートショックプロテイン:Hsp)[用語1]の一種がストレス時の細胞内における自身の消費を感知し、合成を促すことで補充する新たな仕組みを発見した。
細胞に熱などのストレスがかかると、凝集体と呼ばれるタンパク質でできたゴミが発生する。この凝集体すなわちゴミは細胞内に蓄積すると毒性を示すため、どのような生物も凝集体の生成を抑制もしくは隔離・分解などにより処理する仕組みを備えている。処理を行うタンパク質群は凝集体が発生しやすい高温ストレスによって合成が促進されることから、熱ショックタンパク質(Hsp)と呼ばれる。Hspの中でも、凝集体の隔離や分解の補助を行う低分子量Hspは凝集体処理の最初のステップを担う重要なタンパク質で、バクテリアからヒトまでほとんどすべての生物に備わっている。
研究グループは、大腸菌の低分子量Hspの合成が、高温ストレスとは無関係に凝集体が蓄積することで促進されることを発見した。さらに、この仕組みが凝集の蓄積に伴う低分子量Hspの消費をトリガーとしていることを発見した。今回の発見により、低分子量Hspが自身の不足をすぐに補えるように、かつ細胞内で余らせることがないように厳密に制御されていることが明らかになった。 この成果は、低分子量Hspが自身の合成のフィードバックを司るという点でHsp発現制御機構の新たな仕組みの発見であり、ストレス応答という生命に普遍的な現象に対する理解を深めるものともいえる。また、本研究成果を応用することで、細胞中の凝集体蓄積レベルを生きたまま測ることができると期待される。
研究成果は9月21日付の米国の学術誌「Molecular Microbiology(分子微生物学)」電子版に掲載された。
研究の背景と経緯
タンパク質は細胞内の化学反応の触媒や構造の保持を行うなど生命活動に必須の生体高分子である。タンパク質が細胞内で機能を発揮するには、DNAに記された遺伝情報のコピーを取る転写、コピーされた遺伝情報に基づきアミノ酸をつなぐ翻訳、そしてつながったアミノ酸(ポリペプチド鎖)が正しい立体構造を取るフォールディングという過程を経る必要がある。
フォールディングを失敗したタンパク質やストレスに晒されて立体構造が崩れたタンパク質は、正しい立体構造をとることができずにタンパク質凝集体と呼ばれる無秩序な分子集合体を形成する。タンパク質が凝集体になると機能を失うだけでなく、細胞にとって有害になることもある。そのため、どのような生物もタンパク質凝集体を細胞内の特定の位置に隔離し、分解などの処理をする仕組みを備えている。
タンパク質が凝集してしまう代表的な要因が高温ストレスで、そのため、生物は高温ストレスに晒されることで合成される熱ショックタンパク質(Hsp)を備えることでタンパク質凝集体に対処している。
低分子量Hspはバクテリアからヒトまで進化的に保存されたHspで、タンパク質凝集を細胞内で隔離、さらには分解などを補助し、タンパク質凝集体の処理効率を上昇させる役割を果たしている。このことから近年では低分子量Hspがタンパク質凝集体処理の第一段階を担う分子として認識されている。
Hspは熱に晒されることで転写が促進されることが知られていたが、低分子量Hspについてはタンパク質凝集体が蓄積することで、温度に依らず細胞内における量が増加する現象が過去に知られていた。研究グループはこの増加が低分子量Hsp自身による調節機能によるものであることを見つけ、さらにその調節機能が従来から知られている転写段階の制御ではなく、タンパク質凝集体の蓄積に応じて機能する翻訳段階の制御であることを明らかにした。
研究内容と成果
本研究グループは、低分子量Hspの翻訳を再現したレポーター系[用語2]を用いて、タンパク質凝集体が蓄積した大腸菌細胞内では低分子量Hspの翻訳量が増加することを発見した。さらに調査したところ、低分子量Hspは自身の翻訳を自ら抑制する役割を持っていることを見つけた。この役割はタンパク質凝集体と低分子量Hspが結合すると機能しないため、タンパク質凝集体との結合により低分子量Hspが消費されると、翻訳によって発現量が増えるという仕組みである(図1)。この結果は、これまでタンパク質凝集体と結合することが役割だと思われていた低分子量Hspが、ストレスの感知と翻訳の調節因子という役割も担っていることを示している。
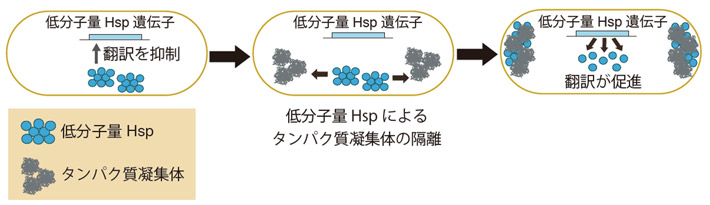
図1. タンパク質凝集体の蓄積の感知と低分子領Hspの発現
Hspは細胞が熱に晒されることで転写が促進されることが知られていた。しかし、本研究によって大腸菌の低分子量Hspは、タンパク質凝集体の蓄積によって消費されることが引き金となり、温度に関係なく翻訳が促進されることがわかった。
今回の発見により、低分子量Hspはストレスの無いときは自らの翻訳を抑え、ストレス時には促進するという制御機構を備えていることがわかった。しかし、他のHspにはストレスの無い状況下で合成を抑えるような、厳密な制御機構は見られない。なぜ低分子量Hspはこのように厳密な制御機構を備えているのだろうか?
低分子量Hspは互いに相互作用し、くっつきやすい性質をしている。これは、自身も強固なタンパク質凝集体となりやすいことを示している。そのため低分子量Hspが細胞内にたくさん余っている状態は細胞にとって毒となってしまうと考えられる。実際に研究グループは低分子量Hspを過剰に作らせると大腸菌の生育が悪くなることも示している。このように、細胞はストレス時には真っ先に必要となるが、余らせると害となるようなタンパク質である低分子量Hspを、必要量だけ保持するために、今回見つけた仕組みを利用していると考えられる(図2)。
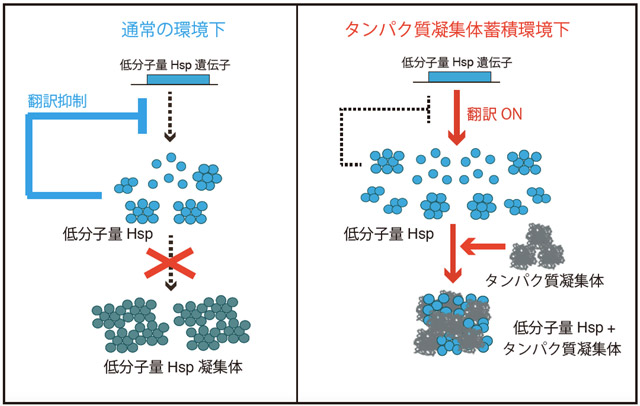
図2. 低分子量Hspの発現量調節
低分子量Hspは、自身もタンパク質凝集体となりやすい性質である。今回発見された制御機構は低分子量Hspが細胞内で凝集体を形成しないよう、必要な量だけ合成を促し、余らせないための仕組みであると考えられる。
今後の展開
タンパク質凝集体の蓄積は全ての生物で起こり得る現象であり、様々なストレスと結びついている。本研究はタンパク質凝集体の蓄積の度合いに応じて特定のタンパク質が増産されることを見いだした(図3)。この制御機構を応用することで、生きている細胞のタンパク質凝集体の蓄積の程度をモニターし、タンパク質凝集体とストレスの関係性を深く探る研究の手がかりとなることが期待できる。
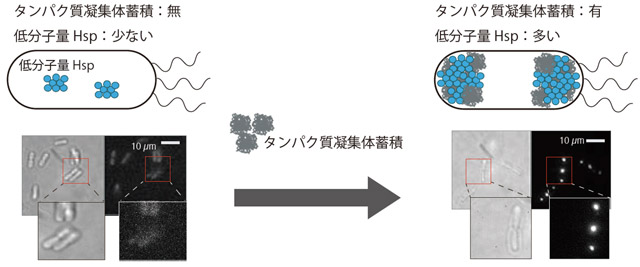
図3. 低分子量Hspの発現によるタンパク質凝集体蓄積の可視化
低分子量Hspはタンパク質凝集体の蓄積により発現量が変化する。そのため、タンパク質凝集体の蓄積は低分子Hspに緑色蛍光タンパク質[用語3]を融合させることで生きている細胞内のタンパク質凝集体の蓄積度合いが測定できる。
- 用語説明
[用語1] 熱ショックタンパク質(ヒートショックプロテイン:Hsp) : 細胞が熱、化学物質などのストレスにさらされた際に発現が上昇して細胞を保護するタンパク質の一群。
[用語2] レポーター系 : 遺伝子の発現を観測するため、観察対象の遺伝子の発現制御領域と、特定の蛍光や化学反応を示してレポーターとなる遺伝子を融合した遺伝子を発現させる実験系。
[用語3] 緑色蛍光タンパク質 : クラゲ由来の緑色の蛍光を示すタンパク質で本研究ではレポーターとして使われている。
- 論文情報
| 掲載誌 : | Molecular Microbiology |
|---|---|
| 論文タイトル : | Escherichia coli small heat shock protein IbpA is an aggregation‐sensor that self‐regulates its own expression at posttranscriptional levels |
| 著者 : | Tsukumi Miwa, Yuhei Chadani, Hideki Taguchi |
| DOI : | 10.1111/mmi.14606 |
- 酵母プリオンタンパク質のアミロイド線維形成を直接観察│生命理工学系 News
- 合成途上のタンパク質が故意に合成を中断する現象を発見 ―細胞内の環境変化を感知する新たなしくみ―│生命理工学系 News
- タンパク質合成過程における「緩急のリズム」を実証―大腸菌遺伝子産物の中間状態を網羅的に解析―│東工大ニュース
- 細胞内で「タンパク質の一生」を支える脇役 シャペロンの謎解明に向けさらなるステージへ ― 田口英樹│研究│研究ストーリー
- 平成30年度手島精一記念研究賞 授与式を挙行│生命理工学系 News
- 【研究室紹介】田口研究室│生命理工学系 News
- 田口ラボ
- 研究者詳細情報(STAR Search) - 田口英樹 Hideki Taguchi
- 科学技術創成研究院 (IIR)
- 科学技術創成研究院 細胞制御工学研究センター
- 生命理工学院 生命理工学系
- 研究成果一覧
お問い合わせ先
東京工業大学 科学技術創成研究院
細胞制御工学研究センター
教授 田口英樹
E-mail : taguchi@bio.titech.ac.jp
Tel / Fax : 045-924-5785