生命理工学系 News
【研究室紹介】林研究室
タンパク質に駆動される システムとしての生命の本質に迫る
生命理工学系にはライフサイエンスとテクノロジーに関連した様々な研究室があり、基礎科学と工学分野の研究のみならず、医学や薬学、農学等、幅広い分野で最先端の研究が活発に展開されています。
研究室紹介シリーズでは、ひとつの研究室にスポットを当てて研究テーマや研究成果を紹介。今回は、タンパク質に駆動されるシステムとしての生命の本質に迫る、林研究室です。

主担当 生命理工学コース
副担当 人間医療科学技術コース/ライフエンジニアリングコース
教授 林宣宏![]()
| キーワード | 臨床プロテオミクス、健康科学、抗体、細胞膜脂質ラフト |
|---|---|
| Webサイト | 林研究室 |
研究紹介
遺伝子(DNA)は細胞を駆動するバイオナノマシンの設計図であり、遺伝情報をもとにつくられるバイオナノマシンがタンパク質です。私たちの研究室では生命現象を分子レベルで完全に理解するために、そのタンパク質の細胞内での機能に着目しています。その際、個々のタンパク質分子を観るだけではなく、生命システムを構成している総てのタンパク質を網羅的に俯瞰しなければ生命現象の本質は解らないと考えています。
近年、細胞が多様な状況に迅速かつ適切に対処するために、生体膜上でドラスティックかつ局所的に生成、消滅する、様々な蛋白質と脂質からなる機能場(細胞膜脂質ラフト)が、シグナル受信の最前線における迅速かつ適切なシグナル処理のために機能していることが分かりました。細胞膜脂質ラフトを生命システムと捉え、その機能発現の本質を理解するために、タンパク質一分子を生きた細胞内で観察する手法、細胞内のタンパク質を網羅的に調べる手法(プロテオミクス)、また、タンパク質を抗体を用いて操作する手法を独自に開発して研究を進めています。
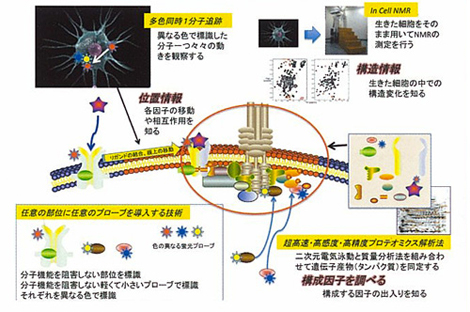
ここで開発した独自の手法は、それぞれ、本研究以外にも様々な対象に使われています。
ハイスループットで、高い再現性(多数の検体の相互比較が可能)、かつ、高感度(少量のサンプルで実施可能)でデータを得ることが出来る二次元電気泳動法を開発したことで、当該分野がこれまでは苦手としてきた臨床研究や工業の分野にプロテオミクスを拡げようとしています。また、機能を改変したバクテリアをプロテオミクスで調べることにより、高性能の物質生産系の開発を進めています。
さらに、任意の抗原に適用出来て、タンパク質工学によりその機能を改変出来る抗体が得られる抗体ライブラリーの手法を用いて、バイオナノツールの開発も進めています。
研究目的
生体は細胞から成るが、その細胞を駆動しているのは細胞内生体高分子である。そのなかで、バイオナノマシンとして様々な役割を担っているのが蛋白質である。遺伝子にはこのバイオナノマシン(蛋白質)の設計図が書かれているが、設計図を調べるだけではシステムとしての細胞を理解することは難しい。本研究では、細胞内の蛋白質の量的、および、(プロセッシングや翻訳後修飾といった)質的な動態を、網羅的、かつ、俯瞰的に調べることで、細胞の究極のプロファイリングを行う。
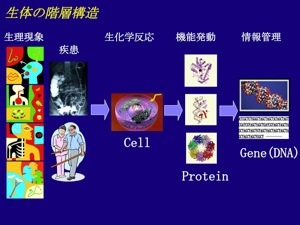
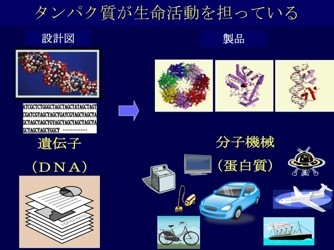
研究の背景
試料の調製方法(検体からのタンパク質の抽出、等)の最適化法、1)ハイスループット性能、2)高感度、3)高い再現性、を特徴とする二次元電気泳動法、および、チューンナップした質量分析装置を組み合わせた高精度ハイスループットプロテオミクス解析システムを開発した(日刊工業新聞:2009年11月18日掲載)。これまで、プロテオミクス解析では、その基盤技術である二次元電気泳動に手間ひまがかかることから、多検体の解析にはあまり用いられなかったが、ハイスループット性能と高い再現性を有する本法では多検体の処理が可能となり、これまでに、細胞から組織にいたる様々な対象の解析に用いてきた(下図:解析例の一部)
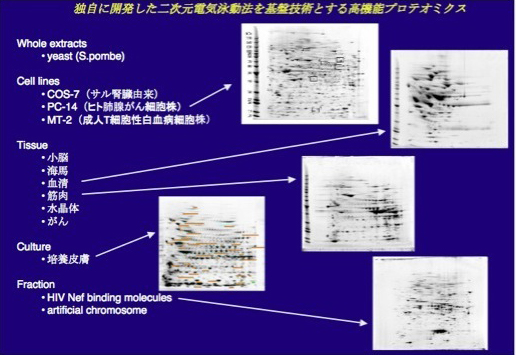
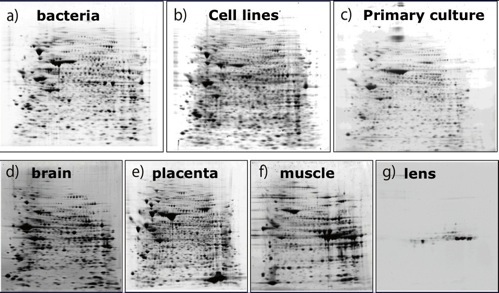
研究のテーマ
生命の状態をプロファイルする;次世代プロテオミクス
システムとしての細胞の理解による生命の本質の解明
生命を理解するためには、細胞をシステムとして理解しなければいけない。細胞を駆動しているタンパク質の状態を網羅的、かつ、俯瞰的に調べて、その量的、および、質的な変化を知る事は、その細胞の状態を把握(プロファイル)する究極の方法である。本研究では、独自に開発したHigh Performance Proteomicsの手法を用いた細胞のプロファイリング法を開発し、個々のタンパク質を個別に見るだけでは得られない知見を獲得することによって、生命現象のこれまでとは異なる側面を知ることで、生命の本質に迫ることを目的とする。
現在、下記の研究を進めています。
生命の理解
- 細胞融合の分子機構
- 高度高熱菌の細胞内シグナル伝達系
- 分裂酵母の極限環境発現遺伝子の探索
- 魚を用いた情緒発動の分子機構の解明
疾患の診断と治療
- アトピー性皮膚炎の発症機構
- 骨芽と破骨のバランスによる骨の健常管理
- 分娩異常に関わる遺伝子の研究
- 低レベル放射線の生体への影響
- 敗血症の発症高速高精度診断法の開発
- リハビリテーションの高精度診断法の開発
バイオテクノロジー開発
- 分裂酵母を用いた高性能物質生産系の開発による未使用バイオマスの活用
疾患プロテオミクスによる診断、治療法の開発
これまでのプロテオミクスでは時間がかかり、さらに、多検体を同時に比較することが困難であったので、多数の患者さんを短時間に診なければいけない臨床現場における実用化は難しかった。本研究室では、ハイスループット、高感度、かつ、高い再現性を有する手法の開発に成功したので、この技術を基盤に臨床プロテオミクスの開発を進めている。
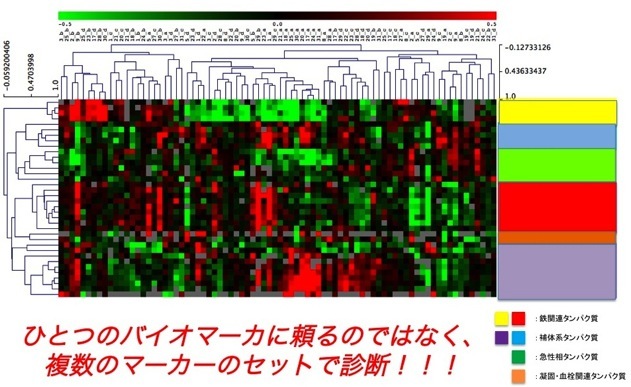
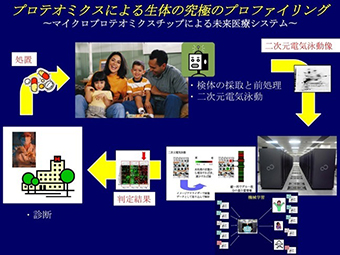
プロテオミクスチップによる未来型健康社会の実現
細胞機能を制御し駆動しているのは多種多様な機能を持ったバイオナノマシンである蛋白質である。蛋白質によって制御し駆動されている細胞の性質や状態は、そのシステムを構成している多種多様な蛋白質の種類と量と状態により決まる。従って、蛋白質の種類と量と状態を網羅的かつ俯瞰的に調べること(プロテオミクス)は、細胞(生体)の究極のプロファイリングである。しかしながら、プロテオミクスは、その手技の難しさから、これまで研究においては用いられても、医療や産業において実用化されることはほとんど無かった。 近年、我々は、プロテオミクスを実用化するために、プロテオミクスの基盤技法である二次元電気泳動技術の(大量の検体を扱うための)ハイスループット化と(微量な検体でも分析を可能とする)高感度化に成功した。この技術を用いてこれまでは扱えなかった分野にプロテオミクスを拡げることを試み、それにも成果が得られたので、現在、さらに適用範囲を拡充するために、簡便に扱えて持ち運べるような小型の装置の開発と大量のデータの自動解析アルゴリズムの開発を進めている。家庭で、簡単に健康診断が出来るシステムを開発し、高額医療費と超高齢化社会の問題を解決することで、未来型健康社会を実現する。
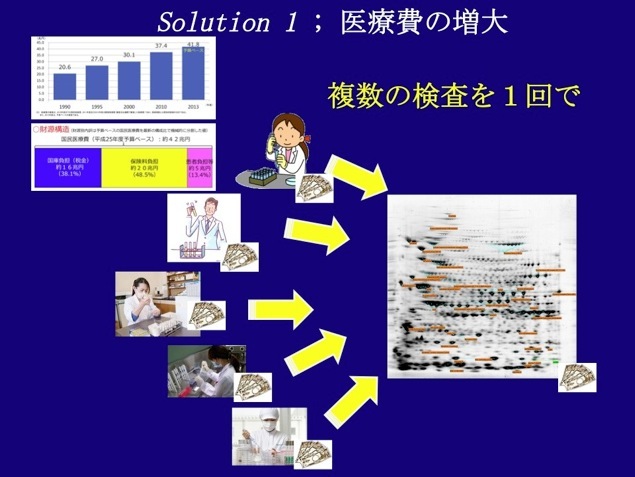

我が国では医療費の膨張が財政を圧迫し、現在では総GDPの10%近く、社会保障費の約3分の1を占めている。この比率は、今後、高齢者化が進むに従って益々増大することが必至である。また、高齢者化が進むのに伴い、高齢者のQOL(Quality Of Life)を考慮した社会規模での生活環境の変革がこれから必要となる。
本課題では、早期、かつ、網羅的な健康診断技術を基盤とする、社会規模での在宅・未病(発病前の状態)での健康管理システムによる医療費の抜本的な大幅削減を目指す。本プロジェクトで開発する在宅、かつ、汎用の健康診断システムは、通院不要でオーダーメイドの健診による高齢者のQOLの高レベルでの維持を実現する。
研究成果
1. ミリストイル化(14炭素飽和脂肪酸による翻訳後修飾)によるタンパク質の機能制御(細胞膜領域と細胞内のシグナルの伝達)の仕組みミリストイル化(14炭素飽和脂肪酸による翻訳後修飾)によるタンパク質の機能制御(細胞膜領域と細胞内のシグナルの伝達)の仕組み(右図)を解明しました。 神経細胞や免疫細胞、また、分化途中の細胞でこの仕組みが使われていることを明らかにしましたが、現在はほとんど全ての細胞で使われていると考えています (1-10) 。
2. 細胞内には、数百から数千のミリストイル化タンパク質が存在する可能性を示しました(11)。特に、細胞膜脂質ラフトにおいてミリストイル化タンパク質が機能していることが示され、現在、ラフトの機能を解明するための研究を進めています。
3. ミリストイル化タンパク質を検出したり、制御したりするのに使える抗体を開発しました(12)。
4. たんぱく質素早く解析高性能の二次元電気泳動法を開発しました(13-18)。この手法を基盤として、これまでに基礎研究から臨床、工業にまで及ぶ、様々な対象に特化したプロテオミクス法を開発し、現在、多くの共同研究を進めています。
- [1] Matsubara M, Yamauchi E, Hayashi N, Taniguchi H:MARCKS, a major protein kinase c substrate, assumes non-helical conformations both in solution and in complex with Ca2+-calmodulin. FEBS Lett. 421: 203-207, 1998
- [2] Takasaki A, Hayashi N, Matsubara M, Yamauchi E, Taniguchi H:Identification of the calmodulin-binding domain of neuron-specific protein kinase C substrate protein CAP-22/NAP-22. J.Biol.Chem. 274: 11848-11853, 1999
- [3] Hayashi N, Izumi Y, Titani K, Matsushima N:The binding of myristoylated N-terminal nonapeptide from neuron-specific protein CAP-23/NAP-22 to calmodulin induces a 'relaxed' globular structure different from the calmodulin - non-myristoylated peptide complex. Protein Science 9: 1905-1913, 2000
- [4] Hayashi N, Matsubara M, Jinbo Y, Titani K, Izumi Y, Matsushima N:Nef of human immunodeficiency virus type 1 (HIV-1) interacts directly with calcium-bound calmodulin. Protein Science 11: 529-537, 2002
- [5] Matsubara M, Hayashi N, Jing T, Titani K:Regulation of Endothelial Nitric Oxide Synthase by Protein Kinase C. J.Biochem. 133: 773-781, 2003
- [6] Matsubara M, Titani K, Taniguchi H, Hayashi N:Direct involvement of protein myristoylation in MRACKS-calmodulin interaction. J.Biol.Chem. 278: 48898-48902, 2003
- [7] Hayashi N, Nakagawa C, Takasaki A, Jinbo Y, Yamakawa Y, Titani K, Hashimoto K, Izumi Y, Matsushima N:Myristoylation-regulated direct interaction between calcium-bound calmodulin and N-terminal region of pp60v-src.J.Mol.Biol. 338: 169-180, 2004
- [8] Matsubara M, Jing T, Kawamura K, Shimojo N, Titani K, Hashimoto K, Hayashi N:Myristoyl moiety of HIV Nef is involved in regulation of the interaction with calmodulin in vivo.Protein Sci. 14: 494-503, 2005
- [9] Hayashi N: Novel intracellular signaling mechanism revealed by functional analyses of myristoyl moiety of NAP22 and a comprehensive analysis of Nα-myristoylated proteins.Current Proteomics, 4: 162-173, 2007
- [10] Hayashi N, Titani K: N-myristoylated proteins, key components in intracellular signal transduction systems enabling rapid and flexible cell responses. Proc.,Jpn.,Acad.,Ser.B, 86(5):494-508, 2010?
- [11] Maurer-Stroh S, Gouda M, Leite FS, Novatchkova M, Schleiffer A, Schneider G, Wildpaner M, Hayashi N, Eisenhaber F:MYRbase: Evaluation of genome-wide glycine myristoylation enlarges functional spectrum of eukaryotic myristoylated proteins. Genome Biology 5: Article R21, 2004
- [12] 発明者:林 宣宏、赤堀 泰、“抗ミリストイル化タンパク質抗体又はその抗原結合フラグメント、ミリストイル化タンパク質検出キット、医薬、遺伝子、及びベクター”出願人:東京工業大学、出願番号:特願2013-088891、出願日:2013年4月19日
- [13] 発明者:中村政志、林宣宏,"等電点電気泳動用ゲル及び等電点電気泳動方法",出願番号 特願2009-181808,出願日:2009年8月4日
- [14] 発明者:中村政志、林宣宏,"等電点電気泳動用膨潤ゲルの作成方法",出願番号 特願2009-181809,出願日:2009年8月4日
- [15] 発明者:中村政志、林宣宏,"等電点電気泳動方法及び粗雑物除去の判定方法",出願番号 特願2009-181810,出願日:2009年8月4日
- [16] 発明者:中村政志、林宣宏,"2次元電気泳動方法",出願番号 特願2009-181811,出願日:2009年8月4日
- [17] 発明者:中村政志、林宣宏,"2次元電気泳動方法",出願番号 特願2009-181812,出願日:2009年8月4日
- [18] 生体の高精度かつハイスループットなプロファイリング:改良型2次元電気泳動法を基盤技術に用いる高性能プロテオミクス、林 宣宏、 未来材料、11(1),42-49,2011
教員紹介
林宣宏 教授 博士(理学)
| 1989年 | 東京大学理学部物理学科卒業 |
|---|---|
| 1994年 | 東京工業大学大学院 総合理工学研究科 生命化学専攻 博士課程修了(理学博士) |
| 1994年 | 藤田保健衛生大学 総合医科学研究所 助手 |
| 2002年 | 藤田保健衛生大学 総合医科学研究所 講師 |
| 2005年 | 藤田保健衛生大学 総合医科学研究所 助教授 |
| 2007年 | 藤田保健衛生大学 総合医科学研究所 准教授 |
| 2008年 | 東京工業大学 大学院生命理工学研究科 分子生命科学専攻 准教授 |
| 2004~2005年 | 山形大学工学部 非常勤講師(兼任) |
|---|---|
| 2006~2007年 | 名古屋大学工学部 非常勤講師(兼任) |
| 2008~2009年 | 岐阜大学工学部 非常勤講師(兼任) |
| 2008~2008年 | 山形大学工学部 非常勤講師(兼任) |
| 2008年~ | 理化学研究所 客員研究員(兼任) |
- 所属学会
- 日本分子生物学会、日本生化学会、蛋白質科学会、日本生物物理学会、Protein Society, USA、The American Society for Biochemistry and Molecular Biology
教員からのメッセージ
- 林教授より
-
生命は長大な時間のなかで創り上げられた極限まで洗練された自立システムです。
その本質を知るにはシステムを構成する因子の機能構造の分子レベルでの理解はもちろんのこと、それらを俯瞰して全体の動きやそれらがお互いに与え合う影響を総体的にとらえ理解することが必要です。
生命現象の本質が理解出来れば、学術的に、あるいは臨床において大きな発展が期待出来るだけでなく、その動作原理をとりいれた新しい自立型人工システムの開発へとつながります。
そのための手法や概念の構築は未だ発展途上ですが、(素要素の開発により)技術的にも(ポストゲノムにおいて)状況的にも現代はそれが出来る時代となりました。
これから研究に参画するひとには、この時代に生まれた幸運を解って、生命の本質を解き明かす醍醐味を謳歌してもらいたいと思います。
- 生命理工オープンイノベーションハブ|未来健康科学グループ
- 未来型スポーツ・健康科学研究推進体|東京工業大学
- 第25回高校生のための夏休み特別講習会「バイオの世界を探検してみよう」開催報告|生命理工学系 News
- 動画で見る東工大研究2023 ~4分で知る!未来を創る最先端研究~|生命理工学系 News
- 研究室と研究テーマ
お問い合わせ先
教授 林宣宏
大岡山キャンパス
緑が丘6号館 3階 302号室
E-mail : nhayashi@bio.titech.ac.jp
※この内容は掲載日時点の情報です。最新の研究内容については研究室サイト![]() をご覧ください。
をご覧ください。
※ 2025年5月1日:一部最新の情報に更新しました。