生命理工学系 News
【研究室紹介】 占部・秦研究室
バイオの原点・有機化学 ― 新反応開発から医薬品まで
生命理工学系にはライフサイエンスとテクノロジーに関連した様々な研究室があり、基礎科学と工学分野の研究のみならず、医学や薬学、農学等、幅広い分野で最先端の研究が活発に展開されています。
研究室紹介シリーズでは、ひとつの研究室にスポットを当てて研究テーマや研究成果を紹介。今回は、有機化合物を自在に変換・合成するための新しい手法を開発し、生物活性化合物、医薬、有機材料を合成する、占部・秦研究室です。
※占部教授は2023年3月31日、東工大を定年退職しました。
※WEBサイトの修正を行いました。2023年6月7日

主担当 生命理工学コース
教授 占部弘和 准教授 秦猛志![]()
| キーワード | 有機化学、合成化学、医薬品化学、天然物化学 |
|---|---|
| Webサイト | 秦研究室 |
研究紹介
バイオの原点 有機化学
- 分子を組み立てる出発点はここ、そして分子を自在に操る者が先端をも制す!
- 新反応開発から生物活性化合物や医薬の合成へ
理工学の観点からのバイオ研究としては、自然にある物質や現象を単に観察・解析するだけでなく、それらを人工的に応用利用することが重要です。
我々のグループでは、バイオ研究の対象である有機分子を思いどおりに合成・変換する新しい合成手法の開発を行い、それらを利用して天然の有機化合物や人工の医薬などの生理活性化合物を実際に手に取ることを可能にしてきました。
特に最近では、新反応を基軸として、いかに短工程で効率よく合成するか、いかに安全な試薬を利用し、不要な廃棄物を軽減するかなど、持続可能社会に必須な「効率性」、「安全性」および「経済性」を重視した未来型反応開発を展開し、次世代の「ものづくり」に貢献するべく研究を推進しています。

2016年研究室集合写真
エキサイティングな有機合成化学
有機合成反応の開発を行っていると、えてして想像を超える「非常識」な現象が起こります。
我々のグループでは、こういったエキサイティングな現象を見逃さないように注視し、見つけた現象を体系化することによって、新概念・新反応機構を開拓して斬新な分子変換反応を開発すること、それらを利用して新しい有機化合物を合成することを研究の基盤としています。
その「非常識」な現象をはじめに発見するのは、ベンチに向かって実験を行っている人(学生)です。
学部生、大学院生、学年を問わず、その現象を手にするチャンスが皆にあります。

すずかけ祭名物

2016年秋 バーベキュー
生物活性化合物の合成
従来の生物活性化合物や医薬の合成は、既存の手法を組み合わせて行うため、効率的とは言えないケースもあり、問題点が山積しています。
我々のグループでは、上述の斬新な分子変換反応から生み出された新規な有機化合物を利用することにより、次世代にふさわしい効率性、経済性、および環境調和性を満足する生物活性化合物や医薬の合成にチャレンジしています。
更に、これまで合成が不可能と考えられていた新規な有機化合物を実際に手にすることにより、新しい発想に基づく応用利用を可能にし、思いもよらぬ有機分子の新機能開拓へ展開できると期待しています。
―高校生向け― 「生物活性化合物や医薬を化学合成する」とは?
数百~千程度の分子量から成る分子は、生物や細胞のスケールからみると非常に小さいですが、たんぱく質・DNA等の「巨大な分子」に直接作用することにより、その巨大な分子の機能を発現させたり、失活させたり、調整することができます。
こういった分子を「生物活性化合物」と呼んでおり、人間は古くから、例えば薬草として摂取・利用してきました。
現在では生薬・抗生物質など医薬品として広く使われています。
これら分子の生産を植物、微生物、あるいは動物に頼っている場合には、そもそも微量しか得られなかったり、変異によって突然に手に入らなくなってしまったり、というリスクがありますので、生物活性化合物を化学によって、人工的につくること、つくれることが重要です。
さらに、人工的に生物活性化合物をつくることができれば、活性を高め、副作用を抑えるための、分子のかたちを改良した化合物(医薬)を創ることに?がります。
研究内容
現在、占部・秦研究室では、以下の分子変換反応の開発に積極的に取り組んでおり、それらを利用した生物活性化合物や医薬合成を行なっています。
- 薬剤分子の創製のための分子変換反応
- 遷移金属触媒反応、多成分ワンポット反応とその利用
- 低環境負荷・経済的な未来合成反応の開発
- 廃棄物を出さない分子再構成反応の開発、安全・経済的な試薬利用への変換
- バイオ分子の利用および変換手法の開発
- バイオ分子をキラル源とする触媒的不斉反応
以下には、最近の研究のトピックスを項目別に記載しています。
1. アミノ酸を利用する触媒的不斉合成法の開発
触媒的不斉合成法は、近年の有機化学の中心的課題の一つであり、光学活性な生物活性化合物の入手のためには必要不可欠な手法である。我々のグループでは、不斉源として安価で入手容易なアミノ酸を触媒に組み込むことにより、キラルなロジウム触媒の調製を可能にし、それを利用して触媒的不斉C-H結合活性化環化反応により、光学活性なヘテロ環を合成することができた(C-H結合活性化に関しては後述する)。
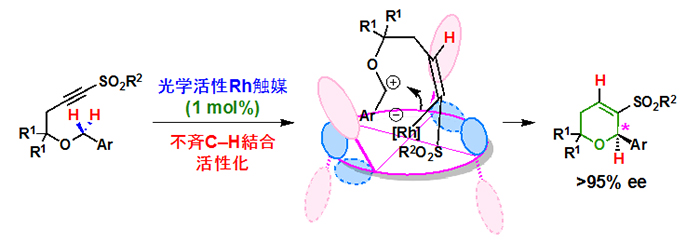
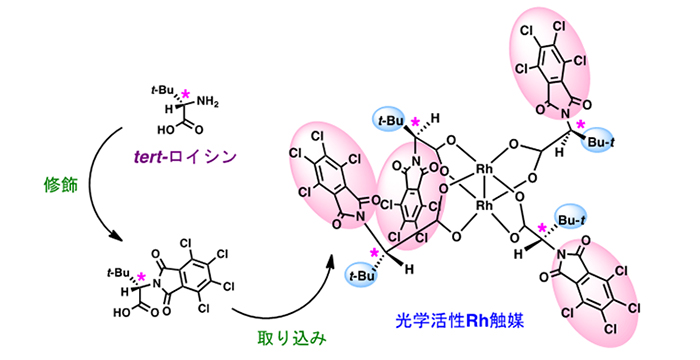
2. 医薬品に多用されるヘテロ環の効率的合成法の開発
ヘテロ環合成法は従来から数多く知られているが、新規かつ簡便な合成法の開発は現在でも活発に研究がなされている。我々のグループでは、ハロアセチレンに対して各種求核剤が効率良く求核付加することを見出し、続くパラジウム触媒によるC-H結合活性化環化反応により、種々のヘテロ環が合成できることを見出した。更に、この研究によって見出されたヘテロ環は、実際に生物活性化合物の骨格として利用されている。
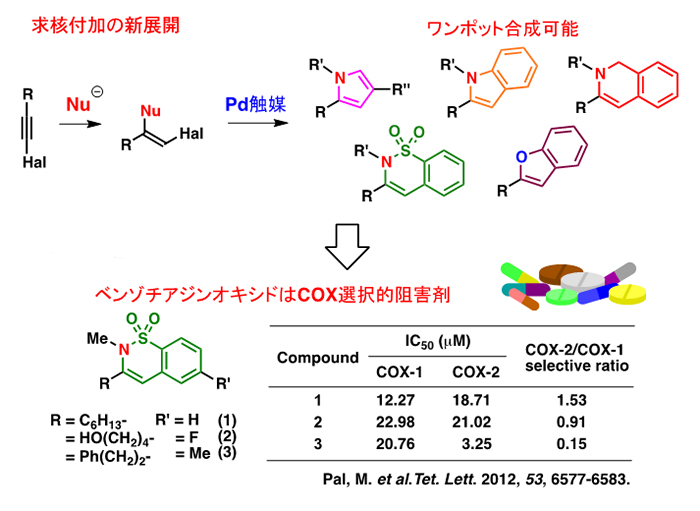
3. サスティナブルな触媒による新合成法の開発
鉄は「豊富・安価・無毒」の三拍子が揃った遷移金属であるにもかかわらず、その他の希少金属と比較すると、有機合成反応の開発および利用が十分とは言えなかった。我々のグループでは、鉄触媒存在下で種々の不飽和結合に対するグリニャール試薬の付加が選択的に進行することを見出し、その応用利用も行なった。
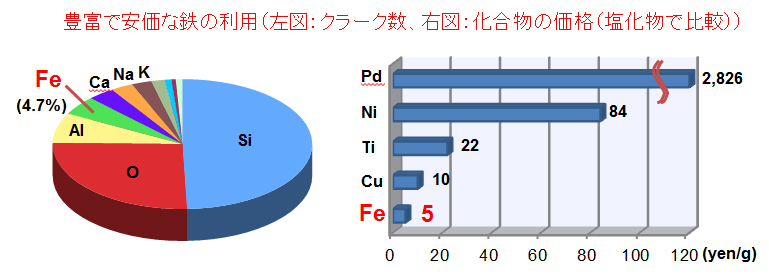
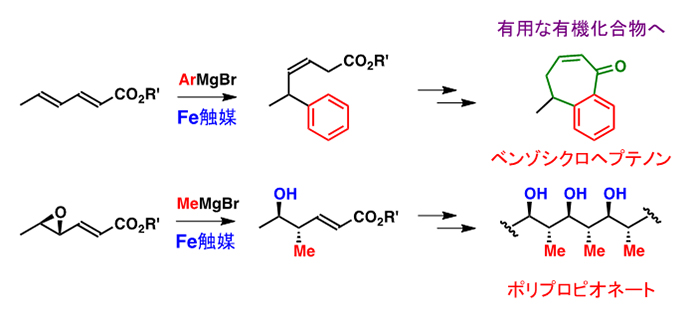
4. 効率的なワンポット合成の新手法の開発
ワンポット反応は、実験操作を簡略化すると同時に、用いる試薬や溶媒を減らすことができるなど様々な利点がある。我々のグループでは、種々のワンポット反応を開発しているが、一例として下記に示すように、ワンポットで連続的に 4回の炭素-炭素結合形成反応が進行し、一挙に3成分をカップリングする多成分連結反応を見出した。この反応は、特異なシクロブテンユニットの構築にも有用である。
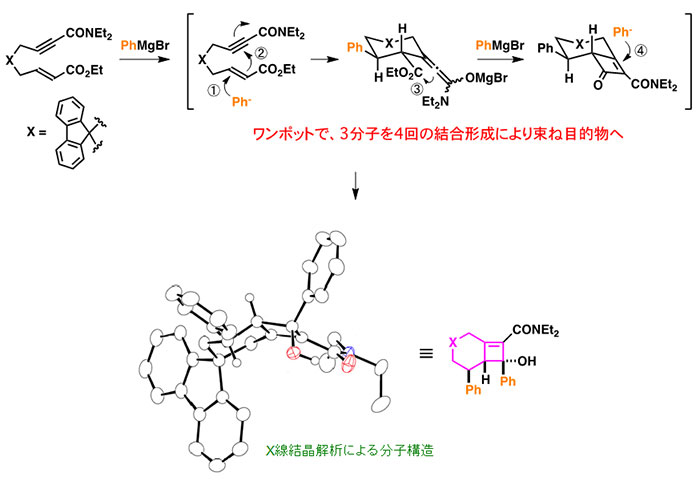
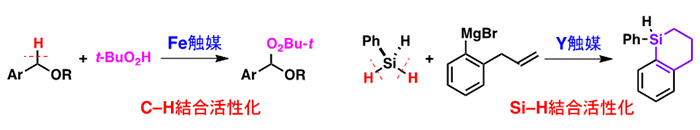
5. C-H、Si-H結合等の活性化による新合成法の開発
反応不活性なC-H結合を切断して、新たなC-C結合や官能基形成を行うことを「C-H結合活性化反応」と言い、従来の有機化学の枠を超える未来型反応として、最近特に注目を集めている。我々のグループでは、上記項目1、2以外にも、鉄触媒による新規な過酸化物合成や、イットリウム触媒による環状ケイ素化合物合成に利用できることを見出した。
6. バイオ分子変換の新手法の開発
核酸、ペプチド、ポリアミン、アミノ糖、アルカロイドなどバイオ分子のアミノ基を利用して、分子構造を局部的に改変できれば、生理活性の改変、分子タグの導入、医薬のための多様な誘導体の入手等々に幅広く貢献できる。我々のグループでは、生体分子に散見されるアミノ基を新たな発想で脱離基に変換し、これが接続する炭素バックボーン上に直接求核剤を接続させる新しいタイプの反応を見出した。

- 我々のグループで開発した新反応により合成される生物活性化合物や医薬など
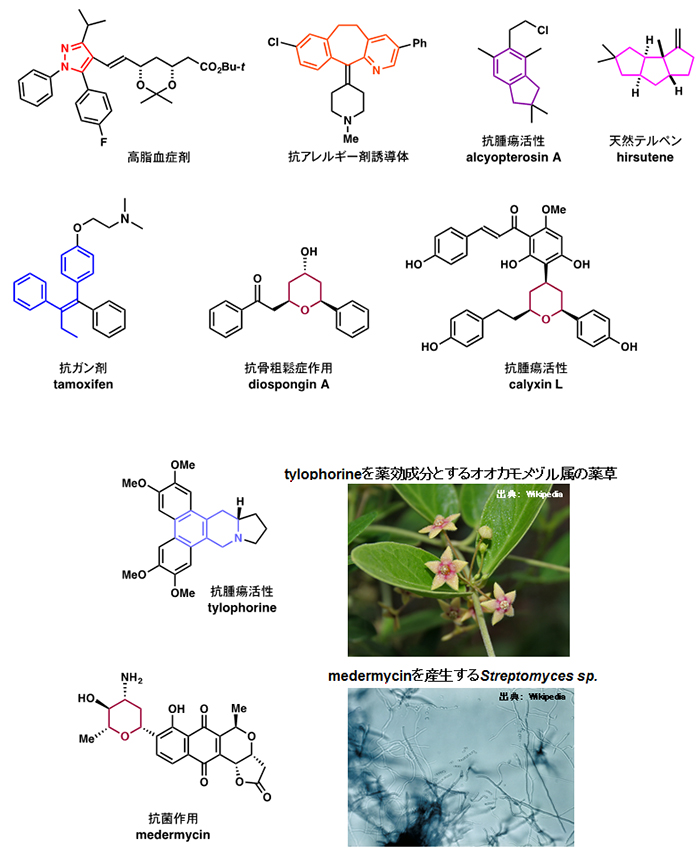
研究成果
代表論文
原書論文 / 占部弘和
- [1] M. Senoo, A. Furukawa, T. Hata, and H. Urabe, "Rh-catalyzed Intramolecular C-H Bond Activation with Triazoles. Preparation of Stereo-defined Pyrrolidines and Other Related Cyclic Compounds," Chem. Eur. J., 22, 890-895 (2016).
- [2] H. Murase, K. Senda, M. Senoo, T. Hata, and H. Urabe, "Rhodium-catalyzed Intramolecular Hydroarylation of 1-Halo-1-alkynes. Regioselective Synthesis of Semihydrogenated Aromatic Heterocycles," Chem. Eur. J., 20, 317-322 (2014).
- [3] M. Yamagishi, K. Nishigai, A. Ishii, T. Hata, and H. Urabe, "Facile Preparation of Indoles and 1,2-Benzothiazine 1,1-Dioxides via Nucleophilic Addition of Sulfonamides to Bromoacetylenes Followed by Pd-Catalyzed Cyclization," Angew. Chem. Int. Ed., 51, 6471-6474 (2012).
- [4] N. Hirone, H. Sanjiki, R. Tanaka, T. Hata, and H. Urabe, "Acceleration of the Substitution of Silanes with Grignard Reagents by Using either LiCl or YCl3/MeLi," Angew. Chem. Int. Ed., 49, 7762-7764 (2010).
- [5] D. Shikanai, H. Murase, T. Hata, and H. Urabe, "Rh-catalyzed Isomerization and Intramolecular Redox Reaction of Alkynyl Ethers Affording Dihydropyrans and Ketoolefins," J. Am. Chem. Soc., 131, 3166-3167 (2009).
- [6] S. Okada,† K. Arayama,† R. Murayama, T. Ishizuka, K. Hara, N. Hirone, T. Hata, and H. Urabe, "Iron-Catalyst-Switched Selective Conjugate Addition of Grignard Reagents. α,β,γ,δ-Unsaturated Amides as Versatile Templates for Asymmetric Three-Component Coupling Process," Angew. Chem. Int. Ed., 47, 6860-6864 (2008). † Equal contribution
- [7] R. Tanaka, H. Sanjiki, and H. Urabe, "Yttrium-Mediated Conversion of Vinyl Grignard Reagent to a 1,2-Dimetalated Ethane and Its Synthetic Application," J. Am. Chem. Soc., 130, 2904-2905 (2008).
- [8] Y. Fukudome, H. Naito, T. Hata, and H. Urabe, "Copper-Catalyzed 1,2-Double Amination of 1-Halo-1-alkynes. Concise Synthesis of Protected Tetrahydropyrazines and Related Heterocyclic Compounds," J. Am. Chem. Soc., 130, 1820-1821 (2008).
- [9] Y. Nobe, K. Arayama, and H. Urabe, "Air-Assisted Addition of Grignard Reagents to Olefins. A Simple Protocol for Three-Component Coupling Process Yielding Alcohols," J. Am. Chem. Soc., 127, 18006-18007 (2005).
- [10] R. Tanaka, A. Yuza, Y. Watai, D. Suzuki, Y. Takayama, F. Sato, and H. Urabe, "One-Pot Synthesis of Metalated Pyridines from Two Acetylenes, a Nitrile, and a Titanium(II) Alkoxide," J. Am. Chem. Soc., 127, 7774-7780 (2005).
原著論文 / 秦猛志
- [1] T. Hata, H. Gotoh, T. Yokomizo, and H. Urabe, "Iron-catalyzed 1,6-Selective Addition of Aryl Grignard Reagent to tert-Butyl (Z)-5-Phenyl-3-hexenoate," Org. Synth., 91, 307-321 (2014).
- [2] T. Hata, T. Nakada, O. Y. Taek, N. Hirone, and H. Urabe, "Iron-Catalyzed Regio- and Stereoselective Conjugate Addition of Aryl Grignard Reagents to α,β,γ,δ-Unsaturated Sulfones and Its Synthetic Application," Adv. Synth. Catal., 355, 1736-1740 (2013).
- [3] T. Hata, H. Imade, and H. Urabe, "Four Nucleophilic Additions to Alkenynedioic Acid Derivatives in Tandem; Efficient One-pot Synthesis of Bicyclo[4.2.0]octenols," Org. Lett., 14, 2450-2453 (2012).
- [4] T. Hata, S. Iwata, S. Seto, and H. Urabe, "Iron-Catalyzed Synthesis of Allenes from 2-Alken-4-ynoates and Grignard Reagents" Adv. Synth. Catal. 354, 1885-1889 (2012).
- [5] T. Hata, S. Sujaku, N. Hirone, K. Nakano, J. Imoto, H. Imade, and H. Urabe, "Iron-Mediated and -Catalyzed Metallative Cyclization of Electron Withdrawing Group-substituted Alkynes and Alkenes with Grignard Reagents," Chem.-Eur. J., 17, 14593-14602 (2011).
総説など
占部弘和
- [1] 占部、秦、"第4章 芳香族化合物 ? 医薬品化学への展開"、生命理工系のための大学院基礎講座 ? 有機化学、湯浅英哉・編、東京工業大学出版会・工学図書、pp. 67-90 (2011).
- [2] H. Urabe and F. Sato, "Titanocene (Cp2Ti(II)" in Encyclopedia of Reagents for Organic Synthesis, 2nd ed.; L. A. Paquette, D. Crich, P. L. Fuchs, G. A. Molander, Eds., Wiley: Chichester, Vol. 12, pp. 9590-9595 (2009).
- [3] 占部、"メタラサイクルをテンプレートとする多成分連結反応の開発"、化学工業、57, 757-762 (2006).
- [4] H. Urabe, "New Synthetic Reactions Mediated by Organometallic Compounds" in My Favorite Organic Synthesis, 有機合成化学協会・竜田邦明・福山透編、化学同人、pp. 244-245 (2002).
- [5] F. Sato, H. Urabe, and S. Okamoto, "Synthesis of Organotitanium Complexes from Alkenes and Alkynes, and Their Synthetic Application," Chem. Rev., 100, 2835-2886 (2000).
教員紹介
占部弘和 教授 理学博士
| 1980年 | 東京工業大学 理学部化学科 卒業 |
|---|---|
| 1985年 | 同大学院理工学研究科 化学専攻 博士課程 修了 |
| 1985 - 1990年 | 同理学部 助手 |
| 1988 - 1990年 | スタンフォード大学 化学科博士 研究員 |
| 1990 - 2000年 | 東京工業大学 生命理工学部 助手 |
| 2000 - 2004年 | 同大学院生命理工学研究科 生命情報専攻 助教授 |
| 2004年より | 現職 |
| 1998年 | 有機合成化学奨励賞 |
|---|---|
| 1999年 | 三共研究企画賞 |
- 教育活動
-
学部:有機化学第三、有機化学第四、医薬品化学、他
大学院:生物活性分子設計(英語)、他
- 研究活動
-
有機化学の研究は「新しい方法論の開発」と「それらに基づく有用化合物の合成・創出」を車の両輪としている。
当グループでは、この2分野のバランスをとりながら研究を推進している。
有機化合物の分子を思い通りに合成する新しい手法の開発は、それまで研究対象としたくても入手不可能と考えられてきた有機化合物を実際に手に取ることを可能にし、新しい発想に基づく応用利用を可能にしてきた。
同時に、東工大での生命理工の研究では、自然にある物質や現象を分析し解釈するだけにとどまらず、それらを人工的・他律的に応用利用することがとりわけ重要となる。
バイオ研究の対象は云うまでもなく有機化合物であり、したがって有機分子を必要に応じて改変しあるいは作り上げることが、この領域のさらなる発展に寄与する。
この観点から、上述した新しい方法論により、実際に天然の生物活性化合物あるいは人工の医薬等の新たな合成を行っている。
- 所属学会
- 日本化学会、アメリカ化学会、有機合成化学協会、近畿化学協会
秦猛志 准教授 工学博士
| 1995年 | 東京工業大学 生命理工学部生体分子工学科 卒業 |
|---|---|
| 1997年 | 東京工業大学 大学院総合理工学研究科 修士課程修了 |
| 2000年 | 京都大学 大学院工学研究科 博士後期課程 修了 |
| 1998 - 2000年 | 日本学術振興会 特別研究員(DC1) |
| 2000 - 2005年 | 三菱ウェルファーマ株式会社 創薬研究所 研究員 |
| 2005 - 2013年 | 東京工業大学 大学院生命理工学研究科 助手(2007年より助教) |
| 2013年より | 現職 |
| 2014 - 2018年 | 科学技術振興機構さきがけ研究者を兼任 「分子技術と新機能創出」領域 |
| 2009年 | 味の素研究企画賞 |
|---|---|
| 2012年 | 日産化学工業研究企画賞 |
| 2012年 | 東工大挑戦的研究賞 |
| 2012年 | 有機合成化学奨励賞 |
| 2019年 | 東工大教育賞優秀賞 |
| 2021年 | 工学教育賞 |
- 教育活動
学部:有機化学第二、有機化学第四、医薬品化学、他
大学院:生物活性分子設計(英語)、他
- 研究活動
-
我々のグループでは、有機分子を自由自在に合成・変換する合成手法の開発を行い、それらを利用して天然の有機化合物や人工の医薬などの生理活性化合物を合成しております。
特に最近では鉄触媒の利用、C-H結合活性化など、持続可能社会に必須な「効率性」、「安全性」および「経済性」を重視した未来型反応開発を展開し、次世代の「ものづくり」に貢献するべく研究を推進しています。
- 所属学会
- 日本化学会、有機合成化学協会、近畿化学会
教員からのメッセージ
- 占部教授より
-
皆さんが小さい頃から大学学部まで取り組んできた勉強は、すでに分かっていること(=やればうまくいくこと)を問題として、それに対する解答を作ることで成り立ってきた。したがって、皆さんは自力でほとんど解答出来たと思うし、もし残念ながら解答にたどり着けない場合には、模範解答を見ればそれで理解出来た。ところが、研究室に所属して始める研究は、もはや上述のようなやればうまくいくことを問題とはせず、所詮うまくいかないことばかりが問題となり、模範解答は当然無い。それでも少しづつ手探りで前進して、自分独自の何らかの答え(応え)を見つけていくことになる。研究室所属の前後で、いままでやってきた勉強とこれから始める研究の違いについて、このような頭の切り替えが早く出来ると、いよいよ研究にやみつきになると思います。
- 秦准教授より
-
有機合成化学は、有機分子を精密に組み立て、医薬等の我々の生活に役立つ分子を生み出す学問であります。しかし、実際に研究を行なっていると、分子を上手く組み立てることができずに失敗することが多々ありますが、時には我々の想像を超える「非常識」な現象が起こり、分子変換のブレークスルーが生み出されます。それを目の前のベンチで見つけた時の喜び、興奮は何事にも変えられません。ものづくりに果敢に挑戦したい人や「非常識」な現象を見つけてみたい人は、是非一度ラボを覗いて見て下さい。
お問い合わせ先
教授 占部弘和
すずかけ台キャンパス B2棟 1131号室
E-mail : hurabe@bio.titech.ac.jp
准教授 秦猛志
すずかけ台キャンパス B2棟 1127号室
E-mail : thata@bio.titech.ac.jp
※この内容は掲載日時点の情報です。最新の研究内容については研究室サイト![]() をご覧ください。
をご覧ください。
※ 2025年5月1日:一部最新の情報に更新しました。