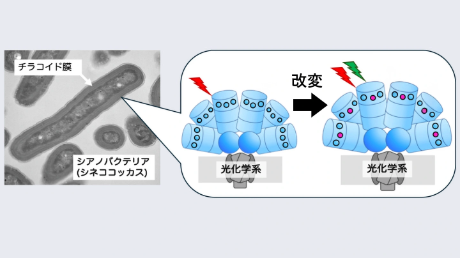
生命理工学系 News
ニトロアレーンとグリニャール反応剤から多官能ビアリールを一段階合成
ベンジジン型[5,5]-転位を制御する新合成戦略
ポイント
- ニトロアレーンとアリールグリニャール反応剤を低温下(-45℃)で反応させることで、遷移金属触媒や多段階の前処理を必要とせず、多官能ビアリールを一段階かつ高位置選択的に合成する新手法を開発。
- 基質設計により、従来は副経路であったベンジジン型[5,5]-シグマトロピー転位を主経路へと転換することに成功。
- 遷移金属触媒を用いない持続可能な芳香族C–C結合形成法を提示し、医薬品や機能性材料分子の効率的合成への応用が期待。
概要
東京科学大学(Science Tokyo)生命理工学院 生命理工学系の秦猛志准教授(生命理工学コース 主担当)、湯浅英哉教授(生命理工学コース 主担当)、金森功吏助教(生命理工学コース 主担当)、古田忠臣助教(生命理工学コース 主担当)、昭和薬科大学の唐澤悟教授、松本祥汰助教らの研究グループは、ニトロアレーンとアリールグリニャール反応剤[用語1]を反応させることで、多官能ビアリール[用語2]を高い位置選択性のもと一段階で合成できる新手法を開発しました。本反応は低温条件下(-45℃)で進行し、遷移金属触媒や多段階の前処理を必要としない点が特長です。
本研究では、従来は副反応としてわずかに進行するに過ぎなかったベンジジン型の[5,5]-シグマトロピー転位[用語3]に着目し、基質設計によってこれを主反応へと転換することに成功しました。具体的には、ニトロアレーンのオルト位およびメタ位に適切な置換基を配置することで、反応中間体の電子状態と立体環境を精密に制御し、従来優勢であった[3,3]-転位ではなく、目的の[5,5]-転位を選択的に進行させました。本手法は遷移金属触媒を必要とせず、低温に冷却した反応系に試薬を加えるという単純な操作で進行する点も大きな特長です。
さらに、トリフルオロメチル(CF3)基[用語4]を含む置換体を原料に用いると、[5,5]-転位後に分子内環化が進行し、医薬化学的に重要なベンゾイミダゾール[用語5]骨格が高選択的に得られることが明らかとなりました。本成果は、古典的な転位反応を再設計し、反応経路そのものを制御可能とした新しい合成戦略を提示するものです。
本成果は、2026年2月15日(現地時間)に「Chemistry – A European Journal 」に掲載されました。
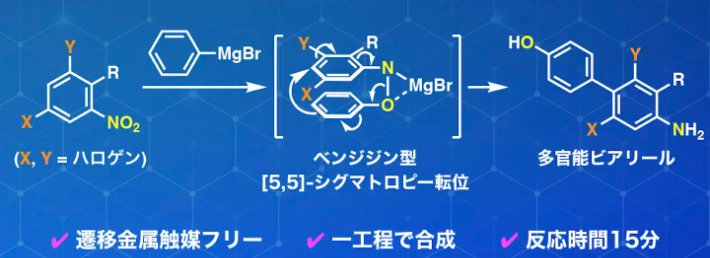
図1. ニトロアレーンとアリールグリニャール反応剤から多官能ビアリールおよびベンゾイミダゾールの一段階で構築するベンジジン型[5,5]-転位反応の概略
背景
ビアリール骨格は、医薬品や機能性材料、π共役分子などに広く含まれる重要な構造単位です。とりわけ、多数の官能基を持つビアリールは、生理活性や光・電子特性を精密に調整できることから、創薬や有機電子材料分野において中核的な役割を担っています。そのため、効率的かつ柔軟にビアリールを構築できる合成手法の開発は、有機合成化学における重要課題の一つとなっています。
これまでビアリールは、パラジウム触媒を用いる鈴木–宮浦カップリング反応[用語6]などの遷移金属触媒反応によって主に合成されてきました。しかし、これらの手法では貴金属触媒に依存するほか、ハロゲン化基質や有機ホウ素反応剤の事前調製が必要であり、合成工程が増えるという課題がありました。そのため、より簡便で持続可能な炭素–炭素結合形成法の開発が求められていました。
本研究では、ビアリール骨格の生成経路としてベンジジン転位[用語7]に着目しました。ベンジジン転位は19世紀から知られる古典的な反応ですが、位置選択性や基質適用範囲の制御が難しく、現代的な有機合成への応用は限定的でした[参考文献1]。今回の研究対象としたニトロアレーンとアリールグリニャール反応剤の反応においても[参考文献2]、ベンジジン型[5,5]-転位は副経路としてわずかに観測されるに過ぎませんでした。この[5,5]-転位を主経路として制御できれば、従来とは異なる新しい芳香族C–C結合形成戦略につながる可能性がありました。
研究成果
本研究では、ニトロアレーンの基質設計によってベンジジン型[5,5]-シグマトロピー転位を主経路として制御することに成功しました。この反応設計により、ニトロアレーンとアリールグリニャール反応剤から多官能ビアリールを高い位置選択性のもと一段階で構築できる新しい合成戦略を確立しました。
具体的には、アリールグリニャール反応剤と反応させる基質として、オルト位に置換基R、メタ位に電子求引性ハロゲン基X・Yを導入したニトロアレーンを設計しました。この分子設計により、反応中間体の電子状態と立体環境を精密に制御し、従来は副経路としてわずかに進行するに過ぎなかったベンジジン型[5,5]-転位を、主経路へと選択的に転換できることを見いだしました(図2)。
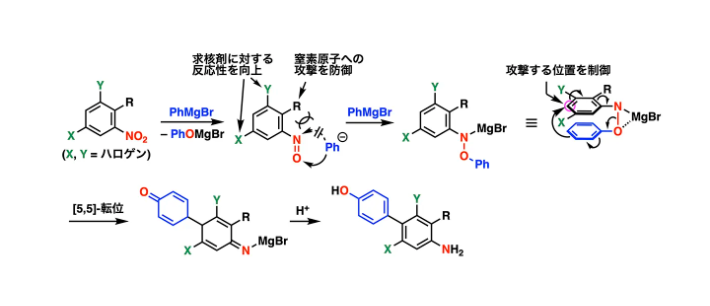
図2. 基質設計によりベンジジン型[5,5]-転位を主経路として制御する反応概念
本反応は遷移金属触媒を必要とせず、-45℃の低温条件下でニトロアレーンとアリールグリニャール反応剤を反応させることで進行します。ハロゲン基、アミノ基、ヒドロキシ基など多様な官能基を保持した多官能ビアリールを高い位置選択性で合成でき、実用的なスケールにおいても再現性よく反応が進行することを確認しました(図3)。
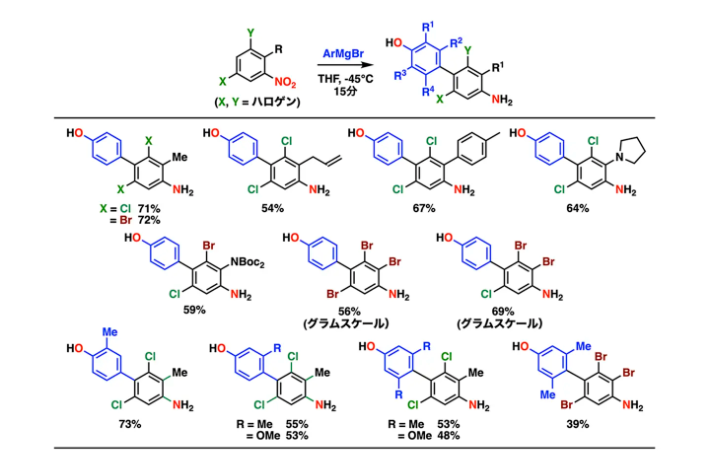
図3. 本手法で得られる多官能ビアリールの例
さらに、CF3CONH基を置換したニトロアレーンを原料に用いた場合には、-78℃の低温条件下で[5,5]-転位後に分子内環化が進行し、医薬品候補分子に広く見られるCF3置換ベンゾイミダゾール骨格を高選択的に合成できることを明らかにしました(図4)。
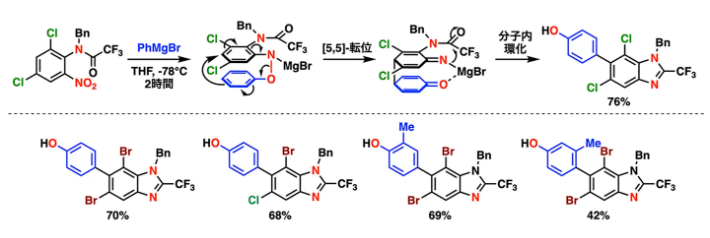
図4. CF3置換ベンゾイミダゾールの反応経路と生成例
加えて、DFT計算(Gaussian 16)により、電子求引性基の導入が[5,5]-転位経路をエネルギー的に安定化させることが理論的に支持されました(図5)。実験結果と理論解析を組み合わせることで、本反応が基質設計によって反応経路を制御できる“mechanistically tunable(機構設計可能)”な合成戦略であることを実証しました。
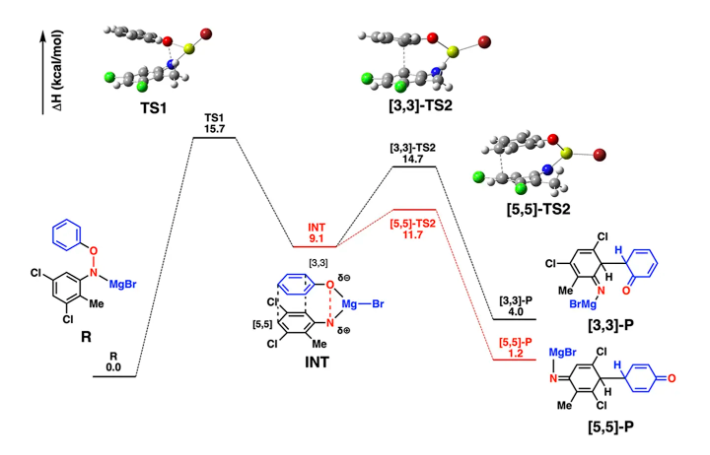
図5. [5,5]-転位と[3,3]-転位の反応経路を比較したDFT計算結果。
THF中における[5,5]-または[3,3]-転位生成物の形成に関する計算された自由エネルギープロファイル(M06-2X / 6-31G(d,p)、LanL2DZ(Cl, Mg, Br))[相対自由エネルギー(ΔHsolv, kcal/mol)を示している]。主要な結合距離(Å)を示した(C原子:灰色、H原子:白色、O原子:赤色;N原子:青色;Mg原子:黄色;Br原子:紫色;Cl原子:黄緑色)。
社会的インパクト
- ・
-
持続可能な分子合成への貢献
貴金属触媒を用いず、マグネシウムを用いる条件で進行する本手法は、資源制約や環境負荷の低減に貢献する持続可能なC–C結合形成法を提供します。
- ・
-
創薬・材料開発の加速
多官能ビアリールやCF3含有複素環を一段階で構築できるため、医薬品候補分子や機能性材料の分子設計と合成の迅速化が期待されます。
- ・
-
古典反応の新たな価値の提示
副反応と考えられていた反応経路を主反応として活用する設計思想は、既存反応の再解釈による新しい合成概念の創出につながります。
今後の展開
今後は、基質適用範囲をさらに拡張し、生理活性分子や機能性材料分子への実用的応用を進めます。また、転位反応と分子内環化を組み合わせた連続反応設計を発展させ、複数の結合再編成を一工程で実現する効率的な合成戦略へと展開します。さらに、理論計算と実験を融合した反応機構解析を深化させることで、新たな転位経路の制御や他の芳香族系への応用可能性を探究します。こうした研究を通じて、本研究で示した“反応経路を設計で制御する”という概念を発展させ、持続可能な芳香族C–C結合形成法の体系化を目指します。
- 付記
本研究は以下の支援を受けて実施されました。
- ・
- 日本学術振興会 科研費(23K04733、20K05507、17K05855、26410112、23750102)
- ・
- 東京科学大学 DLabチャレンジ研究助成
- ・
- 科学技術振興機構(JST)戦略的創造研究推進事業 さきがけ(PRESTO:分子技術、JPMJPR14KC)
- ・
- 科学技術振興機構(JST)戦略的創造研究推進事業 CREST(海洋カーボン、JPMJCR23J2)
- 参考文献
[参考文献1] A. W. Hofmann, Proc. R. Soc. Lond. 1863, 12, 576–578.
[参考文献2] H. Gao, D. H. Ess, M. Yousufuddin, L. Kürti, J. Am. Chem. Soc. 2013, 135, 7086–7089.
- 用語説明
[用語1] グリニャール反応剤:マグネシウム金属とハロゲン化アルキル、アルケニル、アリールを反応させて得られる有機マグネシウム化合物。炭素–炭素結合形成に広く用いられる高反応性の有機金属試薬である。
[用語2] ビアリール:2つの芳香環(アリール基)が単結合で直接結合した構造を持つ有機化合物群。医薬品や機能性材料の基本骨格として重要である。
[用語3] シグマトロピー転位:π電子系を含む分子内で、単結合(σ結合)の切断と新しいσ結合の形成が同時に起こる転位反応の一種。結合の再編成が協奏的に進行する。
[用語4] トリフルオロメチル(CF3)基:メチル基(–CH3)の3つの水素原子がフッ素原子に置き換わった官能基。強い電子求引性と高い脂溶性を示し、医薬品や農薬に導入されることで代謝安定性や生理活性の向上に寄与する。
[用語5] ベンゾイミダゾール:ベンゼン環とイミダゾール環が一辺を共有して縮合した複素環化合物。多くの医薬品や生理活性物質に含まれる重要骨格である。
[用語6] 鈴木–宮浦カップリング反応:パラジウム触媒存在下で、有機ホウ素化合物とハロゲン化アリールを反応させ、炭素–炭素結合を形成するクロスカップリング反応。ビアリール合成法として広く利用され、2010年のノーベル化学賞の対象となった。
[用語7] ベンジジン転位:1,2-ジフェニルヒドラジンが酸性条件下で転位し、4,4’-ジアミノビフェニル(ベンジジン)を与える反応。窒素–窒素結合の切断と炭素–炭素結合の生成を伴う転位反応であり、類似機構で進行する反応をベンジジン型転位と総称する。
- 論文情報
| 掲載誌: | Chemistry – A European Journal |
|---|---|
| タイトル: | Magnesium-Promoted Benzidine-Type Rearrangement for Regioselective Construction of Polyfunctionalized Biaryls |
| 著者: | Shumpei Saito, Manato Ishida, Yuki Busujima, Miki Ebihara, Kodai Kohama, Naomi Tanaka, Eitaro Toya, Minami Nakamura, Takashi Kanamori, Tadaomi Furuta, Shota Matsumoto, Satoru Karasawa, Hideya Yuasa, and Takeshi Hata* |
| DOI: |
10.1002/chem.202503607 |
研究者プロフィール
秦 猛志 Takeshi Hata
東京科学大学 生命理工学院 生命理工学系 准教授
研究分野:有機合成化学、有機金属化学