生命理工学系 News
疾患関連タンパク質PLZFの選択的分解が可能に
白血病などの治療につながる発見
概要
東京医科大学ケミカルバイオロジー講座の清水誠之客員研究員(大分大学医学部)、伊藤拓水准教授、半田宏特任教授らは、東京工業大学生命理工学院の山口雄輝教授、山本淳一助教(共に生命理工学コース主担当)とともに、疾患関連タンパク質PLZFの選択的分解を引き起こす低分子化合物を同定しました。
PLZF遺伝子は、急性前骨髄球性白血病(APL)やT細胞急性リンパ性白血病(T-ALL)に特有の染色体転座領域に存在する遺伝子の1つで、染色体転座によりPLZFの働きが変化することで白血病が引き起こされます。
本研究グループは、多発性骨髄腫の治療薬として使われている低分子化合物ポマリドミドがPLZFタンパク質の分解を誘導し、白血病モデル細胞株の増殖を阻害することを見出しました。
既存薬の新しい薬効を探索し、別の疾患の薬としての転用を目指すドラッグ・リポジショニングは近年、新薬開発の時間やコストを削減する手段として注目されています。今回の発見は、既存薬のポマリドミドが、PLZFが発症に関わる白血病などの治療に適用可能であることを示唆するものです。
本研究成果は11月11日、オープンアクセスの学術誌Communications Biologyにオンライン掲載されました。
背景
PLZF遺伝子は、APLやT-ALLの染色体転座領域に存在しています。PLZF遺伝子は別の遺伝子RARAやABL1と染色体転座によって融合し、その結果生じるキメラタンパク質PLZF-RARAがAPLを、PLZF-ABL1がT-ALLを、それぞれ引き起こすと考えられています(図1)。なお、APLはPML-RARAという別のキメラタンパク質によっても引き起こされますが、PML-RARA型のAPLが標準治療で用いられる全トランス型レチノイン酸によく反応するのに対し、PLZF-RARA型のAPLは全トランス型レチノイン酸に治療抵抗性を示し、有効な治療法がいまだ存在していません。
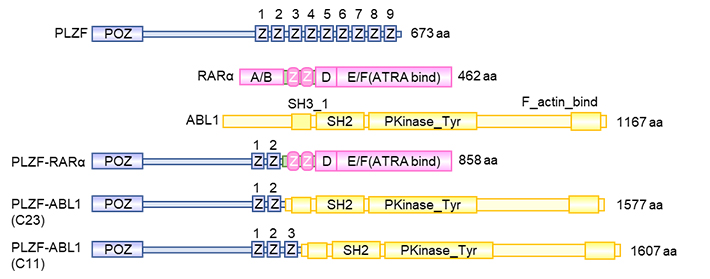
図1.PLZFおよびその融合タンパク質の構造。
本研究の出発点はサリドマイドにあります。サリドマイドは1950年代に鎮静剤として開発された低分子医薬品ですが、胎児に対して深刻な催奇形性を有することが判明し、市場から撤退しました。しかしサリドマイドの基礎研究はその後も続けられ、ハンセン病や多発性骨髄腫に対して優れた治療効果を有することが判明したため、2000年頃、世界各国で再び認可されました。現在では、サリドマイド骨格を有する後継薬であるレナリドミドやポマリドミドが臨床の現場で主に使われています。
これらサリドマイド系医薬品の作用機序は長らく不明でした。しかし2010年、本研究グループはサリドマイドの細胞内標的タンパク質としてセレブロン(CRBN)を同定し、作用機序の解明が一挙に進みました。CRBNは、ユビキチンリガーゼという選択的タンパク質分解に関わる複合体の基質認識サブユニットして機能しています。サリドマイドなどの化合物がCRBNに結合すると、ユビキチンリガーゼの基質特異性が変化し、もともとは基質でないタンパク質(ネオ基質)がユビキチン化され、分解されます。そしてこのことが、サリドマイド系医薬品の薬効の基盤となっていることが分かってきました。たとえば、レナリドミドとポマリドミドは、多発性骨髄腫の増殖に必須なタンパク質IKZF1ならびにIKZF3の分解を引き起こすことで、多発性骨髄腫に対する治療効果を発揮します。
CRBNを標的とすることで、任意の疾患関連タンパク質を細胞内から除去できる可能性があり、CRBNを標的とした創薬は一般性の高いアプローチとして現在、非常に注目されています。
研究成果
本研究グループは、サリドマイド系医薬品のドラッグリポジショニングを目指して、CRBNの新規ネオ基質を探索しました。そしてプロテオミクスや分子生物学的な解析により、PLZFというタンパク質がCRBNの新規ネオ基質の1つであり、ポマリドミドの存在下で分解されることを突き止めました。さらに、酵素-基質認識の分子基盤を詳しく明らかにしました。
前述のように、APLやT-ALLといった白血病患者のがん細胞で見つかるキメラタンパク質PLZF-RARAやPLZF-ABL1は「がんドライバー」として働くと考えられます。そこで、これらのキメラタンパク質を発現する白血病モデル細胞株を樹立し、ポマリドミドの効果を調べました。その結果、ポマリドミドは臨床的に妥当な濃度(0.1µM)でキメラタンパク質の分解を誘導し、白血病モデル細胞株の増殖阻害を引き起こしました(図2)。以上の結果から、ポマリドミドがPLZFならびにPLZF融合タンパク質の分解を引き起こし、PLZFが発症に関わる白血病などに対して治療効果を発揮することが示唆されました。
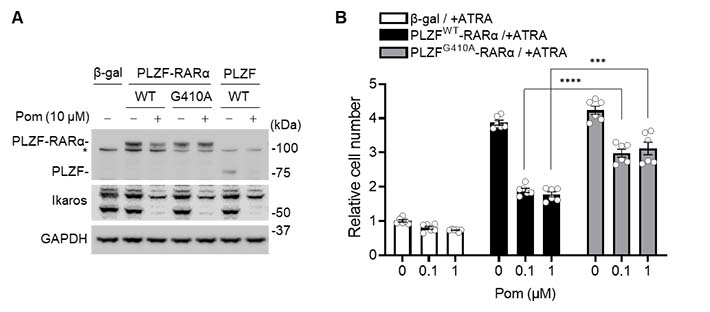
図2.ポマリドミドのPLZF-RARA発現細胞株への影響。
今後の展開
今回の発見は、既存薬のポマリドミドが、PLZFが発症に関わる白血病などの治療に適用可能であることを示唆するものです。しかし、本研究成果は細胞株を用いて得られたものなので、今後、実験動物を用いた前臨床試験やヒトを対象とした臨床試験により、ポマリドミドの白血病などに対する有効性を検証していく必要があります。
- 論文情報
| 掲載誌: | Communications Biology |
|---|---|
| 論文タイトル: | PLZF and its fusion proteins are pomalidomide-dependent CRBN neosubstrates |
| 著者: | Nobuyuki Shimizu, Tomoko Asatsuma-Okumura, Junichi Yamamoto, Yuki Yamaguchi, Hiroshi Handa, and Takumi Ito |
| DOI: |
- 免疫調節薬ポマリドミドの新規作用機序の解明|生命理工学系News
- 研究者という生き方|研究者への第一歩|大学院で学びたい方
- 山口研究室
- 研究者詳細情報(STAR Search) - 山口 雄輝 Yuki Yamaguchi
- 研究者詳細情報(STAR Search) - 山本 淳一 Junichi Yamamoto
- 研究室スポットライト「生命のしくみを徹底的に明らかにし、応用展開を目指す」山口雄輝研究室(YouTube)
- 生命理工学院 生命理工学系
- 研究成果一覧