生命理工学系 News
タンパク質共変動ネットワークが拓くがん治療の新戦略
薬剤作用の多面性を捉え、併用療法の標的を体系的に探索
ポイント
- 鉄依存性細胞死を誘導する化合物AX-53802の作用メカニズム解明と、がん細胞死を促進する併用薬の抽出に成功
- 薬剤により引き起こされるタンパク質の「量・質・局在」の変化を共変動ネットワークとして可視化する「PLOM-CON解析法」を応用
- 薬剤の多面的な作用を捉えることで、併用薬ターゲットの体系的な探索が可能となり、創薬の加速に貢献
概要
東京科学大学 総合研究院 細胞制御工学研究センターの加納ふみ教授(生命理工学コース 主担当)らの研究グループは、がん治療の新戦略として注目される鉄依存性細胞死(フェロトーシス)[用語1]を誘導する新規化合物AX-53802の作用メカニズムをPLOM-CON解析法(Protein Localization and Modification-based Covariation Network)[用語2]により解明するとともに、がん細胞死を促進する併用療法の可能性を提案しました。
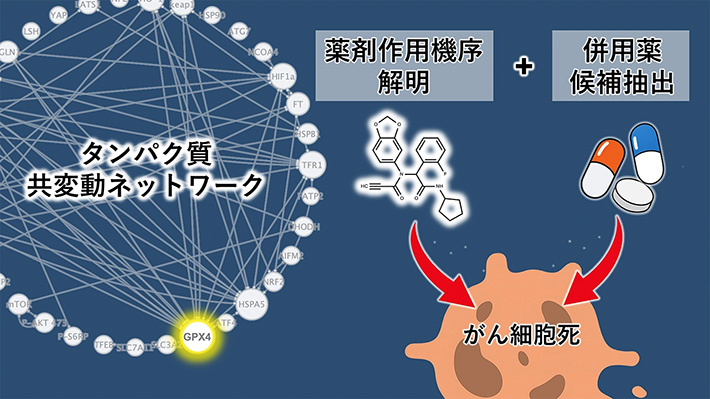
本研究では、薬剤により引き起こされるタンパク質の「量・質・局在」の変化を蛍光抗体染色法[用語3]により捉え、その時間的同調性に基づいて共変動ネットワーク[用語4]として可視化しました。薬剤添加有無の2条件におけるネットワークを比較した際に最も大きな変化を見せたタンパク質であるGPX4がAX-53802の直接の標的分子であることが、検証実験により明らかになりました。また、併用薬ターゲットの体系的な探索を行ったところ、GPX4阻害とFAK経路の阻害剤を組み合わせることでがん細胞死が促進されることを発見しました。今後、PLOM-CON解析法が薬剤の作用メカニズムの解明のみならず、併用療法の開発にも広く応用されることにより、さまざまな薬剤の効力増強や副作用軽減にも役立てられることが期待できます。
本研究成果は、東京科学大学 総合研究院 細胞制御工学研究センターの加納ふみ教授、村田昌之特任教授、國重莉奈特任助教と、東京大学の野口誉之学術専門職員、セルシュートセラピューティクス株式会社の岡本直美研究員と李蕾研究員、Axcelead Drug Discovery Partners株式会社の尾野晃人研究員との共同研究によって行われ、3月31日付の「Communications Biology」に掲載されました。
背景
創薬においては、薬剤による思わぬ毒性や薬効の欠如が大きな問題となります。このことは、薬剤の直接の標的分子だけに注目するのではなく、薬理作用に影響しうるその他の分子を包括的に捉えることの必要性を示しています。従来、薬剤の作用機序解明における主流のアプローチは、薬剤と標的分子との一対一の相互作用に注目するものであり、間接的な影響を及ぼす因子を考慮できないという課題がありました。そこで、薬剤により引き起こされる広範な細胞応答を一挙に捉えることができるネットワーク解析[用語5]を活用した手法が求められています(図1)。
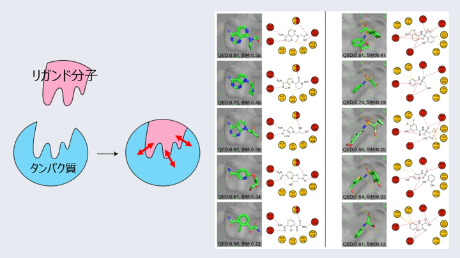
PLOM-CON解析法は、加納ふみ教授らの研究グループが2021年に開発したネットワーク解析法です(図2)。PLOM-CON解析法は、細胞に入力したシグナル(薬剤添加などを含む)に応答して引き起こされるタンパク質の「量・質・局在」の変化を蛍光抗体染色法により捉え、その時間的同調性に基づいて共変動ネットワークとして可視化する手法です。従来のネットワーク解析法の多くは、細胞を破壊して得られるタンパク質を情報源としており、遺伝子発現の「量」のみの可視化にとどまっていました。それに対して、細胞の蛍光抗体染色「画像」情報を基にタンパク質レベルのネットワークを描くPLOM-CON解析法の利点は、「質」情報、つまりタンパク質のリン酸化をはじめとする翻訳後修飾情報と、タンパク質の機能に関わる「局在」情報を反映することができる点にあります。
さまざまな条件下で描いたネットワークを比較することで、薬剤の有無による細胞状態の違いを一目で把握することができ、薬剤の作用機序解明への大きな手がかりが得られることが期待できます。また、ネットワークに現れる多面的な細胞応答には、薬剤により誘導される現象を“進める”作用と、現象の進行に“抗う”細胞応答の両方が含まれていると考えられます。それらの情報を活用することで、より望ましい薬剤の効果を得るための併用薬の探索にも役立てられることが期待できます。
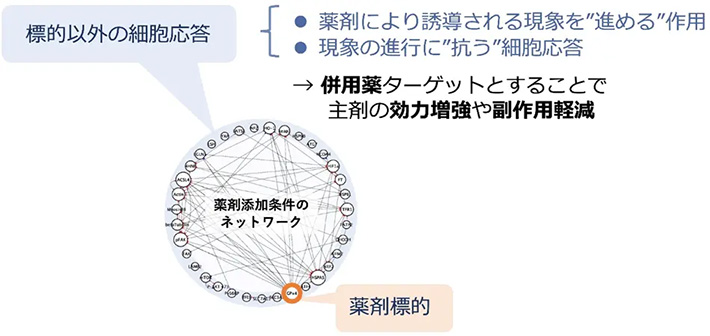
図1.
広範な細胞応答を一挙に捉えることができるネットワーク解析法
(Kunishige et al., Communications Biology, 2025より一部改変)
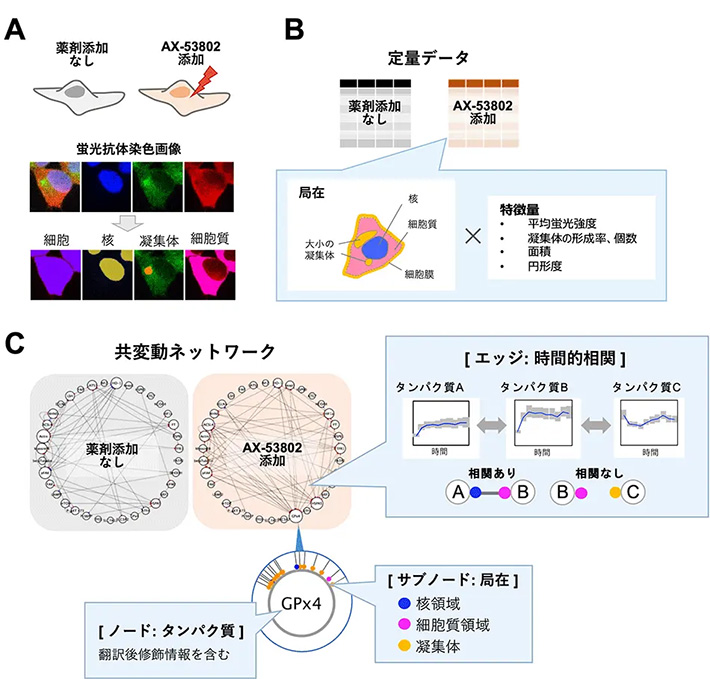
図2. PLOM-CON解析法の概要。(A)PLOM-CON解析法におけるサンプル作製と画像解析。本研究においては、フェロトーシス誘導剤AX-53802を添加した細胞を各時間点において固定し、35種の抗体を用いた蛍光抗体法により染色した。その後、画像解析により核や細胞質領域、凝集体領域を定めた。(B)タンパク質の「量・質・局在」情報を含む定量データ。画像解析により定められた各領域上のさまざまな特徴量が各タンパク質・時間点毎に得られる。(C)定量データを基に描かれた共変動ネットワーク。本研究で染色した35種のタンパク質をノードとして、時間的相関の有無がエッジとして表されている。局在情報はサブノードの色で表される。薬剤の有無のネットワークを比較することにより、大きな変化を示すタンパク質としてGPX4が特定された。(Kunishige et al., Communications Biology, 2025より一部改変)
研究成果
本研究ではPLOM-CON解析を活用した、薬剤スクリーニングにより得られた新規フェロトーシス誘導剤AX-53802の作用メカニズム解明を目指しました。はじめに、フェロトーシス関連タンパク質35種を蛍光抗体染色した細胞画像を基に描いたネットワークを比較することで、AX-53802の処理によって最も大きく変化するタンパク質としてGPX4が特定されました(図2)。GPX4はフェロトーシスの主要な抑制因子であり、GPX4の阻害は脂質過酸化を介した細胞死を引き起こすことが知られています。そこで、AX-53802添加がGPX4に与える影響をより詳細に調べたところ、薬剤添加直後(10分以内)にGPX4が細胞膜移行していることが分かりました。この細胞膜移行は、過酸化脂質の蓄積をFerrostatin-1により抑制した条件においても見られることから(図3A)、作用機序の上流に位置付けられる変化であることが分かりました。その後、試験管内でAX-53802をGPX4タンパク質に作用させた検証実験系においてGPX4の活性阻害が確認されたことから、GPX4がAX-53802の直接の標的であることが分かりました。
次に、ネットワークに表れたより細かな細胞状態の違いを定量的に検出するために、相関異常度[用語6]という指標を用い、AX-53802添加の有無の2条件におけるネットワークの違いにどのタンパク質特徴量が寄与しているかを算出しました。その結果、GPX4以外にもリン酸化FAK、アクチン繊維、トランスフェリン受容体(TfR1)[用語7]といったタンパク質特徴量の変化が抽出されました。特に、GPX4とTfR1において凝集体に関連する特徴量に変化が見られたことに着目し、検証実験を行ったところ、AX-53802添加30分後にGPX4とTfR1、F-アクチンが会合した凝集体を形成することが分かりました(図3B)。また、細胞内の鉄取り込みの動態が変化し、細胞内鉄濃度が減少する事象が観測されたことから、この凝集体形成はフェロトーシス誘導剤に対する細胞の防御機構が作動している可能性が示唆されました。以上のように、共変動ネットワークとその後の検証実験を通じ、AX-53802の作用メカニズムを多面的に明らかにすることができました。
次に、薬剤が引き起こす多面的な細胞応答を一挙に捉えるネットワーク解析法の利点を活かし、併用薬ターゲットの体系的な探索を行いました。相関異常度により抽出されたタンパク質に加え、公共のタンパク間相互作用データベースBioGridを用いてネットワーク拡張を行うことで、より網羅性の高い併用薬候補分子の探索を行ったところ(図4A)、最も有望な候補としてリン酸化FAK、アクチン繊維、MDM2、Ezrin、Cortactinといったタンパク質が抽出されました。そこで、これらの分子の活性を変化させる薬剤をAX-53802と共に添加する実験を行った結果、GPX4とFAK経路の同時阻害によりがん細胞死が促進されることが判明しました(図4B)。一方で、MDM2阻害やEzrin 阻害、Cortactin脱アセチル化、そしてアクチン繊維の分岐を阻害する薬剤によりフェロトーシスが抑制されることが分かりました。以上のことから、併用薬ターゲット候補をネットワーク解析により体系的に抽出する手法の有用性が示されました。
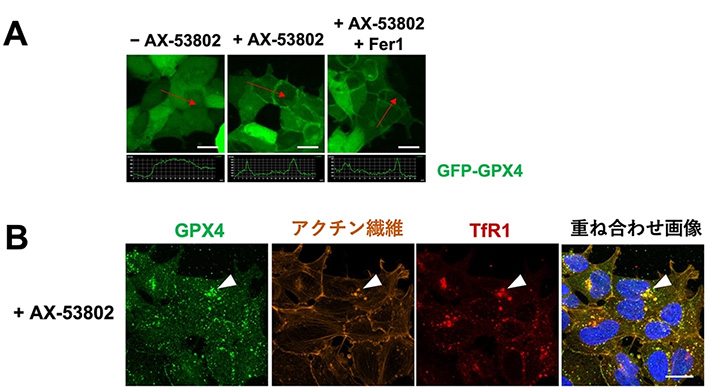
図3. 顕微鏡画像により捉えられたGPX4の変化。(A)フェロトーシス誘導剤AX-53802の添加により10分以内にGPX4の細胞膜移行が見られた。(B)AX-53802の添加30分後にGPX4とTfR1、F-アクチンが会合した凝集体の形成が見られた(白矢印)。(Kunishige et al., Communications Biology, 2025より一部改変)
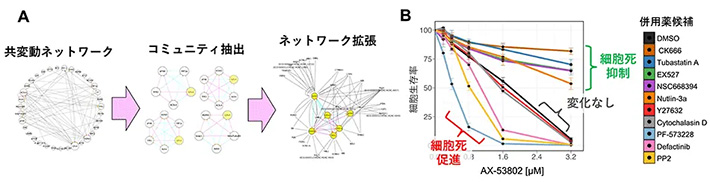
図4. 共変動ネットワークを用いた併用薬ターゲットの探索。(A)ネットワーク拡張による併用薬ターゲットの探索の概略。PLOM-CON解析により描いた共変動ネットワークを基に、お互いが密につながりあったコミュニティを抽出した。その後、公共データベースにおいて相互作用が報告されているタンパク質でネットワークの拡張を行い、併用薬ターゲットタンパク質を抽出した。(B)併用薬ターゲット候補の活性を変化させる薬剤を、AX-53802と共に細胞に添加した実験の結果、細胞死を抑制する薬剤と促進する薬剤をそれぞれ特定できた。FAK経路の阻害剤であるPF-573228 、Defactinib、PP2によりがん細胞死が促進されることが分かった。(Kunishige et al., Communications Biology, 2025より一部改変)
社会的インパクト
がん治療の新戦略としてフェロトーシス誘導剤が注目されていますが、標的タンパク質への特異性や薬効の欠如といった課題が残されています。現在、誘導剤自身の特異性向上や薬効向上に向けたさまざまなアプローチが提案されているなか、本研究では、共変動ネットワークというタンパク質ネットワークを基に薬剤の作用機序を調べることで、併用薬によるフェロトーシス薬剤の効力増強や副作用軽減を目指しました。本研究により有用性が示されたGPX4とFAK経路の同時阻害によるフェロトーシスの効率的誘導法はがん治療の新戦略として期待できます。また、近年フェロトーシスが神経変性疾患や虚血再灌流障害の進行に関係することが明らかになってきており、フェロトーシスから細胞を保護するための治療法の開発も求められています。この治療法を開発する上で、本研究で見つかったフェロトーシスを抑制するタンパク質群が重要な標的分子となることが期待されます。PLOM-CON解析法を用いた、共変動ネットワークを活用した薬剤の作用メカニズムの解明と併用薬ターゲット探索が今後さまざまな薬剤について行われることで、新しい創薬戦略の立案や創薬プロセスの加速化への貢献が期待できます。
今後の展開
創薬分野では、生体内により近いオルガノイドや神経系(ニューロンとグリア細胞)などの共培養系で、多種類の細胞間での薬剤の反応・応答を調べる必要性が増大しています。本研究で使用されたPLOM-CON解析法により得られる共変動ネットワークでは、解析対象のタンパク質同士の「時間的同調性」のみを指標にエッジが張られるため、隣接する細胞内にある「直接相互作用していないタンパク質間」の共変動を解析でき、異種細胞間でのコミュニケーションへの薬剤の影響を捉えることができます。また、細胞染色画像から機械学習やAIにより細胞種や病態進行別に細胞を識別して共変動ネットワークを描くこともできるため、特定の細胞種や病態段階にある細胞に特異的に作用する薬効の検出など、新薬開発や安全性に対する新しい戦略を提供できる可能性があります。このような創薬課題に対して、本研究で行った薬剤作用機序解明や併用薬ターゲット探索を駆使し、「画像」を基にした新しい創薬・細胞医薬を展開していきます。
- 付記
本研究は下記の支援により行われました。
・セルシュートセラピューティクス株式会社
・AMED-PRIME
研究領域:ソロタイプ「プロテオスタシスの理解と革新的医療の創出」研究開発領域
研究課題:シングルセル共変動ネットワーク解析による代謝関連タンパク質のプロテオスタシス変動制御機構の解明
- 用語説明
[用語1] 鉄依存性細胞死(フェロトーシス) : 細胞内の過酸化脂質の蓄積に特徴づけられる、鉄依存性のプログラム細胞死の一種。生体膜の過酸化脂質を還元することのできる酵素であるGPX4(グルタチオンペルオキシダーゼ4)が阻害されると、過酸化脂質が蓄積し、フェロトーシスが誘導される。
[用語2]
PLOM-CON(Protein Localization and Modification-based Covariation Network)解析法 :2021年に加納ふみ教授らの研究グループが開発したネットワーク解析法。細胞に入力したシグナルに応答して引き起こされるタンパク質の「量・質・局在」の変化を蛍光抗体染色法により捉え、その時間的同調性に基づいて共変動ネットワークとして可視化する手法。このネットワークには、タンパク質のリン酸化をはじめとする翻訳後修飾情報(「質」)と、タンパク質の機能に関わる「局在」情報が反映される。ネットワークにおいて、抗体により染色される各タンパク質はノード(節点)として、時間的相関の有無がエッジ(辺)として表され、局在情報はサブノード(ノードの周りの小円)の色で示される。
[参考1] 加納研究室ホームページ![]()
[参考2] Noguchi, Y. et al. Microscopic image-based covariation network analysis for actin scaffold-modified insulin signaling. iScience 24, 102724 (2021). DOI:10.1016/j.isci.2021.102724![]()
[用語3] 蛍光抗体法:蛍光色素で標識した抗体を用いて、特定の抗原(ターゲット分子)を検出・可視化することで、細胞や組織中のタンパク質の局在や発現量を調べることができる手法。この方法では、まず固定化・細胞膜の透過化を行った細胞に対して、目的のタンパク質に特異的に結合する一次抗体を加え、続いて一次抗体に結合する蛍光標識二次抗体を加えた後、蛍光顕微鏡を使用してタンパク質が可視化できる。
[用語4] 共変動ネットワーク:異なる要素間の共変動(時間的同調性)を表現することで、動的な関係性を効果的に捉えることができるネットワーク。
[用語5] ネットワーク解析:グラフ理論を基礎として物事をノード(節点)とエッジ(辺)からなるグラフとして抽象化する手法。多数の要素間の複雑な関係性の理解に有効であり、社会ネットワーク分析やWebページの検索システムなど、多様な分野や場面で活用されている。
[用語6] 相関異常度:変数間の関係の強弱を表す二つのネットワークにおいて、両者の相違に最も寄与する頂点を定量的に表す指標 (Idé, T. et al. Proceedings of the 2009 SIAM International Conference on Data Mining. 2009)。
[用語7] トランスフェリン受容体(TfR1):細胞の表面に存在するタンパク質で、鉄イオンの細胞内への取り込みを調節することで鉄のホメオスタシス(恒常性維持)を保つ重要な役割を担う。トランスフェリンと呼ばれる鉄を運ぶタンパク質が鉄イオンを結合した状態でTfR1に結びつくことで、その複合体が細胞内に取り込まれる。
- 論文情報
| 掲載誌: | Communications Biology |
|---|---|
| タイトル: | Protein covariation networks for elucidating ferroptosis inducer mechanisms and potential synergistic drug targets |
| 著者: | Rina Kunishige, Yoshiyuki Noguchi, Naomi Okamoto, Lei Li, Akito Ono, Masayuki Murata, and Fumi Kano |
| DOI: | 10.1038/s42003-025-07886-3 |
研究者プロフィール
加納 ふみ Fumi KANO
東京科学大学 総合研究院 細胞制御工学研究センター 教授
研究分野:細胞デザイン、細胞編集


國重 莉奈 Rina KUNISHIGE
東京科学大学 総合研究院 細胞制御工学研究センター 特任助教
研究分野:細胞画像解析、細胞生物学、生化学


関連リンク
- 加納 ふみ Fumi Kano|研究者検索システム Science Tokyo STAR Search
- 國重 莉奈 Rina Kunishige|研究者検索システム Science Tokyo STAR Search
- 村田 昌之 Masayuki Murata|研究者検索システム Science Tokyo STAR Search
- 加納ふみ研究室
- 細胞制御工学研究センター
- 生命理工学院 生命理工学系
- 総合研究院
お問い合わせ
東京科学大学 総合研究院 細胞制御工学研究センター
教授 加納 ふみ
Tel 045-924-5682
Fax 045-924-5682
E-mail kanou.f.f7f1@m.isct.ac.jp