融合理工学系 News
熱化学電池の蘊奥を開く
熱を電気に変える液体技術の予測設計に道
要点
- 「熱化学電池」は電解液につけた温度差と電極面での可逆反応から発電する技術
- 電圧や電流を決める根本因子やそれらの値の理由を説明する規範は未解明だった
- 前世紀に発達した溶液理論と量子化学計算とを組み合わせてこれらの疑問を解明
- 性能予測設計に道を開き、熱化学電池の社会実装に向けた開発を加速させる成果
概要
東京工業大学 科学技術創成研究院 ゼロカーボンエネルギー研究所の村上陽一教授(地球環境共創コース 主担当)と工学院 機械系の長勇毅大学院生(村上研究室所属)、日本化薬株式会社の研究チームは、熱エネルギーを電気に変える「熱化学電池」の性能を決める因子群の根底的な性質を明らかにし、その性能予測設計に道を開いた。
熱化学電池とは、水や有機溶媒に酸化還元対[用語1]を溶かした液体(電解液)に温度差をつけ、温度が異なる2電極における可逆反応から電力を生む熱電変換技術であり、近年研究が活発化している。これまでの熱化学電池研究は、主に電解液や電極などの材料面での開発と改善に注力して行われてきた。
本成果は、熱化学電池の特性を決める因子群とそれらの間の関係を、量子化学計算と前世紀に開拓された溶液理論とを組み合わせて解明したもので、「その電圧や電流の値が得られるのはなぜか?」等の疑問に理解と説明規範を与え、社会に多量にある熱エネルギーから電気を生む液体技術の実装に向けた設計指針を与える基礎研究成果である。
本研究成果はPhysical Chemistry Chemical Physics(王立化学会、英国)の9月21日号に掲載![]() された。
された。
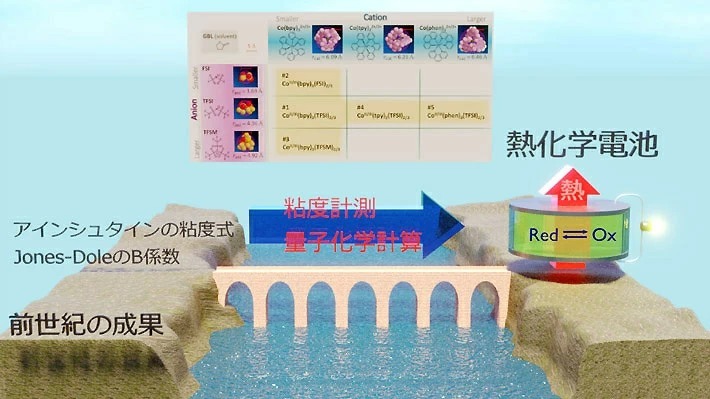
- 液体で「熱→電気」の変換を行う熱化学電池の領域と、前世紀に開拓された溶液理論との間にあった断絶をわたる橋を築き、前者に新しい洞察と設計指針をもたらした。
背景
日本の年間エネルギー消費(約12エクサ・ジュール、エクサは10の18乗)の約4分の3が非電力での消費であり(資源エネルギー庁 時系列表![]() 、2022年4月15日公表)、その大半は最終的に熱エネルギーとなり環境に放出され、散逸している。原理的に「温度差のもとで熱が流れている所では発電が可能」なため、このような大量の熱エネルギーを一部でも電力に変換すること(熱電変換)は重要な課題となっている。
、2022年4月15日公表)、その大半は最終的に熱エネルギーとなり環境に放出され、散逸している。原理的に「温度差のもとで熱が流れている所では発電が可能」なため、このような大量の熱エネルギーを一部でも電力に変換すること(熱電変換)は重要な課題となっている。
従来、熱電変換には固体素子(主に半導体)を用いるアプローチが検討されているが、世の中に多く存在する200 ℃以下の排熱・廃熱[用語2]には適用が難しい側面がある。また、熱電素子は通常剛体板のため、さまざまな表面形状をもつ熱源に適用しづらいという側面もある。そこで、形が自由に変形でき、それ自体が熱輸送の媒体となる「液体」を用いた熱電変換が近年急速に注目を集めている。これは「熱電気化学発電[注1]」と呼ばれ、図1に模式的に示す「熱化学電池[注2]」によって行われる。
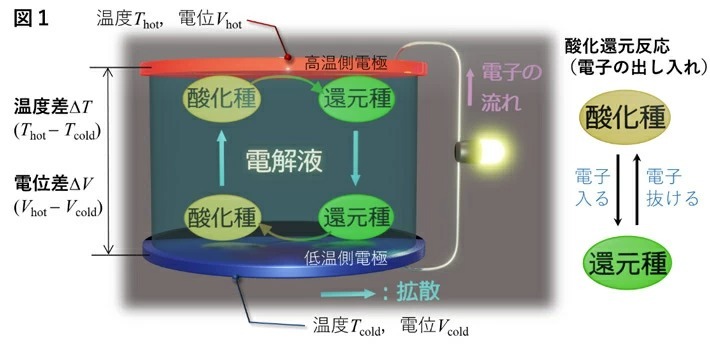
図1. 熱化学電池とその原理の模式図。
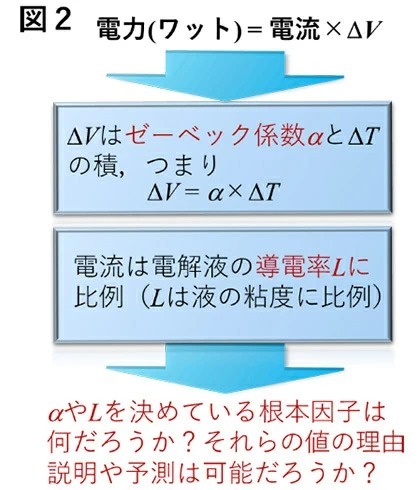
図2. 本研究の命題。
この技術は、酸化還元対(酸化種と還元種のペア)を溶媒に溶かした電解液を用いて行われる。熱化学電池には、容器に電解液を密閉し両端の電極間に温度差をつける図1の形態と、電解液を循環させて発熱面を冷却しつつ発電する形態[注3]とがあるが、以下では典型的な図1の形態を想定する。図1は、高温側電極(温度Thot、電位Vhot)で「酸化種→還元種」の反応(電極からの電子の受け入れ)が、低温側電極(温度Tcold、電位Vcold)ではその逆の反応が進行する場合を描いている。温度差(ΔT )に対して電位差(ΔV )が発生する理由は酸化還元平衡電位[用語3]に温度依存性があるためである。開回路状態でのΔV とΔT との比例定数を「ゼーベック係数α[注4]」と呼ぶ。
発電量はΔV ×I に等しい(I : 電流)。したがって発電量の増大には「ゼーベック係数α」と「電解液の導電率L」の値を決めている根本因子を解明・理解し、これらの値に対する説明規範と予測性を確立する必要がある(図2)。近年の熱化学電池研究の進展は「材料面での革新と性能向上」を起こしたが、上記の点はほとんど未確立であった。そのため、本技術の発展と社会実装に向けてはこれらの点の解明と確立が必要となっていた。
研究成果
村上教授らの研究グループは、前世紀に溶液化学分野で蓄積されてきた知見の幾つかが、熱化学電池研究が抱える上記問題の解決に有用であることに気付いた。前世紀に構築された「過去の財産」と「最近の熱化学電池の発展」とはこれまで相互によく関連づけられていなかったが、本成果は、以下のように両者間に初めて明示的な橋渡しを行い、性能支配因子について根本的な理解と洞察を構築し、その性能予測設計への道を拓いた。
以前から理解が確立している点として、「ゼーベック係数αは、酸化還元反応に伴うエントロピーの変化に比例する」という点がある。エントロピー(記号:S )は「複雑さ」を表す量(単位はJ/K;Jはジュール、Kはケルビン)で、図3のように理解できる。
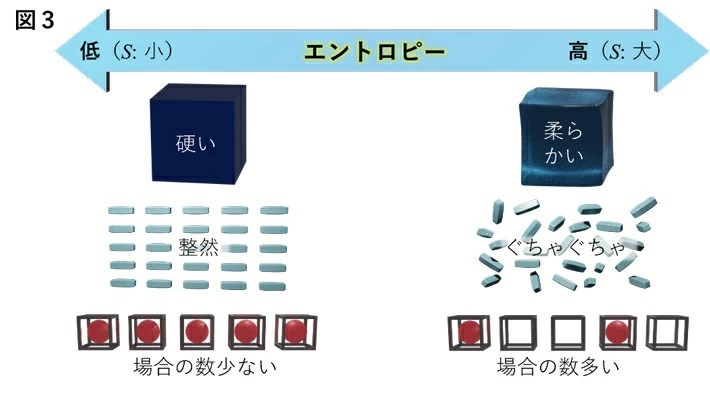
図3. エントロピーの概念を表す模式図。
αは、酸化還元反応(図1右)に伴う「内圏エントロピーの変化分」(図4の「内側」)と「外圏エントロピーの変化分」(図4の「外側」)の和をファラデー定数(図中参照)で割った値に等しい。図4の下部に挙げた命題はこれまでほとんど研究されてこなかった。本研究チームは、前世紀に研究され、知見と知識が蓄積されていたJones-DoleのB 係数[用語4]とアインシュタインの粘度式[用語5]の本問題への適用を着想し、それらを考察と解析の起点に選んだ。そして、酸化種・還元種の量子化学計算(内圏エントロピーの評価)と電解液の粘度計測(外圏エントロピーの評価)とを組み合わせることにより、図4下部の命題に対する洞察と説明の規範を築くことに成功した。さらに、量子化学計算による酸化還元種の適切なイオン半径の算出法を考案し、これとネルンスト-アインシュタインの式[用語6]とを組み合わせることで、電流値の予測を行う方法論を示した。
具体的に、図5に要約したように、本成果の知見には (i) αに対する内圏エントロピーと外圏エントロピーの寄与割合はおよそ1:1であり、溶媒が同じであれば「αの大小」は「内圏エントロピー変化分の大小」をよく反映すること(すなわち、量子化学計算から同系統の他の酸化還元対のαを予測可能になったこと(意義1))、(ii) 電解液の粘度に対する説明規範を得たこと(意義2)、および、(iii) 創案したイオン半径算出法により電解質の導電率(すなわち、得られる電流値)が予測可能になったこと(意義3)が含まれる。
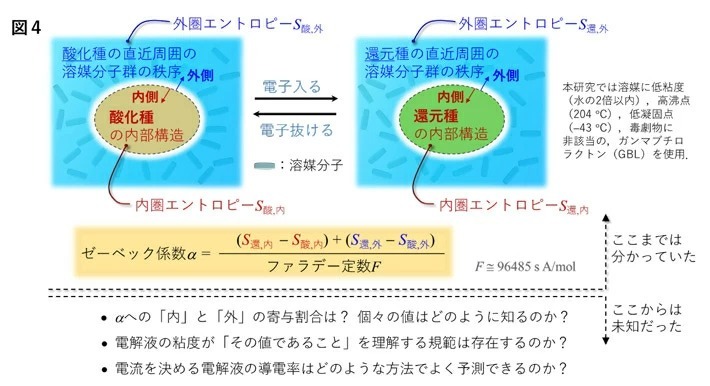
図4. これまで分かっていたこと(原理)と未知だったこと(命題)。
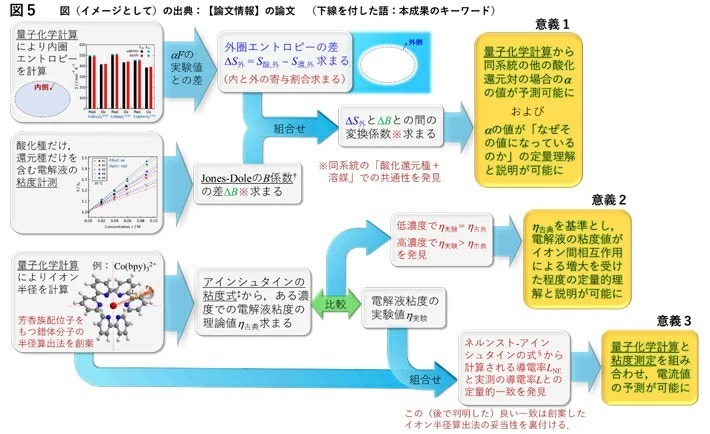
図5. 本研究の成果と意義。"†"、"‡"、"§"を付した語はそれぞれ用語4、5、および6参照。
社会的インパクト
熱化学電池(熱電気化学発電)は、現在社会の広い場面において未利用な大量の熱エネルギーの一部を電力に変換する有用性をもつ。高性能な熱化学電池を、その酸化還元対の最適選択も含めて創製しようとするとき、以前には明確な性能予測指針や測定結果に対する説明規範は存在していなかった。本研究の成果はこれらの諸課題を解決したものであり、今は黎明期にある熱化学電池の社会実装に向け、今後企業等においても指針や規範を伴う研究開発が遂行できる基礎を築いた。
今後の展開
本研究で獲得した知見から、同系統内の酸化還元対についてであれば、新たに検討する酸化還元種の性能は、実際にその合成や購入をしなくとも、ゼーベック係数や電流値に関する性能予想が可能となった。この利点を生かし、今後、さらなる協力パートナーを募りつつ、より大電力を発生可能な酸化還元対の探索と開発を進めてゆく。
- 用語説明
[用語1] 酸化還元対 : 同種の粒(原子、分子)だが電荷が1つだけ違うペア。例えば "X+とX"、"Y3+とY2+"、"Z-とZ2-"など(太字が酸化種)。酸化還元対は世の中で広く用いられており、例えばリチウムイオン電池は"Li+とLi"のペアを用いている。
[用語2]
排熱・廃熱 : 「排熱」はシステム内の熱源から出てくる(出てきてしまう)熱、「廃熱」はシステム外に捨てられた状態にある熱。工学において両者の区別は非常に重要となる。この論点の詳細は、電気評論 2018年12月号の解説記事![]() 参照。
参照。
[用語3] 酸化還元平衡電位 : 電極面において「酸化種→還元種」の反応レートと、その逆の「還元種→酸化種」の反応レートとが等しくなる電極の電位。
[用語4] Jones-DoleのB 係数 : イオン溶液の粘度と濃度の関係をプロットしたときの、濃度の2乗の項の係数。イオンと溶媒との相互作用の程度を表すと考えられている。
[用語5] アインシュタインの粘度式 : 剛体微粒子(コロイドや糖分子などの球と近似できる微粒子)の懸濁液について、その液の粘度を、その粒子が液中で占める体積分率で表す理論式。アインシュタインが流体力学を用いて導出した式で、粒子間の相互作用は考慮されていない。本研究では、液の溶質が(この理論の枠組みでは想定されていない)イオン種であるにも関わらず、低濃度域ではこの理論とよく一致すること、そして、濃度の増大とともにこの理論からの逸脱が明確に見え、「粘度の値がなぜその値になっているのか」の説明規範を見出したことが新規点となっている。
[用語6] ネルンスト-アインシュタインの式 : 導電率を溶質イオンの半径と溶液粘度で表す、流体力学に基づく理論式。個々のイオンが独立に(すなわち、粒子間の相互作用やペアリングなどは無く)振る舞うことを仮定している。論文情報の論文の式13。
- 注釈
[注1] 英語ではThermoelectrochemical conversionまたはThermogalvanic conversion。
[注2] 英語ではThermoelectrochemical cell, Thermogalvanic cell, Thermocellなど。
[注3] 村上教授らが先駆けて創出してきた「フロー熱電発電」のこと。
本学のニュースリリース 世の中で広く用いられる強制対流冷却において「物体を冷やしながら発電する」新技術を創出![]() (2019年11月18日)および 発電ができる新世代冷却技術「レドックス・フロー熱電発電」の実用性を初めて証明
(2019年11月18日)および 発電ができる新世代冷却技術「レドックス・フロー熱電発電」の実用性を初めて証明![]() (2021年10月8日)参照。
(2021年10月8日)参照。
[注4] 本来、ゼーベック係数という語はゼーベック効果に基づく場合にのみ用いられるべきだが、酸化還元反応に基づく熱化学電池についても慣習的に用いられている。
- 論文情報
| 掲載誌 : | Physical Chemistry Chemical Physics(王立化学会、英国) |
|---|---|
| 論文タイトル : | Thermoelectrochemical Seebeck coefficient and viscosity of Co-complex electrolytes rationalized by the Einstein relation, Jones–Dole B coefficient, and quantum-chemical calculations |
| 著者 : | Yuki Cho, Shinya Nagatsuka, and Yoichi Murakami |
| DOI : | 10.1039/D2CP02985E |
- 世界最高性能の固体フォトン・アップコンバージョン材料を開発|東工大ニュース
- 発電ができる新世代冷却技術「レドックス・フロー熱電発電」の実用性を初めて証明|東工大ニュース
- 未利用な光エネルギーを利用可能な波長に変えるフォトン・アップコンバージョンの理論体系を構築|東工大ニュース
- 共有結合性有機骨格(COF)のサブミリメートル単結晶を開発|東工大ニュース
- 可視光を波長340 nm以下の紫外光に変換する溶液系を開発|東工大ニュース
- 世の中で広く用いられる強制対流冷却において「物体を冷やしながら発電する」新技術を創出|東工大ニュース
- 未利用光を利用可能な波長に変換する新しい材料プラットフォームを開発|東工大ニュース
- 未利用の太陽光エネルギーを利用可能にする透明・不燃な光波長変換ゲルを開発―太陽電池や光触媒等の変換効率向上に資する材料革新|東工大ニュース
- 村上陽一教授らがMaterials Horizons Outstanding Paper Runner-up Awardを受賞|融合理工学系News
- 村上陽一准教授が総務省「異能vation」ジェネレーションアワード部門 企業特別賞を受賞|東工大ニュース
- 村上研究室
- 村上研究室 -研究室紹介 #21-|融合理工学系News
- 村上陽一|研究者検索システム 東京工業大学STARサーチ
- ゼロカーボンエネルギー研究所
- 科学技術創成研究院(IIR)
- 地球環境共創コース(大学院課程)|教育|環境・社会理工学院 融合理工学系
- 原子核工学コース(大学院課程)|教育|環境・社会理工学院 融合理工学系
- 工学院 機械系
- 日本化薬株式会社
- 研究成果一覧