生命理工学系 News
ドーパミンD2受容体を介して 膵臓のβ細胞量が調節される
糖尿病治療のための再生医療実現化に重要な情報を得た
要点
- マウスから膵β細胞を取り出し、β細胞数を増やす化合物を探索
- ドーパミンD2受容体の阻害剤によりβ細胞の分裂促進や細胞死と脱分化の抑制が起こることを発見
- ドーパミンD2受容体はアデノシンA2a受容体との会合によりβ細胞量を制御する機構の一端を担っていることを解明
概要
東京工業大学生命理工学院の坂野大介助教と粂昭苑教授(生命理工学コース主担当)らは、血糖値を下げるホルモンであるインスリン[用語1]を産生する膵臓のβ細胞の量がドーパミン[用語2]を介する細胞間シグナルによって調節されていることを明らかにした。体内のβは糖尿病が進行すると減少していくことから、どんどん病態が悪化することが問題である。今回の発見が生体内でのβ細胞数を維持するための創薬研究や再生医療に役立つと期待される。
成果は6月30日、国際幹細胞学会(ISSCR)の 公式ジャーナルである「Stem Cell Reports」のオンライン版に掲載された(Dopamine D2 Receptor-Mediated Regulation of Pancreatic β Cell Mass: Stem Cell Reports![]() )。
)。
研究の背景
膵臓は、主にアミラーゼなどの消化酵素を十二指腸内へ分泌する外分泌細胞と内分泌細胞が集まった膵島から構成される。膵島にはα細胞、β細胞、δ細胞、ε細胞、PP細胞の5つの細胞が存在する。α細胞はグルカゴン、β細胞がインスリン、δ細胞がソマトスタチン、ε細胞がグレリン、PP細胞が膵ポリペプチドを分泌する。糖尿病の原因は、β細胞が破壊されることによるインスリン分泌量の低下と、インスリン受容体の応答性の低下、の2つに大きく分けられる。糖尿病が重篤になれば最終的に膵βの不足に陥る。糖尿病患者への膵島移植や膵臓移植は有効な治療であるが、ドナー不足が大きな問題である。その解決策として、新たな移植源として膵β細胞を試験管内で作る、いわゆる再生医学が考えられる。その材料としては主に2つがあげられる。1つめは多能性幹細胞であるembryonic stem cells(ES細胞)、あるいはinduced pluripotent stem cells(iPS細胞)から分化させる手法である。なかでもiPS細胞を用いる分化誘導研究は疾患特異的iPS細胞を利用した病態解明や創薬のための薬剤スクリーニングのほか、免疫拒絶を回避した再生医療への応用が期待されている。2つ目は、患者自身のβ細胞の自己複製を促進する薬剤を作ることである。そのために膵臓β細胞がどのように分化・増殖し、細胞量を保つのかを理解することが必要である。また、創薬によって体内のβ細胞量の低下を防ぐことは糖尿病の治療に役立つ(図1)。
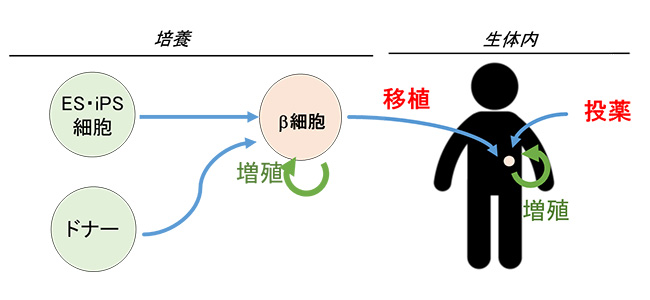
図1. さまざまなβ細胞源
移植するために試験管内でβ細胞を増やすこと、β細胞数維持の仕組みを理解して創薬を行うことで糖尿病治療の新しい治療に貢献する。
研究の経緯と成果
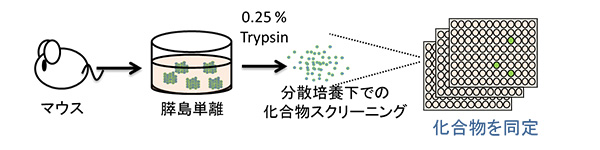
図2. 化合物スクリーニング
マウスの膵島を取り出し分散培養する過程で化合物を作用させた。3日後にインスリン産生細胞が増えるものを選抜し、ヒット候補を同定した。
私たちはまず、マウスから膵臓の膵島を取り出し、約1200の低分子化合物を1つずつ培地に添加してβ細胞数の細胞分裂を促進するものを探索した(図2)。
そして、ドーパミンD2受容体の阻害剤であるドンペリドン(DPD)[用語3]という化合物によってβ細胞特異的に細胞数が増えることを発見した。このβ細胞が増える要因としては、細胞自身の自己複製能を高めること、細胞死を抑制すること、あるいは脱分化を抑制することがわかっている。脱分化とは、一旦インスリンを産生・分泌できるように成熟化したβ細胞がインスリンの発現が低下したり、分泌能を失ったり"β細胞らしさ"をなくしてしまう状態である。最近、β細胞の脱分化が糖尿病の1つの成因として新たに唱えられている。また、膵島の細胞を試験管内で培養を続けることにより、経時的に脱分化が進むことが知られているが、これが糖尿病状態を反映しているものと考えられる。今回の研究により、DPDはβ細胞らしさをより長い期間保たせる作用があることが分かった(図3、図4)。
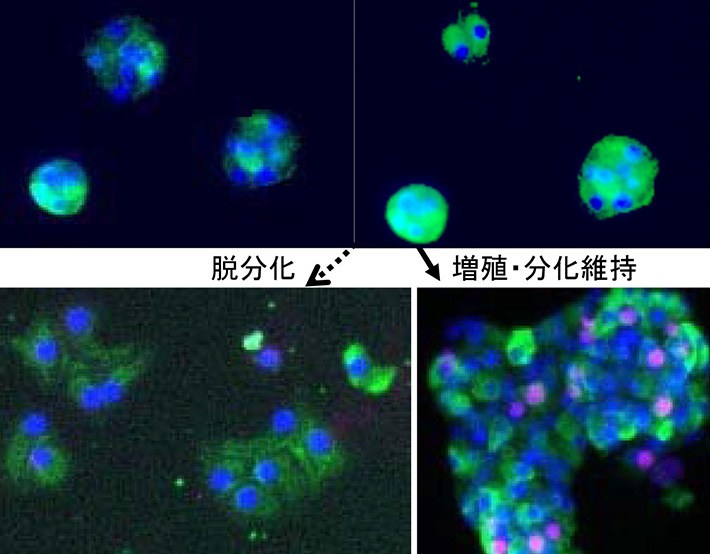
図3. ドーパミンは膵臓内分泌β細胞の増殖と分化を負に制御する
マウス体内から取り出された膵島をばらばらにして培養する際、DPD処理(あり:実線矢印)により、分化形質が維持された。DPD処理しない場合では、膵β細胞が脱分化した。緑;インスリン(膵β細胞マーカー)、赤;5-ethynyl-2'-deoxyuridine(EdU, 分裂している細胞の核を標識)、青;DAPI, 核。
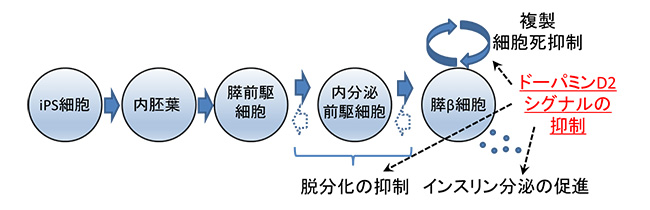
図4. ドーパミンシグナルの役割
DPDによって膵β細胞のドーパミンシグナルが抑制されると細胞分裂の促進、細胞死の抑制、細胞の脱分化抑制が起こる。
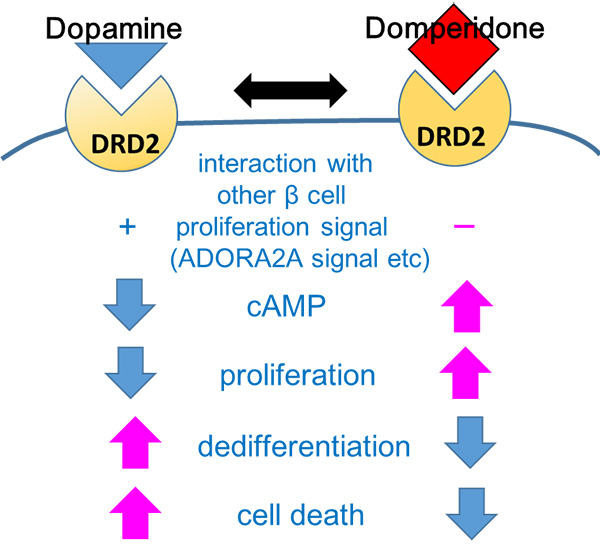
図5. DPDの作用
DPDがDRD2に作用することでアデノシンA2a受容体(ADORA2A)をはじめとするGPCRとの間で形成される"GPCR-DRD2複合体"の機能を調節していると考えられる。
これまでにも生体から取り出したβ細胞を試験管内で増やす目的でさまざまな研究が進んできた。たとえば、ゼブラフィッシュの稚魚の膵β細胞を薬剤により壊した後に、アデノシンA2a受容体(ADORA2A)を活性化させると膵β細胞数の回復が促進されることが報告されている。さらに、ヒトやマウスの膵島の細胞を培養する過程でも、アデノシンシグナルを活性化させると膵βの分裂が活性化されることが報告されている。興味深いことに、今回の私たちが発見したDRD2の阻害によるβ細胞数の増加はこれらの先行研究と関連している。すなわち、DRD2がADORA2Aと会合して、ヘテロ受容体の形成を介してアデノシンシグナルを阻害していることを明らかにした。私たちは今回、DPDはDRD2のADORA2Aに対する阻害を抑制することでアデノシンシグナルの機能を促進していることを明らかにした(図5)。
今後の展開
今回の研究の中で相互作用を明らかにした、DRD2とADORA2AはどちらもGタンパク質共役受容体(GPCR)である。マウス膵島においては少なくとも28種のGPCRが発現していることが知られている(Regard et al. 2007)。神経において、DRD2は「ハブ受容体」として注目されており、複数のGPCRとヘテロ二量体を形成し、細胞内シグナルを調節する役割を担っていると予想されている(Borroto-Escuela et al. 2014)。今回の研究によって、インスリン分泌をはじめとする膵島全体の機能調節において、GPCRが重要な役割を担っていると考えられ、それについて研究を進めていきたい。
用語説明
[用語1] インスリン : 膵臓のランゲルハンス島(膵島)のβ細胞から分泌されるペプチドホルモンの一種。脂肪の合成促進・分解抑制などにより血糖を抑制し、グリコーゲンや脂肪などの各種貯蔵物質の新生を促進することで血糖を低下させる。
[用語2] ドーパミン : おもに中枢神経系に存在する神経伝達物質の1つ。アミノ酸の一種であるチロシンからL-ドーパを介して生合成される。生体内で代謝されアドレナリン、ノルアドレナリンとなる。運動調節、ホルモン調節、快の感情、意欲、学習などに関わることが明らかにされている。セロトニン、ノルアドレナリン、アドレナリン、ヒスタミン、ドーパミンはモノアミンと総称される。またドーパミンは、ノルアドレナリン、アドレナリンはさらにカテコールアミンと呼ばれる。
[用語3] ドンペリドン : ドンペリドン(Domperidone、DPD)は、ドーパミン受容体拮抗薬の1つで、制吐薬、消化管機能改善薬として臨床で利用されている。商品名ナウゼリンとして協和発酵キリンなどが販売している。
論文情報
| 掲載誌 | Stem Cell Reports |
|---|---|
| 論文タイトル | Dopamine D2 receptor-mediated regulation of pancreatic β cell mass |
| 著者 | Daisuke Sakano, Choi Sungik, Masateru Kataoka, Nobuaki Shiraki, Motonari Uesugi, Kazuhiko Kume, and Shoen Kume |
| DOI | 10.1016/j.stemcr.2016.05.015 |
- 粂・白木研究室
- 研究者詳細情報(STAR Search) - 坂野 大介 Daisuke Sakano
- 研究者詳細情報(STAR Search) - 粂 昭苑 Shoen Kume
- Dopamine D2 Receptor-Mediated Regulation of Pancreatic β Cell Mass: Stem Cell Reports
お問い合わせ先
東京工業大学 生命理工学院 生命理工学系
教授 粂昭苑
E-mail : skume@bio.titech.ac.jp
Tel : 045-924-5812
Fax : 045-924-5813