生命理工学系 News
【研究室紹介】 西山・三浦研究室
高分子ナノテクノロジーを基盤とした革新的ナノ医薬品の開発
生命理工学系にはライフサイエンスとテクノロジーに関連した様々な研究室があり、基礎科学と工学分野の研究のみならず、医学や薬学、農学等、幅広い分野で最先端の研究が活発に展開されています。
研究室紹介シリーズでは、ひとつの研究室にスポットを当てて研究テーマや研究成果を紹介。今回は、高分子ナノテクノロジーを基盤として、がんをはじめとする難病の治療や疾患の前触れを検出するための高感度イメージング技術等の未来医療の実現に向けた革新的ナノ医薬品の開発を目指している、西山研究室です。

ライフエンジニアリングコース
教授 西山伸宏![]()
| キーワード | ナノ医薬品、DDS、ナノテクノロジー、機能性高分子 |
|---|---|
| Webサイト | 西山・三浦研究室 |
研究紹介
精密合成高分子をプラットフォームとしたナノメディシンの開発
ナノバイオテクノロジーの飛躍的な進歩により、タンパク質、ペプチド、核酸などの様々な生体機能性分子や環境・刺激応答材料・分子、イメージング分子などが開発され、それらの医療分野への応用が期待されています。しかしながら、これらの分子は、単独では、生体内で狙った機能・効果を得ることは困難であり、ときには副作用の発現が大きな問題となります。また、優れた機能・効果を得るために、複数の分子を化学的に結合する試みがなされていますが、多くの場合、それぞれの機能が損なわれ、十分な効果を発揮することができません。西山研究室では、リビング重合によって分子量、組成、官能基の位置を精密に制御した高分子材料をプラットフォームとして、上述の生体機能性分子や標的指向性機能や環境応答機能といった任意の機能を位置選択的に創り込むことによって、生体内で高度な機能を狙いどおりに発現させることができる理想的な薬剤(ナノメディシン)の開発を目指しています(図1)。
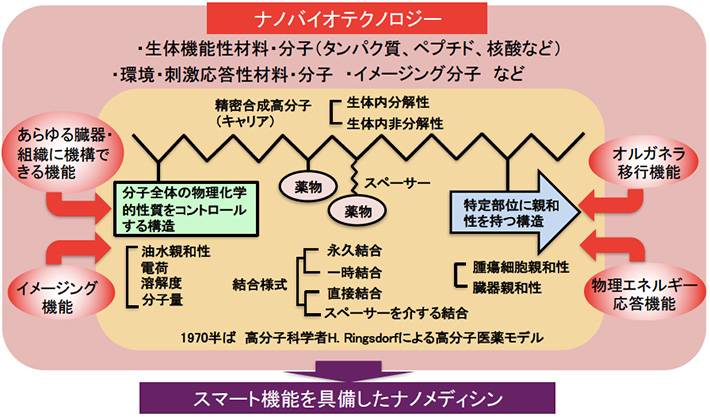
図1. 精密合成高分子をプラットフォームとするナノメディシンの創製
新規機能性ポリマーの開発から革新的診断・治療薬の実現へ
西山研究室では、従来には無い機能を有する新規ポリマーの開発し、疾患の診断・治療システムへの応用を展開しています。最近の成果としては、がん細胞で過剰発現するグルタミントランスポーターに多価相互作用を介して結合する新規ポリマーの開発に成功しました(Sci. Rep. 2017)(図2(A))。この他にもpHに応答して性質が変化するさまざまなポリマーの開発を行い、ナノメディシンへの応用を目指しています。また、これらのポリマーを標的細胞に選択的に作用させるための要素技術の開発も行っており、最近の成果としては、細胞質内のGlutathione / Glutathione S-transferase(GSH/GST)存在下で選択的に開裂するリンカー分子を新規に開発し、ポリマー-siRNAコンジュゲートの細胞内における機能発現効率を向上させることに成功しました(ChemMedChem. 2016) (図2(B))。診断・治療への応用に関しては、がん組織内の低pH環境に応答して信号強度が増大するナノ粒子型MRI造影剤の開発に成功しています(Nature Nanotech. 2016)。本システムを利用することによって、腫瘍内低酸素領域(Hypoxia)を選択的にイメージングし、さらに1.5 mmの微小がんを高感度に検出できることも明らかになっています(図2(C))。この他にも、抗がん剤や核酸医薬などの標的組織に選択的に作用させるナノメディシンの開発を行い、既に一部のシステムは臨床試験へと進んでいます。最近の成果としては、ホウ素クラスターをがん組織内に万遍なく送達できるポリマーコンジュゲートの開発を行い、ホウ素中性子捕捉治療(BNCT)による優れた治療効果が確認されています(J. Control. Release. 2016) (図2(D))。
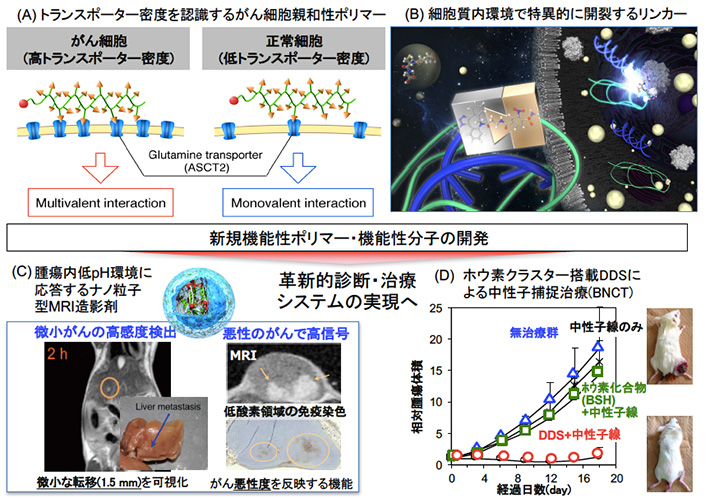
図2. 新規機能性ポリマーの開発から革新的診断・治療システムの実現へ
以上は最近の研究成果の一部ですが、西山研究室では、ポリマー合成から細胞・動物実験による機能検証までのすべてを行う環境を整えており、活発な共同研究によって新しい概念の診断・治療システムの開発を目指しています。研究成果は、論文として発表するだけに留まらず、医療機関・企業と連携して画期的な診断・治療薬として実用化し、医療の発展に貢献したいと考えています。
研究成果
国際誌 160編(Nature Nanotech, Nature Mater., Nature Commun., Science Transl. Med., PNAS, JACS, Angew Chem., Int. Ed.等)h-index: 55
最近の主な成果
- [1] N. Yamada, Y. Honda, H. Takemoto, T. Nomoto, Makoto M., K. Tomoda, M. Konno, H. Ishii, M. Mori, N. Nishiyama*, Engineering tumour cell-binding synthetic polymers with sensing dense transporters associated with aberrant glutamine metabolism. Sci. Rep., in press
- [2] H. Taniguchi, D. Hoshino, C. Moriya, H. Zembutsu, N. Nishiyama, H. Yamamoto, K. Kataoka, K. Imai, Silencing PRDM14 expression by an innovative RNAi therapy inhibits stemness, tumorigenicity, and metastasis of breast cancer. Oncotarget, in press
- [3] P. Mi*, H. Yanagie, N. Dewi, H.-C. Yen, X. Liu, M. Suzuki, Y. Sakurai, K. Ono, H. Takahashi, H. Cabral*, K. Kataoka*, N. Nishiyama*, Block copolymer-boron cluster conjugate for effective boron neutron capture therapy of solid tumors. J. Control. Release, 254 1-9 (2017)
- [4] C. H. Huang, H. Takemoto*, T. Nomoto, K. Tomoda, M. Matsui, N. Nishiyama*, Utility of the 2-nitrobenzenesulfonamide group as a chemical linker for enhanced extracellular stability and cytosolic cleavage in siRNA-conjugated polymer systems. ChemMedChem 12 (1) 19-22 (2017)
- [5] N. F. Che Harun, H. Takemoto*, T. Nomoto, K. Tomoda, M. Matsui, N. Nishiyama*, Artificial control of gene silencing activity based on siRNA conjugation with polymeric molecule having coil-globule transition behavior. Bioconjugate Chem. 27 (9) 1961-1964 (2016)
- [6] H. Hino, M. Kamiya, K. Kitano, K. Mizuno, S. Tanaka, N. Nishiyama, K. Kataoka, Y. Urano*, J. Nakajima*, Rapid cancer fluorescence imaging using a γ-glutamyltranspeptidase-specific probe for primary lung cancer. Transl Oncol. 9 (3) 203-210 (2017)
- [7] M. Iijima, D. Ulkoski, S. Sakuma, D. Matsukuma, N. Nishiyama, H. Otsuka, C. Scholz*, Synthesis of PEGylated poly(amino acid) pentablock copolymers and their self-assembly. Polymer International 65 (10) 1132-1141 (2016)
- [8] P. Mi, D. Kokuryo, H. Cabral, H. Wu, Y. Terada, T. Saga, I. Aoki*, N. Nishiyama*, K. Kataoka*, A pH-activatable nanoparticle with signal-amplification capabilities for non-invasive imaging of tumour malignancy. Nature Nanotech. 11 (8) 724-730 (2016)
- [9] H. Kinoh, Y. Miura, T. Chida, X. Liu, K. Mizuno, S. Fukushima, Y. Morodomi, N. Nishiyama, H. Cabral*, K. Kataoka*, Nanomedicines eradicating cancer stem-like cells in vivo by pH-triggered intracellular cooperative action of loaded drugs. ACS Nano 10 (6) 5643-5655 (2016)
- [10] Y. Matsumoto, Y. Miyamoto, H. Cabral, Y. Matsumoto, K. Nagasaka, S. Nakagawa*, D. Maeda, T. Yano, K. Oda, K. Kawana, N. Nishiyama, K. Kataoka*, T. Fujii, Enhanced efficacy against cervical carcinomas through polymeric micelles physically incorporating the proteasome inhibitor MG132. Cancer Sci. 107 (6) 773-781 (2016)
- [11] Y. Matsumoto, J. W. Nichols, K. Toh, T. Nomoto, H. Cabral, Y. Miura, R. J. Christie, N. Yamada, T. Ogura, M. R. Kano, Y. Matsumura, N. Nishiyama, T. Yamasoba, Y. -H. Bae*, K. Kataoka*, Vascular bursts enhance permeability of tumour blood vessels and improve nanoparticle delivery. Nature Nanotech. 11 (6) 533-538 (2016)
- [12] H. Nishida, Y. Matsumoto, K. Kawana*, R. J. Christie, M. Naito, B. -S. Kim, K. Toh, H. -S. Min, Y. Yi, Y. Matsumoto, H. -J. Kim, K. Miyata*, A. Taguchi, K. Tomio, A. Yamashita, T. Inoue, H. Nakamura, A. Fujimoto, M. Sato, M. Yoshida, K. Adachi, T. Arimoto, O. Wada-Hiraike, K. Oda, T. Nagamatsu, N. Nishiyama, K. Kataoka*, Y. Osuga, T. Fujii, Systemic delivery of siRNA by actively targeted polyion complex micelles for silencing the E6 and E7 human papillomavirus oncogenes. J. Control. Release 231 29-37 (2016)
- [13] M. Wang, Y. Miura, K. Tsuchihashi, K. Miyano, O. Nagano, M. Yoshikawa, A. Tanabe, J. Makino, Y. Mochida, N. Nishiyama, H. Saya, H. Cabral*, K. Kataoka*, Eradication of CD44-variant positive population in head and neck tumors through controlled intracellular navigation of cisplatin-loaded nanomedicines. J. Control. Release 230 26-33 (2016)
- [14] T. Nomoto, S. Fukushima, M. Kumagai, K. Miyazaki, A. Inoue, P. Mi, Y. Maeda, K. Toh, Y. Matsumoto, Y. Morimoto, A. Kishimura, N. Nishiyama*, K. Kataoka*, Calcium phosphate-based organic-inorganic hybrid nanocarriers with pH-responsive on/off switch for photodynamic therapy. Biomater. Sci. 4 (5) 826-838 (2016)
- [15] H. Uchida, K. Itaka, S. Uchida, T. Ishii, T. Suma, K. Miyata, M. Oba, N. Nishiyama, K. Kataoka*, Synthetic polyamines to regulate mRNA translation through the preservative binding of eukaryotic initiation factor 4E to the cap structure. J. Am. Chem. Soc. 138 (5) 1478-1481 (2016)
- [16] Y. Anraku, A. Kishimura*, M. Kamiya, S. Tanaka, T. Nomoto, K. Toh, Y. Matsumoto, S. Fukushima, D. Sueyoshi, M. R. Kano, Y. Urano, N. Nishiyama, K. Kataoka*, Systemically injectable enzyme-loaded polyion complex vesicles as in vivo nanoreactors functioning in tumors. Angew. Chem. Int. Ed. 128 (2) 570-575 (2016)
- [17] P. Mi, N. Dewi, H. Yanagie, D. Kokuryo, M. Suzuki, Y. Sakurai, Y. Li, I. Aoki, K. Ono, H. Takahashi, H. Cabral, N. Nishiyama*, K. Kataoka*, Hybrid calcium phosphate-polymeric micelles incorporating gadolinium chelates for imaging-guided gadolinium neutron capture tumor therapy. ACS Nano 9 (6) 5913-5921 (2015)
- [18] H. Cabral, J. Makino, Y. Matsumoto, P. Mi, H. Wu, T. Nomoto, K. Toh, N. Yamada, Y. Higuchi, S. Konishi, M. R. Kano, H. Nishihara, Y. Miura, N. Nishiyama, K. Kataoka*, Systemic targeting of lymph node metastasis through the blood vascular system by using size-controlled nanocarriers. ACS Nano 9 (5) 4957-4967 (2015)
- [19] H.-C. Yen, H. Cabral, P. Mi, K. Toh, Y. Matsumoto, X. Liu, H. Koori, A. Kim, K. Miyazaki, Y. Miura, N. Nishiyama, K. Kataoka*, Light-induced cytosolic activation of reduction-sensitive camptothecin-loaded polymeric micelles for spatiotemporally controlled in vivo chemotherapy. ACS Nano 8 (11) 11591-11602 (2014)
- [20] T. Nomoto, S. Fukushima, M. Kumagai, K. Machitani, Arnida, Y. Matsumoto, M. Oba, K. Miyata, K. Osada, N. Nishiyama*, K. Kataoka*, Three-layered polyplex micelle as a multifunctional nanocarrier platform for light-induced systemic gene transfer. Nature Commun. 5 3545 (2014)
- [21] H. Chen, L. Xiao, Y. Anraku, P. Mi, X. Liu, H. Cabral, A. Inoue, T. Nomoto, A. Kishimura*, N. Nishiyama*, K. Kataoka*, Polyion complex vesicles for photo-induced intracellular delivery of amphiphilic photosensitizer. J. Am. Chem. Soc. 136 (1) 157-163 (2014)
- [22] Y. Miura, T. Takenaka, K. Toh, S. Wu, H. Nishihara, M. R. Kano, Y. Ino, T. Nomoto, Y. Matsumoto, H. Koyama, H. Cabral, N. Nishiyama*, K. Kataoka*, Cyclic RGD-linked polymeric micelles for targeted delivery of platinum anticancer drugs to glioblastoma through the blood-brain tumor barrier. ACS Nano 7 (10) 8583-8592 (2013)
- [23] H. Cabral, M. Murakami, H. Hojo, Y. Terada, M. R. Kano, U. -I. Chung, N. Nishiyama*, K. Kataoka*, Targeted therapy of spontaneous murine pancreatic tumors by polymeric micelles prolongs survival and prevents peritoneal metastasis. Proc. Natl. Acad. Sci. USA. 110 (28) 11397-11402 (2013)
- [24] H. Takemoto, K. Miyata, S. Hattori, T. Ishii, T. Suma, S. Uchida, N. Nishiyama, K. Kataoka*, Acidic pH-responsive siRNA conjugate for reversible carrier stability and accelerated endosomal escape with reduced IFNα-associated immune response. Angew. Chem. Int. Ed. 52 (24) 6218-6221 (2013)
- [25] H. Cabral, Y. Matsumoto, K. Mizuno, Q. Chen, M. Murakami, M. Kimura, Y. Terada, M.R. Kano, K. Miyazono, M. Uesaka, N. Nishiyama*, K. Kataoka*, Accumulation of sub-100 nm polymeric micelles in poorly permeable tumours depends on size. Nature Nanotech. 6 (12) 815-823 (2011)
- [26] M. Murakami, H. Cabral, Y. Matsumoto, S. Wu, M. R. Kano, T. Yamori, N. Nishiyama*, K. Kataoka*, Improving drug potency and efficacy by nanocarrier-mediated subcellular targeting. Science Transl. Med. 3 (64) 64ra2 (2011)
教員紹介
西山伸宏 教授 博士(工学)
| 1996年 | 東京理科大学 基礎工学部 卒業 |
|---|---|
| 2001年 | 東京大学 大学院工学系 研究科 博士課程 修了(博士(工学)取得) |
| 2001年 | 米国ユタ大学 薬学部 ポストドクトラルフェロー |
|---|---|
| 2003年 | 東京大学 医学部附属病院 TE部 血管再生医療講座 助手 |
| 2004年 | 東京大学 大学院医学系研究科 疾患生命工学センター 臨床医工学部門 助手 |
| 2006年 | 同上 講師 |
| 2009年 | 同上 准教授 |
| 2013年 | 東京工業大学 資源化学研究所 高分子材料部門 教授 |
| 2016年 | 改租により現所属に名称変更 現在に至る |
| 2007年 | 高分子学会 高分子研究奨励賞 |
|---|---|
| 2009年 | 第一回日本DDS学会奨励賞(基礎) |
| 2012年 | 日本癌学会奨励賞 |
| 2016年 | 新製剤技術とエンジニアリング振興基金 第3回パーティクルデザイン賞 |
- 所属学会
- 高分子学会、日本DDS学会、日本バイオマテリアル学会、日本癌学会、日本分子イメージング学会
教員からのメッセージ
- 西山教授より
-
西山研究室では、それぞれの学生さんが異なるテーマを持って、ポリマー合成から細胞・動物実験による評価までのすべてを行うことをモットーとしています。特に専門知識等がなくても大丈夫ですので、興味があれば好奇心だけで飛び込んで来ていただければと思います。学生さんには幅広い知識と俯瞰的な物事の捉え方を身につけて頂き、将来、自分にしかできない何かを実現できるようになってほしいと思っています。留学生が多いことも当研究室の特徴です。就職先は、化学メーカー、製薬企業などです。

- 研究室と研究テーマ
- がんの悪性度を検知する「ナノマシン造影剤」を開発
- "切らない手術"を実現するナノマシンを開発―がんの日帰り治療の実現に向けて―
- がんへの光選択的遺伝子導入に成功 ―三層構造の高分子ミセル型ナノマシンで実現―
- 科学技術創成研究院 化学生命科学研究所
お問い合わせ先
教授 西山伸宏
すずかけ台キャンパス R1棟 812号室
E-mail : nishiyama.n.ad@m.titech.ac.jp
※この内容は掲載日時点の情報です。最新の研究内容については研究室サイト![]() をご覧ください。
をご覧ください。