生命理工学系 News
【研究室紹介】 三原・堤研究室
ペプチド工学と生命化学
生命理工学系にはライフサイエンスとテクノロジーに関連した様々な研究室があり、基礎科学と工学分野の研究のみならず、医学や薬学、農学等、幅広い分野で最先端の研究が活発に展開されています。
研究室紹介シリーズでは、ひとつの研究室にスポットを当てて研究テーマや研究成果を紹介。今回は、さまざまな機能をもったペプチドの開発に取り組む、三原・堤研究室です。
| キーワード | 生命化学、生物有機化学、ペプチド工学、生体高分子化学 |
|---|---|
| Webサイト | 三原研究室 |
研究紹介
ペプチド工学に基づいた機能性ペプチドの創製

研究室集合写真
私たちの研究室では、アミノ酸の並び方を工夫して、らせん状のα-ヘリックス構造やジグザグ構造のβ-シートなどの特徴的な構造をもち、さまざまな機能を発揮するペプチドを設計しています。これまでに、「水と混じることでゲルをつくって細胞が増殖・成長するのに適した環境をつくる自己組織化ペプチド(細胞足場材料)」、「がん細胞を見分けて細胞の中に入り薬物を運ぶ細胞膜透過性ペプチド(ドラッグデリバリー)」、「遺伝子工学の手法と有機化学の手法を組み合わせてつくる糖ペプチドライブラリを利用したレクチンタンパク質結合リガンドの探索とレクチン検出プローブ」といったさまざまな機能をもったペプチドの開発に取り組んでいます。
1. 自己組織化ペプチドの創製とナノ・バイオマテリアルへの応用
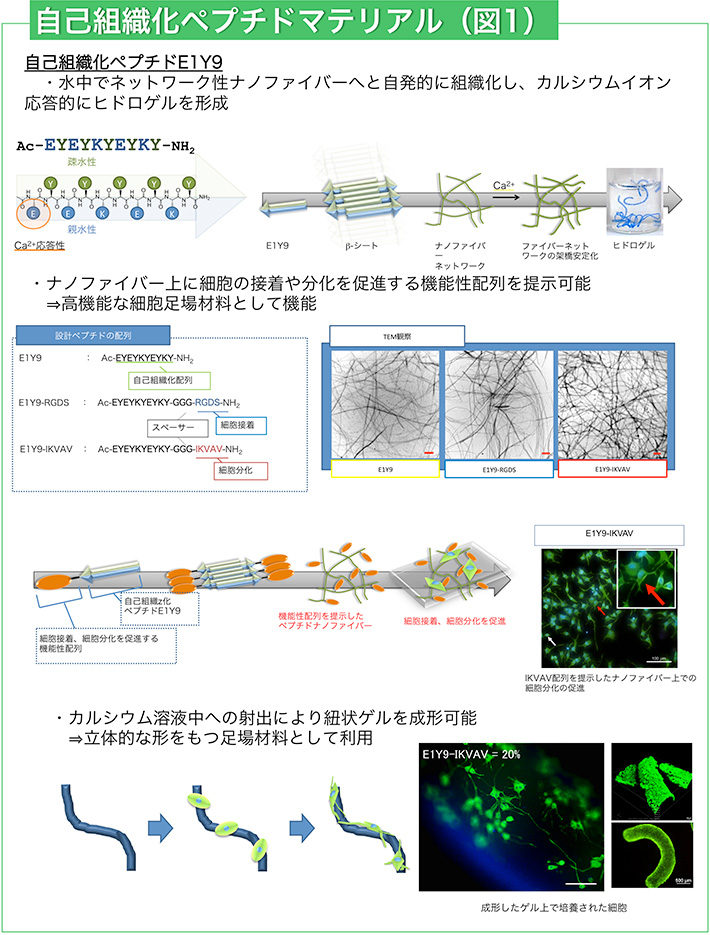
静電相互作用や疎水性相互作用などの相互作用を利用すると、水中で自発的に規則正しく集合してさまざまな構造体を組み上げるペプチドを設計することができます。これまでに水中でβ-シート構造をとって自己組織化し、ナノメートルサイズの繊維(ナノファイバー)へと集合化するペプチドE1Y9を設計しています(図1)。
E1Y9はカルシウムイオン(Ca2+)と相互作用することでナノファイバーが絡み合ったネットワーク構造が安定化し、水分子をトラップすることで「ゲル(ジェル)」になるという面白い特性を発揮します。
このようなゲルは細胞が増殖・成長するために必要な環境を提供することができ、体外で細胞を培養するのに適した材料として再生医療などへの応用が考えられます。例えば、細いヒモ状に成形したペプチドゲルの上で神経様細胞を培養し、神経突起を伸ばした状態に誘導することができています(図1)。
この自己組織化ペプチドでつくる細胞足場材料上で、さまざまな組織に分化する幹細胞の培養も行っています。
2. 細胞膜透過能をもったα-ヘリックスペプチドの創製とドラッグデリバリー応用
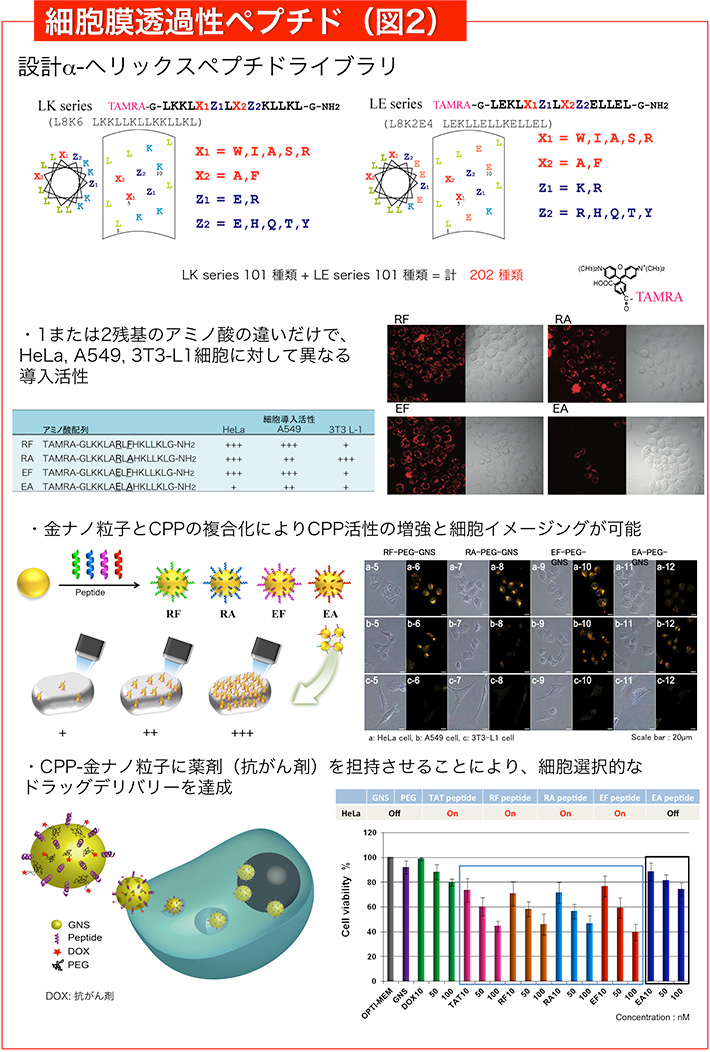
細胞は中と外を区別する膜(細胞膜)につつまれており、栄養素などの細胞に必要なもの以外の分子は通常この膜を通過できません。近年、設計次第で細胞膜を透過するペプチドをつくることが可能であることがわかってきました。これまでにα-ヘリックス構造をつくるペプチド配列中のアミノ酸をさまざまに置換したペプチドライブラリを設計し、その中から細胞膜を透過して自発的に細胞の中に入るペプチドを見つけています(図2)。
中でも、正常な細胞とがん細胞を見分けてがん細胞に選択的に入るペプチドは将来的に抗がん剤などの薬物を効率よく送達するドラッグデリバリーにおいて有効です。
実際に、このようながん細胞選択性をもった膜透過ペプチドと金の微小な粒子(ナノ粒子)を組み合わせて、金ナノ粒子表面に抗がん剤をもたせて、がん細胞へのデリバリーなどを行っています(図2)。
また、より高いがん細胞選択性や膜透過性をもったペプチドを開発する研究も進めています。
3. 糖ペプチドライブラリを利用したレクチン結合性リガンドとレクチン検出プローブの創製
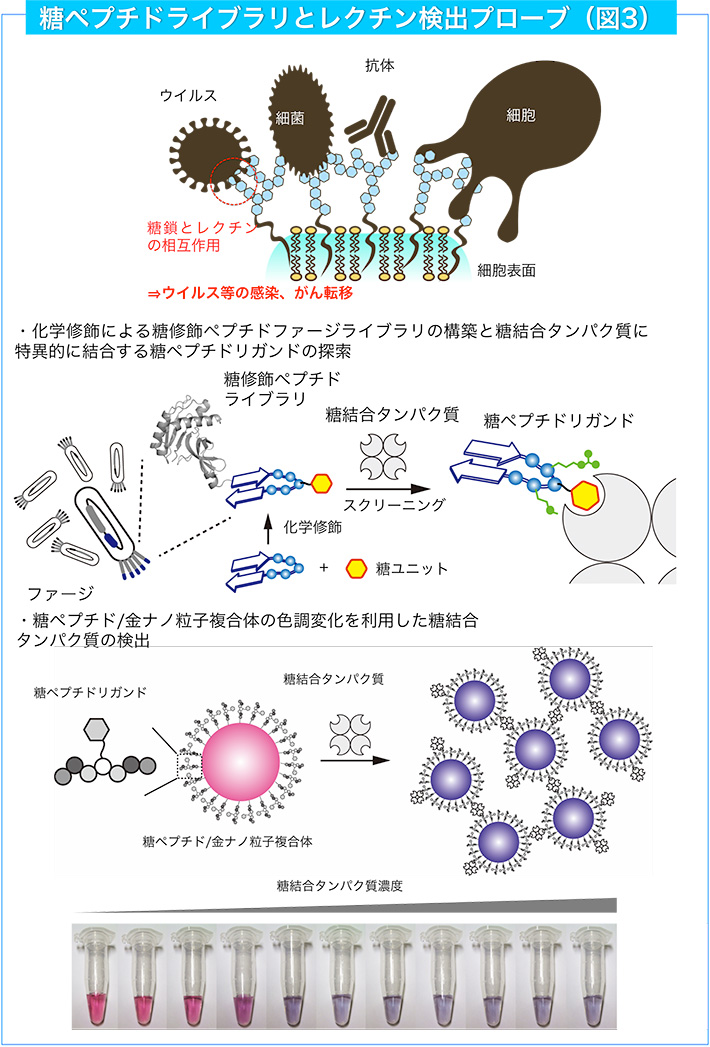
糖はペプチド・タンパク質と並んで生命現象を支える重要な分子です。栄養源としてのグルコースなどの糖分子の他にも、多数の糖が複雑につながった糖鎖が細胞やウイルス・細菌の表面に存在しています。
細胞の表面にはこれらの糖鎖を結合するレクチンと呼ばれるタンパク質も存在しており、ウイルス・細菌の感染やがんの転移といった疾病と深く関わっています。そこで、糖とペプチドを組み合わせた分子「糖ペプチド」を設計してレクチンを検出する研究を行っています。糖とペプチドを組み合わせることで、複雑な糖鎖と同等かそれ以上の能力を発揮してレクチンと結合すると期待しています。これまでに、遺伝子工学的手法(ファージライブラリ)と有機化学的手法(糖修飾)を組み合わせることにより糖ペプチドライブラリを構築し、その中からレクチンに選択的かつ強く結合する優れた糖ペプチドリガンドの獲得に成功しています(図3)。
また、糖ペプチドを金ナノ粒子の上に多数集積したナノ粒子複合体は、レクチンと結合して凝集体を形成します。ステンドグラスの鮮やかな赤色のもととして知られている金ナノ粒子の溶液は、凝集前は赤色ですが凝集すると青色になります。つまり、レクチンを金ナノ粒子溶液の色の変化として検出することが可能です。
糖ペプチドを利用することで高感度の検出が可能になりました(図3)。
研究成果
代表論文
- [1] K. Fukunaga, H. Tsutsumi, H. Mihara. Cell Differentiation on Disk- and String-Shaped Hydrogels Fabricated from Ca2+-responsive Self-Assembling Peptides. Biopolymers (Pept. Sci), 2016, 106, 476-483.
- [2] H. Tsutsumi, K. Nakano, H. Mihara. Dihydrofolate Reductase Inhibitory Peptides Screened from a Structured Design β-Loop Peptide Library Displayed on Phage. Mol. BioSyst., 2015, 11, 2713-2716.
- [3] J. Yang, T. Furuta, M. Sakurai, H. Tsutsumi, H. Mihara. A Computational Study of the Interaction of Amphiphilic α-Helical Cell-Penetrating Peptides with Heparan Sulfate. Bull. Chem. Soc. Jpn., 2014, 87, 1074-1082.
- [4] K. Usui, T. Kikuchi, K. Kikuchi, M. Mie, E. Kobatake, H. Mihara. Cellular Differentiation Assessments by Measuring the Degree of Cellular Internalization and Membrane Adsorption Using Designed Peptides. Bioorg Med Chem Lett, 2014, 24, 4129-4131.
- [5] J. Yang, H. Tsutsumi, T. Furuta, M. Sakurai, H. Mihara. Interaction of Amphiphilic α-Helical Cell-Penetrating Peptides with Heparan Sulfate. Org. Biomol. Chem., 2014, 12, 4673-4681.
- [6] H. Park, H. Tsutsumi, H. Mihara. Cell-Selective Intracellular Drug Delivery Using Doxorubicin and α-Helical Peptides Conjugated to Gold Nanoparticles. Biomaterials, 2014, 35, 3480-3487.
- [7] K. Usui, T. Kikuchi, KY. Tomizaki, T. Kakiyama, H. Mihara. A Novel Array Format for Monitoring Cellular Uptake Using a Photo-Cleavable Linker for Peptide Release. Chem. Commun., 2013, 49, 6394-6396.
- [8] H. Tsutsumi, H. Mihara. Self-Assembly of Designed Peptides and Their Nanomaterials Applications. Amino Acids, Peptides and Proteins, ed. E. Farkas and M. Ryadnov, Royal Society of Chemistry Publishing, Cambridge, UK, 2013, vol. 38, pp. 122-150.
- [9] H. Tsutsumi, H. Mihara. Soft Materials Based on Designed Self-Assembling Peptides: from Design to Application. Mol. BioSyst., 2013, 9, 609-617.
- [10] K. Fukunaga, H. Tsutsumi, H. Mihara. Self-Assembling Peptide Nanofibers Promoting Cell Adhesion and Differentiation. Biopolymers (Pept. Sci), 2013, 100, 731-737.
- [11] K. Arai, H. Tsutsumi, H. Mihara. A Monosaccharide-Modified Peptide Phage Library for Screening of Ligands to Carbohydrate-Binding Proteins. Bioorg. Med. Chem. Lett., 2013, 23, 4940-4943.
- [12] H. Park, H. Tsutsumi, H. Mihara. Cell Penetration and Cell-Selective Drug Delivery Using α-Helix Peptides Conjugated with Gold Nanoparticles. Biomaterials, 2013, 34, 4872-4879.
- [13] K. Usui, T. Kikuchi, M. Mie, E. Kobatake, H. Mihara. Systematic Screening of the Cellular Uptake of Designed Alpha-Helix Peptides. Bioorg. Med. Chem., 2013, 21, 2560-2567.
- [14] H. Tsutsumi, H. Ohkusa, H. Park, T. Takahashi, H. Yuasa, H. Mihara. Gold Nanoparticles Conjugated with Monosaccharide-modified Peptide for Lectin Detection. Bioorg. Med. Chem. Lett., 2012, 22, 6825-6827.
- [15] T. Sawada, M. Tsuchiya, T. Takahashi, H. Tsutsumi, H. Mihara. Cell-Adhesive Hydrogels Composed of Peptide Nanofibers Responsive to Biological Ions. Polymer J., 2012, 44, 651-657.
- [16] T. Sawada, H. Mihara. Dense Surface Functionalization Using Peptides that Recognize Differences in Organized Structures of Self-assembling Nanomaterials. Mol. BioSyst., 2012, 8, 1264-1274.
- [17] A. Syahir, K. Kajikawa, H. Mihara. Sensitive Detection of Small Molecule-Protein Interactions on a Metal-Insulator-Metal Label-Free Biosensing Platform. Chem. Asia. J., 2012, 7, 1867-1874.
- [18] K. Usui, T. Kakiyama, K. Tomizaki, M. Mie, E. Kobatake, H. Mihara. Cell Fingerprint Patterns Using Designed α-Helical Peptides to Screen for Cell-Specific Toxicity. Bioorg. Med. Chem. Lett., 2011, 21, 6281-6284.
- [19] T. Sawada, K. Ishiguro, T. Takahashi, H. Mihara. A Novel β-loop Scaffold of Phage-Displayed Peptides for Highly Specific Affinities. Mol. BioSyst., 2011, 7, 2558-2562.
- [20] A. Miyachi, T. Takahashi, S. Matsumura, H. Mihara. Peptide Nanofibers Modified with a Protein by Using Designed Anchor Molecules Bearing Hydrophobic and Functional Moieties. Chem. Eur. J., 2010, 16, 6644-6650.
- [21] T. Sawada, T. Takahashi, H. Mihara. Affinity-Based Screening of Peptides Recognizing Assembly States of Self-Assembling Peptide Nanomaterials. J. Am. Chem. Soc., 2009, 131, 14434-14441.
- [22] K. Usui, K.-Y. Tomizaki, H. Mihara. Screening of α-Helical Peptide Ligands Controlling a Calcineurin-phosphatase Activity. Bioorg. Med. Chem. Lett., 2007, 17, 167-17
- [23] S. Matsumura, S. Uemura, H. Mihara. Metal-triggered Nanofiber Formation of His-containing β-sheet Peptide. Suplamolc. Chem., 2006, 18, 397-403.
- [24] K. Usui, T. Ojima, K.-Y. Tomizaki,, H. Mihara. A Designed Glycopeptide Array for Characterization of Sugar-Binding Proteins Toward a Glycopeptide Chip Technology. NanoBiotechnology, 2005, 1, 191-200.
- [25] S. Matsumura, S. Uemura, H. Mihara. Construction of biotinylated peptide nanotubes for arranging proteins. Mol. BioSyst., 2005, 1, 146-148.
著書
- [1] 堤浩、三原久和 第Ⅰ編 第2章 自己組織化現象を利用したペプチド性足場材料の開発 再生医療用足場材料の開発と市場、2016年、シーエムシー出版
- [2] 臼井健二、堤浩、三原久和 第2章 タンパク質チップ, ペプチドチップ. 9. 生体分子解析・細胞解析に向けた設計ペプチドチップ、伊藤嘉浩 監修、バイオチップの基礎と応用-原理から最新の研究・開発動向まで-、2015 年、シーエムシー出版
- [3] 三原久和 設計ペプチドライブラリーを利用するタンパク質・細胞分析チップ. 最新ペプチド合成技術とその創薬研究への応用、メディカルドウ、2012年、323-238
- [4] 臼井健二、富崎欣也、三原久和 “オミクス”研究に向けた設計ペプチドアレイの構築. 分析化学、2012年、61(6)、523-534
- [5] 臼井健二、菊池卓哉、三原久和 タンパク質・細胞分析用デザインペプチドチップ. シングルセル解析の最前線(神原秀記、松永是、植田充美監修)、シーエムシー出版、2010年、17-24
教員紹介
三原久和 教授 理学博士
| 1986年3月 | 九州大学 大学院理学研究科 化学専攻 博士課程修了 |
|---|---|
| 1986年 | 日本学術振興会 特別研究員 |
| 1986 - 1988年 | 米国ロックフェラー大学 博士研究員 |
| 1988 - 1993年 | 九州工業大学 工学部 助手 |
| 1993 - 1995年 | 長崎大学 工学部 助教授 |
| 1995 - 2005年 | 東京工業大学 大学院生命理工学部 助教授 東京工業大学 大学院生命理工学研究科 准教授 |
| 2005年より | 現職 |
| 1998 - 2005年 | 科学技術振興機構 さきがけ・SORST研究員を兼任 |
| 2001年 | 手島記念研究賞研究論文賞 |
|---|---|
| 2005年 | 英国王立科学会FELLOW(FRSC) |
| 2009年 | バイオインダストリー協会賞 |
| 2011年 | 東工大教育賞 |
| 2015年 | 日本化学会学術賞 |
- 教育活動
- 学部:生物化学第一(生命工学科)、生命理工学課題解決演習第一(生命工学科)、生命工学基礎実験第一(生命工学科)、生物有機科学(生物工学コース)、生命工学総合実験第一(生物工学コース)
大学院:大学院有機化学、Advanced Course of Bioorganic Engineering(生物プロセス専攻)
- 所属学会
- 日本化学会、日本ペプチド学会(理事)、高分子学会、Royal Society of Chemistry
堤浩 准教授 博士(工学)
| 1999年 | 東京工業大学 生命理工学部 卒業 |
|---|---|
| 2004年 | 東京工業大学 大学院生命理工学研究科 後期博士課程修了 博士(工学)を取得 |
| 2004 - 2005年 | 九州大学 先導物質化学研究所・京都大学 大学院工学研究科 さきがけ博士研究員 |
| 2005 - 2007年 | 東京医科歯科大学 生体材料工学研究所 特任助手 |
| 2007 - 2009年 | 同 助教 |
| 2009 - 2011年 | 京都大学 大学院工学研究科 特定研究員 |
| 2011 - 2016年 | 東京工業大学 大学院生命理工学研究科 助教 |
| 2016年より | 現職 |
| 2013年 | 平成25年度ペプチド学会奨励賞受賞 |
|---|---|
| 2014年 | 平成26年度竹田国際貢献賞受賞 |
- 所属学会
- 日本化学会 日本ペプチド学会 高分子学会
教員からのメッセージ
- 三原教授より
-
最先端研究を通じて、自分の能力を伸ばしましょう。
三原研モットー:3J(自己増進、自己責任、自己安全) - 堤准教授より
-
三原・堤研では、ペプチドを自在に設計して分子ツールを創り出し、タンパク質や細胞の機能の制御などに取り組んでいます。設計ペプチドを化学合成したり、大腸菌などを用いて100万種類以上のペプチドから成るライブラリを生合成させたりして、その中からさまざまな機能をもつペプチドを探索し、分子ツールとして利用しています。ケミストリーとバイオロジーの両方に興味のある学生さんは一緒に面白い研究をしましょう!
お問い合わせ先
教授 三原久和
すずかけ台キャンパス B1棟 801号室
E-mail : hmihara@bio.titech.ac.jp
准教授 堤浩
すずかけ台キャンパス B1棟 802号室
E-mail : htsutsum@bio.titech.ac.jp
※この内容は掲載日時点の情報です。最新の研究内容については研究室サイト![]() をご覧ください。
をご覧ください。